
【題目】用含有Al2O3、SiO2和少量FeO·xFe2O3的鋁灰制備Al2(SO4)3·18H2O,工藝流程如下(部分操作和條件略):
Ⅰ.向鋁灰中加入過量稀H2SO4,過濾;
Ⅱ.向溶液中加入過量KMnO4溶液,調節溶液的pH約為3;
Ⅲ.加熱,產生大量棕色沉淀,靜置,上層溶液呈紫紅色;
Ⅳ.加入MnSO4至紫紅色消失,過濾;
Ⅴ.濃縮、結晶、分離,得到產品。
(1)H2SO4溶解Al2O3的離子方程式是:_____________________________________。
(2)將MnO4-氧化Fe2+的的離子方程式補充完整:_____
![]()
(3)己知:生成氫氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
開始沉淀時 | 3.4 | 6.3 | 1.5 |
完全沉淀時 | 4.7 | 8.3 | 2.8 |
注意:金屬離子的起始濃度為0.1mol·L-1。
根據表中數據解釋步驟Ⅱ的目的_______________________________。
(4)已知:一定條件下,MnO4-可與Mn2+反應生成MnO2。
①向Ⅲ的沉淀中加入濃HCl并加熱,能說明沉淀中存在MnO2的現象是_______________。
②Ⅳ中加入MnSO4的目的是_______________________________________。
【答案】 Al2O3+6H+=2Al3++3H2O 5 8 H+ 5 4 H2O pH約為3時,Fe2+和Al3+不能形成沉淀,將Fe2+氧化為Fe3+,可使鐵完全沉淀 生成黃綠色氣體 除去過1的MnO4-
【解析】(1)硫酸溶解氧化鋁生成硫酸鋁和水,反應的離子方程式為:Al2O3+6H+=2Al3++3H2O;(2)高錳酸根離子在酸溶液中被還原為錳離子,亞鐵離子被氧化為鐵離子,反應的離子方程式為:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O,故答案為:1、5;8H+;1、5;4H2O;(3)向濾液中加入過量KMnO4溶液,目的是氧化亞鐵離子為三價鐵離子,依據圖表數據分析可知,鐵離子開始沉淀和沉淀完全的溶液pH為1.5--2.8,鋁離子和亞鐵離子開始沉淀的溶液pH大于3,所以調節溶液的pH約為3,可以使鐵離子全部沉淀,鋁離子不沉淀分離;故答案為:pH約為3時,Fe2+和Al3+不能形成沉淀,將Fe2+氧化為Fe3+,可使鐵完全沉淀;(4)一定條件下,MnO4-可與Mn2+反應生成MnO2,①向Ⅲ的沉淀中加入濃HCl并加熱,二氧化錳和濃鹽酸在加熱條件下反應生成氯化錳、氯氣和水,生成的氯氣是黃綠色氣體,能說明沉淀中存在MnO2的現象是生成黃綠色氣體;②MnO4-可與Mn2+反應生成MnO2,過濾除去,所以可以利用MnSO4的溶液和高錳酸鉀溶液反應生成二氧化錳,把過量高錳酸根離子除去;


科目:高中化學 來源: 題型:
【題目】夾緊下列裝置中的彈簧夾并進行相關操作。下列情形中,表明相應裝置漏氣的是( )
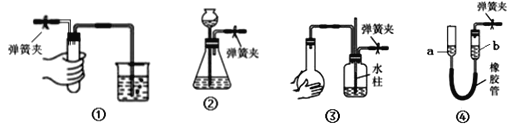
A. 裝置①中,用手捂住試管,燒杯中出現氣泡,放開手后,導管中形成一段穩定的水柱
B. 裝置②中,向長頸漏斗中加入一定量水,形成水柱,隨后水柱下降至與瓶中液面相平的位置
C. 裝置③中,雙手捂住燒瓶,導管中形成一段穩定的水柱,雙手放開后,水柱慢慢回落
D. 裝置④中,將a管向上提至一段高度,a、b兩管之間水面形成穩定的高度差
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32﹣、SO42﹣、NO3﹣中的幾種.①若加入鋅粒,產生無色無味無毒的氣體;②若加入NaOH溶液,產生白色沉淀,且產生的沉淀的物質的量與加入NaOH的物質的量之間的關系如圖所示.則下列說法正確的是( )

A. 溶液中的陽離子只有H+、Mg2+、Al3+
B. 溶液中一定不含CO32﹣,一定含有SO42﹣和NO3﹣
C. 溶液中n(NH4+)=0.2 mol
D. 三種離子的物質的量之比n(H+):n(Al3+):n(Mg2+)=1:1:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將0.2molMnO2和50ml 12mol/L鹽酸混合后充分加熱,反應完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀的物質的量為(不考慮鹽酸的揮發) ( )
A、等于0.3mol B、小于0.3mol C、大于0.3mol,小于0.6mol D、等于0.6mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟他胺G是一種可用于治療腫瘤的藥物。實驗室由芳香烴A制備G的合成路線如下:

回答下列問題:
(1)A的結構簡式為____________。C的化學名稱是______________。
(2)③的反應試劑和反應條件分別是____________________,該反應的類型是__________。
(3)⑤的反應方程式為_______________。吡啶是一種有機堿,其作用是____________。
(4)G的分子式為______________。
(5)H是G的同分異構體,其苯環上的取代基與G的相同但位置不同,則H可能的結構有______種。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精細化工中間體,寫出由苯甲醚(
)是重要的精細化工中間體,寫出由苯甲醚(![]() )制備4-甲氧基乙酰苯胺的合成路線___________(其他試劑任選)。
)制備4-甲氧基乙酰苯胺的合成路線___________(其他試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖a為在恒溫恒容密閉容器中分別充入X、Y、Z三種氣體,一定條件下發生反應,各物質濃度隨時間的變化。若從t2開始,每個時刻只改變一個且不同的條件,物質Z 的正、逆反應速率隨時間變化如圖b。下列說法不正確的是( )

A. 0~t1min內X與Y的平均反應速率之比為3:2
B. t2時刻改變的條件可能是壓強或催化劑
C. 該反應的正反應為放熱反應
D. 該反應中Z一定為產物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下是實驗室常用的部分儀器,請回答下列問題

(1)序號為⑩的儀器的名稱為______________;
(2)能作反應容器且可直接加熱的儀器是上述中的___________(填名稱);
(3)儀器上標有溫度的是_________(填序號);
(4)若用CCl4 提取碘水中的碘,必須用到上述儀器中的_________(填序號),試描述靜置后的現象_____________________________________________;
(5)甲同學想用如下圖裝置,以大理石和稀鹽酸反應制取CO2。老師指出,這需要太多的稀鹽酸,造成浪費。該同學選用了上述①~⑩中的一種儀器,加在裝置上,解決了這個問題。丙同學采用的方法是___________________________;

(6)乙同學也想制取CO2氣體,而實驗室只有H2SO4、濃HNO3、水、塊狀純堿、塊狀石灰石,比較合理的方案應選用的藥品是__________________________________;

(7)丙同學在沒有現成的CO2氣體發生器的情況下,選用下圖中的部分儀器,裝配成一個簡易的、能隨用隨停的CO2氣體發生器,應選用的儀器是________(填編號)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組探究SO2和Fe(NO3)3溶液的反應,其反應裝置如下圖所示:

已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1,請回答下列問題:
(1)裝置A中反應的化學方程式是______________________________________
(2)為排除空氣對實驗的干擾,滴加濃硫酸之前應進行的操作是______________________________________________________
(3)裝置B中產生了白色沉淀,其成分是 _________ ,說明SO2具有_______ 性。
(4)分析B中產生白色沉淀的原因:
猜想1:_____________________________________________________________;
猜想2:SO2與Fe3+反應;
猜想3:在酸性條件下SO2與NO3—反應;
①按猜想2,裝置B中反應的離子方程式是 _____________________________________。
②按猜想3,只需將裝置B中的Fe(NO3)3溶液替換為等體積的下列溶液,在相同條件下進行實驗。應選擇的試劑是 ________(填字母)。
a.0.1 mol·L-1硝酸鈉溶液 b.1.5 mol·L-1Fe(NO3)2溶液
c.6.0 mol·L-1 NaNO3和0.2 mol·L-1鹽酸等體積混合的溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com