
【題目】一種利用電解錳陽極泥(主要成分MnO2、MnO)制備MnO2的工藝流程如下:
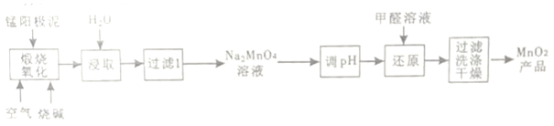
(1)“煅燒氧化”時,1mol MnO煅燒完全轉化為Na2MnO4失去電子的物質的量為___________;MnO2煅燒反應的化學方程式為__________________。
(2)“浸取”時,為提高Na2MnO4的浸取率,可采取的措施有____________、____________(列舉2點)
(3)“調pH”是將溶液pH 調至約為10,防止pH較低時Na2MnO4自身發生氧化還原反應,生成MnO2和___________;寫出用pH試紙測定溶液pH的操作_______________。
(4)“還原”時有無機含氧酸鹽生成,發生反應的化學方程式為_____________。
(5)測定產品中MnO2質量分數的步驟如下:
步驟1. 準確稱取mg產品,加入c1mol·L-1Na2C2O4溶液V1mL (過量)及適量的稀硫酸,水浴加熱煮沸一段時間。(已知:Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4)
步驟2. 然后用c2mol·L-1KMnO4標準溶液滴定剩余的Na2C2O4滴定至終點時消耗KMnO4標準溶液V2mL。(已知:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
步驟2達滴定終點時判斷依據是_____________;產品中MnO2的質量分數為ω(MnO2)=____________(列出計算的表達式即可)。
【答案】 4mol 2MnO2+4NaOH+O2![]() 2Na2MnO4+2H2O 煅燒后固體進行粉碎,適量增大水的量 適當提高浸取溫度,充分攪拌 MnO4-(或NaMnO4) 取一小段pH試紙置于表面皿(點滴板上)中,用玻璃棒蘸取試液滴在pH試紙上,立刻與標準比色卡對照讀出pH 2Na2MnO4+HCHO=2MnO2↓+Na2CO3+2NaOH 滴入最后一滴KMnO4溶液時,溶液呈淺紅色且30s內不褪去
2Na2MnO4+2H2O 煅燒后固體進行粉碎,適量增大水的量 適當提高浸取溫度,充分攪拌 MnO4-(或NaMnO4) 取一小段pH試紙置于表面皿(點滴板上)中,用玻璃棒蘸取試液滴在pH試紙上,立刻與標準比色卡對照讀出pH 2Na2MnO4+HCHO=2MnO2↓+Na2CO3+2NaOH 滴入最后一滴KMnO4溶液時,溶液呈淺紅色且30s內不褪去 ![]() ×100%
×100%
【解析】 (1)“煅燒氧化”時MnO![]() Na2MnO4錳由+2價變成+6價,失去電子為4e- ,1mol MnO煅燒完全失去電子的物質的量為4mol;MnO2煅燒反應的化學方程式為2MnO2+4NaOH+O2
Na2MnO4錳由+2價變成+6價,失去電子為4e- ,1mol MnO煅燒完全失去電子的物質的量為4mol;MnO2煅燒反應的化學方程式為2MnO2+4NaOH+O2![]() 2Na2MnO4+2H2O。
2Na2MnO4+2H2O。
(2)“浸取”時,為提高Na2MnO4的浸取率,就是增大化學反應速率,所以可采取的措施有:煅燒后固體進行粉碎,增大接觸面積,適量增大水的量促進溶解,;適當提高浸取溫度,加快化學反應速率,充分攪拌讓物質充分迅速
(3)Na2MnO4中Mn的化合價為+6 ,MnO2中Mn的化合價為+4, Na2MnO4自身發生氧化還原反應,Mn的化合價為要升高,即發生MnO2 ![]() Na2MnO4
Na2MnO4 ![]() MnO4_,所以能生成MnO2,MnO4-(或NaMnO4)
MnO4_,所以能生成MnO2,MnO4-(或NaMnO4)
用pH試紙測定溶液pH的操作操作為(6). 取一小段pH試紙置于表面皿(點滴板上)中,用玻璃棒蘸取試液滴在pH試紙上,立刻與標準比色卡對照讀出pH 。答案:MnO4-(或NaMnO4) 取一小段pH試紙置于表面皿(點滴板上)中,用玻璃棒蘸取試液滴在pH試紙上,立刻與標準比色卡對照讀出pH 。
(4)由 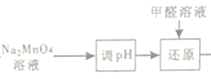 “還原指Na2MnO4與甲醛反應,發生反應的化學方程式為2Na2MnO4+HCHO=2MnO2↓+Na2CO3+2NaOH。
“還原指Na2MnO4與甲醛反應,發生反應的化學方程式為2Na2MnO4+HCHO=2MnO2↓+Na2CO3+2NaOH。
(5)達滴定終點時判斷依據是:滴入最后一滴KMnO4溶液時,溶液呈淺紅色且30s內不褪去。
由5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
5 2
X c2v2 X=![]() = 2.5C2V2
= 2.5C2V2
由Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4
1 1
C1V1-2.5C2V2 Y Y= (C1V1-2.5C2V2)mol
產品中MnO2的質量分數為m(MnO2)= (C1V1-2.5C2V2)mol![]() 87g/mol=87 (C1V1-2.5C2V2)/1000g
87g/mol=87 (C1V1-2.5C2V2)/1000g
產品中MnO2的質量分數為ω(MnO2)= 87(C1V1-2.5C2V2)/1000m![]() 100
100![]()


科目:高中化學 來源: 題型:
【題目】Ⅰ.明礬石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,還含有少量Fe2O3雜質。利用明礬石制備氫氧化鋁的流程如下:

(1)焙燒爐中Al2(SO4)3與硫磺反應生成一種能使品紅溶液褪色的物質和一種具有兩性的物質,寫出該反應化學方程式______________________________________________________。
(2)試劑X最好為下列試劑中的_________
A.NaOH B.CO2 C.鹽酸 D.氨水
熟料溶解時,發生反應的離子方程式為_____________________________________。
(3)母液中溶質主要成分的化學式為__________。溶液調節pH后經過濾、洗滌可得Al(OH)3沉淀,證明沉淀已洗滌干凈的實驗操作和現象是_______________________________________________。
Ⅱ. 有100ml某透明溶液,可能含有以下離子中的若干種:Mg2+、Cu2+、Fe2+、Al3+、NH4+、K+、HCO3-、SO42-。當加入一種淡黃色粉末狀固體物質時,有刺激性氣味的混合氣體放出,同時生成白色沉淀。當加入0.6mol淡黃色粉末時,共收集到0.8mol混合氣體,且此時生成的沉淀最多。此后繼續加入淡黃色粉末時,沉淀量逐漸減少,至加入0.65mol粉末后,沉淀量由0.3mol減少至0.2mol,再加入粉末后,沉淀就不再減少。由此實驗現象及數據判斷:
(4)淡黃色粉末為_________________;
(5)溶液中肯定有__________________離子;
(6)溶液中陽離子按量由少到多其物質的量之比為______________(H+及沒有確定的離子除外)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA為阿伏加德羅常數的值,下列說法正確的是
A. 標準狀況下,2.24L乙烷與2.24L苯含C-H鍵數均為0.6NA
B. 16.8gFe與足量的水蒸氣加熱充分反應,轉移電子數為0.8NA
C. 25C時,1LpH=7的CH3COONH4溶液中含NH4+數一定為1.0×10-7NA
D. 0.2molCO2與0.1molC在密閉容器中充分反應生成CO分子數為0.2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列有機物:
① CH2=CH2 ②![]()
③ CH3CH(OH)CH2CH3 ④ (CH3)2C=CH2
⑤ CH3CH2OCH2CH3 ⑥ CH3CH=CHCH=CHCOOH
(1)屬于羧酸的是_____(填序號)。
(2)與③互為同分異構體的是_____(填序號)。
(3)與①互為同系物的是_____(填序號)。
(4)用系統命名法給④命名,其名稱為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室需用![]() 的硫酸銅溶液,以下操作正確的是
的硫酸銅溶液,以下操作正確的是![]()
![]()
A. 將![]() 膽礬配成500mL溶液
膽礬配成500mL溶液
B. 將![]() 膽礬溶于少量水中,再用水稀釋至500mL
膽礬溶于少量水中,再用水稀釋至500mL
C. 稱取![]() 硫酸銅,加入500mL水
硫酸銅,加入500mL水
D. 在![]()
![]() 溶液中加入400mL水
溶液中加入400mL水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是幾種常見有機物之間的轉化關系,下列有關說法正確的是( )
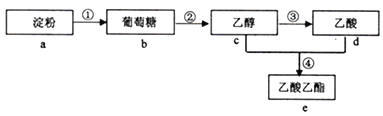
A. 反應①、②、③、④均屬于取代反應
B. 反應④的條件為:稀硫酸,加熱
C. 與d含有相同官能團的e的同分異構體只有1種
D. a遇碘單質變藍,b能與銀氨溶液水浴加熱條件下反應析出銀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是石蠟油在熾熱碎瓷片的作用下產生C2H4,并檢驗C2H4性質的實驗,完成下列各題。

(1)B 中溶液褪色,原因是______________
(2)C 中反應的化學方程式為_____________
(3)在D 處點燃時必須進行的操作是___________,D 處反應的化學方程式為______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗需要![]() NaOH溶液475mL和
NaOH溶液475mL和![]() 硫酸溶液
硫酸溶液![]() 根據這兩種溶液的配制情況回答下列問題:
根據這兩種溶液的配制情況回答下列問題:
(1)如圖所示的儀器中配制溶液肯定不需要的是______![]() 填序號
填序號![]() ,配制上述溶液還需用到的玻璃儀器是______
,配制上述溶液還需用到的玻璃儀器是______![]() 填儀器名稱
填儀器名稱![]() .
.

(2)下列操作中,不能用容量瓶實現的有______![]() 填序號
填序號![]() .
.
A.配制一定體積準確濃度的標準溶液
B.量取一定體積的液體
C.測量容量瓶規格以下的任意體積的液體
D.準確稀釋某一濃度的溶液
E.貯存溶液
F.用來加熱溶解固體溶質
(3)根據計算用托盤天平稱取NaOH的質量為______![]() 在實驗中其他操作均正確,若定容時俯視刻度線,則所得溶液濃度______
在實驗中其他操作均正確,若定容時俯視刻度線,則所得溶液濃度______![]() 填”大于”、“等于”或“小于”,下同
填”大于”、“等于”或“小于”,下同![]() 若定容時,有少許蒸餾水灑落在容量瓶外,則所得溶液濃度______
若定容時,有少許蒸餾水灑落在容量瓶外,則所得溶液濃度______![]() .
.
(4)根據計算得知,所需質量分數為![]() 、密度為
、密度為![]() 的濃硫酸的體積為______
的濃硫酸的體積為______![]() 計算結果保留一位小數
計算結果保留一位小數![]() 如果實驗室有10mL、15mL、20mL、50mL量筒,選用______mL量筒最好.
如果實驗室有10mL、15mL、20mL、50mL量筒,選用______mL量筒最好.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:S(g) + O2 (g) = SO2(g) ΔH=-Q1kJ/mol ; S(s) + O2 (g) = SO2(g) ΔH=-Q2 kJ/mol。 則Q1 Q2
A. 大于 B. 小于 C. 等于 D. 無法比較
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com