
 (1)黑火藥爆炸時,發生的反應之一為:S+2KNO3+3C$\stackrel{引燃}{→}$K2S+3CO2↑+N2↑,該反應中氧化劑為S、KNO3,1molS能氧化C0.5mol
(1)黑火藥爆炸時,發生的反應之一為:S+2KNO3+3C$\stackrel{引燃}{→}$K2S+3CO2↑+N2↑,該反應中氧化劑為S、KNO3,1molS能氧化C0.5mol分析 (1)該反應中S元素化合價由0價變為-2價、N元素化合價由+5價變為0價、C元素化合價由0價變為+4價,得電子化合價降低的反應物是氧化劑,根據S和C之間的關系式計算;
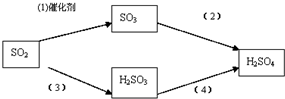
(2)二氧化硫和氧氣在催化劑、加熱條件下發生反應生成三氧化硫;
二氧化硫具有氧化性,能氧化硫化氫生成淡黃色固體S;
減少酸雨產生的途徑是脫硫、開發新能源、減少煤的燃燒等.
解答 解:(1)該反應中S元素化合價由0價變為-2價、N元素化合價由+5價變為0價、C元素化合價由0價變為+4價,得電子化合價降低的反應物是氧化劑,所以S、KNO3作氧化劑;
1molS得到2mol電子,轉移2mol電子需要0.5molC,
故答案為:S、KNO3;0.5;
(2)二氧化硫和氧氣在催化劑、加熱條件下發生反應生成三氧化硫,反應方程式為2SO2+O2$\frac{\underline{\;催化劑\;}}{\;}$2 SO3;
二氧化硫具有氧化性,能氧化硫化氫生成淡黃色固體S,且同時生成水,所以瓶壁有淡黃色粉末和無色的小液滴,反應方程式為SO2+2H2S=3 S↓+2H2O,減少酸雨產生的途徑是脫硫、開發新能源、減少煤的燃燒等,故選C,
故答案為:2SO2+O2$\frac{\underline{\;催化劑\;}}{\;}$2 SO3;瓶壁有淡黃色粉末和無色的小液滴;SO2+2H2S=3 S↓+2H2O;C.
點評 本題以二氧化硫為載體考查氧化還原反應、化學方程式的書寫、二氧化硫性質、環境污染等知識點,側重考查基本理論,注意(1)中硫還原C的物質的量的計算,為易錯點.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ③④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A和M的原子序數之差為6 | |
| B. | A和M原子的最外層電子數之差為7 | |
| C. | A和M原子的最外層電子數之和可能為9 | |
| D. | A和M原子的電子總數之和可能為11 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稀硝酸與氫氧化鉀溶液反應 H++OH-→H2O | |
| B. | 鋁與稀鹽酸反應 Al+2H+→Al3++H2↑ | |
| C. | 氯化鐵溶液與氫氧化鈉溶液反應 FeCl3+3OH-→Fe(OH)3↓+3C1- | |
| D. | 二氧化碳與石灰水反應 CO2+2OH-→CO32-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v(X)=0.5mol•s-1 | B. | v(X)=0.025mol•L-1•s-1 | ||
| C. | v(y)=0.05mol•L-1•s-1 | D. | v(y)=0.075mol•L-1•s-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲苯能使酸性高錳酸鉀溶液褪色,而甲烷不能 | |
| B. | 乙醇電離出H+的能力不及H2O | |
| C. | 乙烯能發生加成反應,而乙烷不能發生加成反應 | |
| D. | 苯酚能與NaOH溶液反應,而乙醇不能與NaOH溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 甲燒杯中鋅片逐漸溶解,乙燒杯中鋅片不溶解 | |
| B. | 兩燒杯中銅片表面均無氣泡產生 | |
| C. | 兩燒杯中溶液的酸性均減弱 | |
| D. | 甲燒杯中銅片上的電極反應為:Cu2++2e-=Cu |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 發展水電,開發新能源,如核能、太陽能、風能等,減少對礦物能源的依賴 | |
| B. | 限制化學發展,關停化工企業,消除污染源頭 | |
| C. | 推廣煤的氣化、液化技術,提供清潔、高效燃料和基礎化工原料,挖掘使用價值 | |
| D. | 推廣利用微生物發酵技術,將植物桔桿、動物糞便等制成沼氣以替代液化石油氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v甲>v乙>v丙 | B. | v乙>v甲>v丙 | C. | v甲>v丙>v乙 | D. | v甲=v乙=v丙 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com