
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
分析 前半分鐘內 v(H2)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{(3-2.1)mol}{4L}}{0.5min}$=0.45 mol•L-1•min-1,同一可逆反應同一時間內,各物質的反應速率之比等于其計量數之比,據此計算氮氣、氨氣反應速率,據此分析解答.
解答 解:前半分鐘內 v(H2)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{(3-2.1)mol}{4L}}{0.5min}$=0.45 mol•L-1•min-1,同一可逆反應同一時間內,各物質的反應速率之比等于其計量數之比,
v(N2)=$\frac{1}{3}$×v(H2)=$\frac{1}{3}$×0.45 mol•L-1•min-1=0.15mol•L-1•min-1;
v(NH3)=$\frac{2}{3}$×v(H2)=$\frac{2}{3}$×0.45 mol•L-1•min-1=0.30 mol•L-1•min-1,
故選C.
點評 本題考查化學反應速率的有關計算,側重考查分析解答能力,明確計量數與速率關系是解本題關鍵,注意速率公式中各個字母含義,題目難度不大.


 王后雄學案教材完全解讀系列答案
王后雄學案教材完全解讀系列答案 海淀課時新作業金榜卷系列答案
海淀課時新作業金榜卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 若A是一種淡黃色固體,B是造成酸雨的“罪魁禍首”,則X為O2 | |
| B. | 若X是生活中常見的過渡金屬,A是黃綠色氣體,則B→C的離子方程式為Fe+2Fe3+=3Fe2+ | |
| C. | 若C是一種酸式鹽,則X一定是CO2 | |
| D. | A既可以為金屬單質,也可以為非金屬單質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
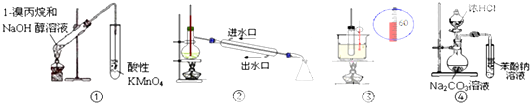
| A. | ①裝置用于檢驗1-溴丙烷消去產物 | B. | ②裝置用于石油的分餾 | ||
| C. | ④裝置可證明酸性:鹽酸>碳酸>苯酚 | D. | ③裝置用于實驗室制硝基苯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鎂條作負極,電極反應:Mg-2e-=Mg2+ | |
| B. | 鋁片作負極,電極反應:Al+4OH--3e--=[Al(OH)4]- | |
| C. | 電流從Al電極沿導線流向Mg電極 | |
| D. | 鋁片上有氣泡產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
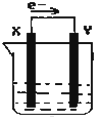 如圖,在盛有稀硫酸的燒杯中放入用導線連接的電極X、Y,外電路中電子流向如圖所示,下列 關于該裝置的說法正確的是( )
如圖,在盛有稀硫酸的燒杯中放入用導線連接的電極X、Y,外電路中電子流向如圖所示,下列 關于該裝置的說法正確的是( )| A. | 外電路電流方向為:X→外電路→Y | |
| B. | 若兩極分別為鐵棒和碳棒,則X為碳棒,Y為鐵棒 | |
| C. | X極上發生的是還原反應,Y極上發生的是氧化反應 | |
| D. | 若兩極都是金屬,則它們的活動順序為X>Y |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯 | B. | 乙基(-CH2CH3) | C. | 碳正離子[(CH3)3C+] | D. | 碳烯(:CH2) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
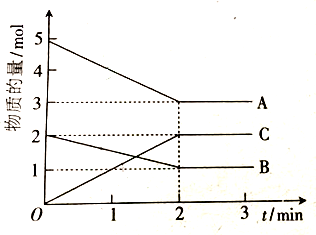
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
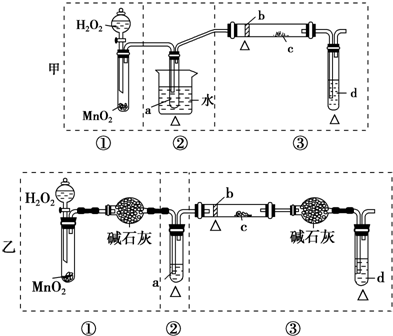
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗組 | 溫度 | 起始時物質的量/mol | 平衡時物質的量/mol | 達到平衡所需的時間/min | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | |||
| 1 | 650℃ | 2.0 | 6.0 | 0 | 1.0 | 5 | ||
| 2 | 900℃ | 2.0 | 6.0 | 0 | 1.2 | 2 | ||
| 3 | 650℃ | 1.0 | 4.0 | 2.0 | a | b | c | t |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com