
某溶液中加過量鹽酸生成白色沉淀,過濾后向濾液中加過量氫氧化鈉溶液,又有白色沉淀生成,再過濾后向濾液中加碳酸鈉溶液,又生成白色沉淀,原溶液中含有的離子可能是
A.Ag+、Ba2+、Cu2+ B.Ag+、Ba2+、Fe3+
C.Ag+、Ba2+、Mg2+ D.K+、Ca2+、Fe2+
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2017屆甘肅省高三上12月月考化學試卷(解析版) 題型:填空題
空氣質量評價的主要污染物為PM10、PM2.5、SO2、NO2、O3和CO等物質。
(1)煙氣的脫硝(除NOx)技術和脫硫(除SO2)技術都是環境科學研究的熱點。
選擇性催化還原技術(SCR)是目前最成熟的煙氣脫硝技術,即在催化劑作用下,用還原劑(如NH3)選擇性地與NOx反應生成N2和H2O。
①已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=﹣905.5kJ/mol
N2(g)+O2(g)=2NO(g) △H= +180kJ/mol
則4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H=
②在催化劑作用下,尿素[CO(NH2)2]也可以將NOx反應生成N2和H2O。寫出CO(NH2)2與NO2反應的化學方程式 。
(2)電化學法是合成氨的一種新方法,其原理如圖1所示,陰極的電極反應是 。
(3)氨碳比[n(NH3)/n(CO2)]對合成尿素[2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)]有影響,恒溫恒容時,將總物質的量3 mol的NH3和CO2以不同的氨碳比進行反應,結果如圖2所示。a、b線分別表示CO2或NH3的轉化率變化,c線表示平衡體系中尿素的體積分數變化。[n(NH3)/ n(CO2)]= 時,尿素產量最大;經計算,圖中y= (精確到0.01)。
CO(NH2)2(g)+H2O(g)]有影響,恒溫恒容時,將總物質的量3 mol的NH3和CO2以不同的氨碳比進行反應,結果如圖2所示。a、b線分別表示CO2或NH3的轉化率變化,c線表示平衡體系中尿素的體積分數變化。[n(NH3)/ n(CO2)]= 時,尿素產量最大;經計算,圖中y= (精確到0.01)。
(4)廢水中含氮化合物的處理方法有多種。
①用次氯酸鈉氧化氨氣,可以得到N2H4的稀溶液,該反應的化學方程式是__________。
②用H2催化還原法可降低水中NO 的濃度,得到的產物能參與大氣循環,則反應后溶液的pH (填“升高”、“降低”或“不變”)。
的濃度,得到的產物能參與大氣循環,則反應后溶液的pH (填“升高”、“降低”或“不變”)。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二12月月考化學試卷(解析版) 題型:選擇題
關于某酸的酸式鹽NaHY的水溶液的下列敘述中,正確的是
A.該酸式鹽的水溶液一定顯酸性
B.在該鹽溶液中,離子濃度為:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C.若HY-能水解,水解方程式為:HY-+H2O Y2-+H3O+
Y2-+H3O+
D.若HY-能電離,電離方程式為:HY-+H2O Y2-+H3O+
Y2-+H3O+
查看答案和解析>>
科目:高中化學 來源:2016-2017學年青海省高二11月月考化學試卷(解析版) 題型:選擇題
在恒溫、恒容下發生反應:A(s)+B(g) = C(g)+D(g) △H<0。則下列判斷正確的是( )
A.向該容器中加入少量A,反應速率增大
B.向該容器中充入氬氣,反應速率增大
C.將粉末狀A代替塊狀A能加快反應
D.該反應為放熱反應,無需加熱即可發生
查看答案和解析>>
科目:高中化學 來源:2016-2017學年青海省高二11月月考化學試卷(解析版) 題型:選擇題
下列有關燃料的說法錯誤的是( )
A.燃料燃燒產物CO2是溫室氣體之一
B.化石燃料完全燃燒不會造成大氣污染
C.以液化石油氣代替燃油可減少大氣污染
D.燃料不完全燃燒排放的CO是大氣污染物之一
查看答案和解析>>
科目:高中化學 來源:2016-2017學年內蒙古高一期中化學卷(解析版) 題型:選擇題
如果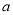 g某氣體中含有的分子數為
g某氣體中含有的分子數為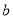 ,則
,則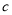 g該氣體在標準狀況下占有的體積應表示為(式中
g該氣體在標準狀況下占有的體積應表示為(式中 為阿伏加德羅常數)
為阿伏加德羅常數)
A. B.
B.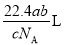 C.
C.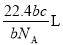 D.
D.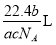
查看答案和解析>>
科目:高中化學 來源:2016-2017學年內蒙古高一期中化學卷(解析版) 題型:選擇題
下列反應的現象描述與離子方程式 都正確的是
都正確的是
A.金屬鎂與稀硫酸反應:有氫氣產生;Mg+2H++SO42? =MgSO4?+H2↑
B.氫氧化鋇溶液與硫酸反應:有白色沉淀生成;Ba2+ +SO42-=BaSO4?
C.碳酸鈣溶液與鹽酸反應:有氣泡生成;CaCO3+2H+=Ca2++CO2?+H2O
D.碳酸鈣加入醋酸:有氣體生成;CaCO3+2H+=CO2↑+ Ca2+ +H2O
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上段考二化學試卷(解析版) 題型:填空題
在實驗室模擬工業上以黃銅礦精礦為原料,制取硫酸銅及金屬銅的工藝如下所示:
Ⅰ.將黃銅礦精礦(主要成分為CuFeS2,含有少量CaO、MgO、Al2O3)粉碎
Ⅱ.采用如下裝置進行電化學浸出實驗
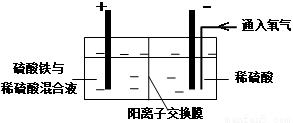
將精選黃銅礦粉加入電解槽陽極區,恒速攪拌,使礦粉溶解。在陰極區通入氧氣,并加入少量催化劑。
Ⅲ.一段時間后,抽取陰極區溶液,向其中加入有機萃取劑(RH)發生反應:
2RH(有機相)+ Cu2+(水相) R2Cu(有機相)+ 2H+(水相)
R2Cu(有機相)+ 2H+(水相)
分離出有機相,向其中加入一定濃度的硫酸,使Cu2+得以再生。
Ⅳ.電解硫酸銅溶液制得金屬銅。
(1)黃銅礦粉加入陽極區與硫酸及硫酸鐵主要發生以下反應:
CuFeS2+4H+=Cu2++Fe2++2H2S
2Fe3++H2S=2Fe2++S↓+2H+
① 陽極區硫酸鐵的主要作用是 _____________。
② 電解過程中,陽極區Fe3+的濃度基本保持不變,原因是_____________。(使用化學用語作答)
(2)若在實驗室進行步驟Ⅲ,分離有機相和水相的主要實驗儀器是 _____________;加入有機萃取劑的目的是___________________。
(3)步驟Ⅲ,向有機相中加入一定濃度的硫酸,Cu2+得以再生的原理是 _____________。
(4)步驟Ⅳ,若電解200mL0.5 mol/L的CuSO4溶液,生成銅3.2 g,此時溶液中離子濃度由大到小的順序是 ___________________。(忽略電解前后溶液體積的變化)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年廣西省欽州港區高一上11月月考化學卷(解析版) 題型:選擇題
ClO2是新一代飲用水的消毒劑,許多發達國家的自來水廠采用ClO2代替Cl2來進行自來水消毒,我國最近成功研 制出制取ClO2的新方法,其反應的微觀過程如下所示:
制出制取ClO2的新方法,其反應的微觀過程如下所示:
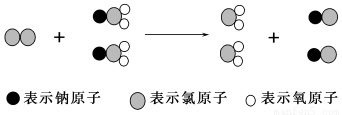
下列有關該反應的敘述中正確的是( )
A.該反應是復分解反應
B.該反應的化學方程式為Cl2+2NaClO2===2ClO2+2NaCl
C.反應中Cl2既是氧化劑,又是還原劑
D.生成2 mol ClO2時轉移的電子數為6 mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com