【答案】
分析:(1)根據(jù)反應“2Ag
+(aq)+Cu(s)═Cu
2+(aq)+2Ag(s)”分析,在反應中,Cu被氧化,失電子,應為原電池的負極,電極反應為Cu-2e
-=Cu
2+,則正極為活潑性較Cu弱的Ag,Ag
+在正極上得電子被還原,電極反應為Ag
++e=Ag,電解質溶液為AgNO
3 ;
(2)負極上失電子,金屬變成離子進入溶液;正極上金屬離子得電子析出金屬單質;溶液中陰離子移向負極,陽離子移向正極;外電路中電子從負極沿導線流向正極;
(3)根據(jù)同一反應中同一時間段內各物質的反應速率之比等于計量數(shù)之比計算;
(4)根據(jù)原電池的形成條件判斷,原電池的形成條件為:①有兩個活潑性不同的電極,②將電極插入電解質溶液中,③兩電極間構成閉合回路,④能自發(fā)的進行氧化還原反應.
解答:解:(1)根據(jù)反應“2Ag
+(aq)+Cu(s)═Cu
2+(aq)+2Ag(s)”分析,在反應中,Cu被氧化,失電子生成銅離子,電極反應為應為Cu-2e
-=Cu
2+,所以銅為原電池的負極;則正極為活潑性較Cu弱的Ag,Ag
+在正極上得電子被還原生成銀單質,電極反應為Ag
++e=Ag,電解質溶液為AgNO
3 ,
故答案為:銅棒;Cu-2e
-=Cu
2+;銀棒;Ag
++e=Ag;AgNO
3 溶液;
(2)銅為負極,負極上失電子生成銅離子進入溶液,所以看到的現(xiàn)象是銅棒不斷溶解;正極上銀離子得電子生成銀單質,所以看到的現(xiàn)象是有固體析出;電子在正極上聚集,所以負極附近有大量的陽離子,溶液中的銀離子移向負極銅棒;外電路上,電子從負極銅棒沿導線流向正極銀棒,
故答案為:銅棒不斷溶解;有固體析出;銅棒;銀棒;
(3)同一反應中同一時間段內各物質的反應速率之比等于計量數(shù)之比,由方程式2Ag
+(aq)+Cu(s)═Cu
2+(aq)+2Ag(s)得,銅離子的反應速率是銀離子反應速率的

,所以銅離子的反應速率是 0.025mol/L.min,故答案為:0.025mol/L.min;
(4)原電池的形成條件為:①有兩個活潑性不同的電極,②將電極插入電解質溶液中,③兩電極間構成閉合回路,④能自發(fā)的進行氧化還原反應.該反應不是自發(fā)進行的化學反應,所以不能設計為原電池,故答案為:不能,該反應不能自發(fā)進行.
點評:本題原電池原理為載體考查了原電池的設計,難度較大,注意設計原電池時要緊扣原電池的形成條件,會根據(jù)原電池的電池反應式判斷正負極及電解質溶液.

 ,所以銅離子的反應速率是 0.025mol/L.min,故答案為:0.025mol/L.min;
,所以銅離子的反應速率是 0.025mol/L.min,故答案為:0.025mol/L.min;

 依據(jù)氧化還原反應:2Ag+ (aq)+Cu(s)═Cu2+ (aq)+2Ag(s)設計的原電池如圖所示.
依據(jù)氧化還原反應:2Ag+ (aq)+Cu(s)═Cu2+ (aq)+2Ag(s)設計的原電池如圖所示.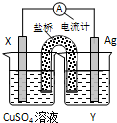 依據(jù)氧化還原反應:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)設計的原電池如圖所示.請回答下列問題:
依據(jù)氧化還原反應:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)設計的原電池如圖所示.請回答下列問題: 依據(jù)氧化還原反應:
依據(jù)氧化還原反應: