
【題目】含n克HNO3的稀溶液恰好與m克Fe完全反應,若HNO3只被還原為NO,則n:m可能( )
①5:1、②9:2、③3:1、④2:1、⑤4:1
A. ②③ B. ①③④ C. ②③⑤ D. ①③
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】除去乙醇中溶解的微量食鹽可采用_____的方法。除去 Fe2O3 中混有的 A12O3 雜質的試劑是__________,對應的離子方程式為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是 ( )
A. 氫氧化鋁與鹽酸反應:H++OH-=H2O
B. 碳酸鈣與稀硝酸反應:CO32-+2H+=H2O+CO2↑
C. 鋅與稀硫酸反應:Zn+2H+=Zn2++H2↑
D. 氯化鎂溶液與氫氧化鈉溶液反應:Mg2++OH-=Mg(OH)2↓
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SO2的催化氧化是工業制取硫酸的關鍵步驟之一,該反應的化學方程式為:2SO2+O2![]() 2SO3,
2SO3,
△H<0。請回答下列問題:
(1)判斷該反應達到平衡狀態的標志是__________(填字母)。
a.SO2和SO3濃度相等 b.SO2百分含量保持不變
c.容器中氣體的壓強不變 d.SO3的生成速率與SO2的消耗速率相等
(2)當該反應處于平衡狀態時,在體積不變的條件下,下列措施中有利于提高SO2平衡轉化率的
是______________(填字母)。
a.向裝置中再充入N2 b.向裝置中再充入O2
c.改變反應的催化劑 d.降低溫度
(3)將0.050 mol SO2 (g)和0.030 mol O2 (g)放入容積為1L的密閉容器中,在一定條件下達到平衡,測得c(SO3) =0.040mol/L。計算該條件下反應的平衡常數K和SO2的轉化率(不必寫出計算過程)。
①平衡常數K=______________;
②平衡時,SO2的轉化率α (SO2) =_____________。
(4)SO2尾氣常用飽和Na2SO3溶液吸收,減少SO2氣體污染并可得到重要的化工原料NaHSO3。己知NaHSO3溶液同時存在以下兩種平衡:①HSO3-![]() SO32-+H+ ②HSO3-+H2O
SO32-+H+ ②HSO3-+H2O![]() H2SO3+OH-、常溫下,0.1 mol/LNaHSO3溶液的 pH<7,則該溶液中 c (H2SO3)__________c (SO32-)(填“>”或“=”或“<”下同)。
H2SO3+OH-、常溫下,0.1 mol/LNaHSO3溶液的 pH<7,則該溶液中 c (H2SO3)__________c (SO32-)(填“>”或“=”或“<”下同)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組要完成中和熱的測定。
(1)實驗桌上備有燒杯(大、小兩個燒杯)、泡沫塑料、泡沫塑料板、膠頭滴管、環形玻璃棒、0.5mol·L-1鹽酸、0.55mol·L-1NaOH溶液,尚缺少的實驗玻璃用品是______________、_________________。
實驗用品 | 溶液溫度 | 中和熱△H | |||
t1 | t2 | ||||
① | 50mL0.55mol·L-1NaOH | 50mL.0.5mol·L-1HCl | 20℃ | 23.3℃ | _______ |
② | 50mL0.55mol·L-1NaOH | 50mL.0.5mol·L-1HCl | 20℃ | 23.5℃ | |
(2)他們記錄的實驗數據如下:
已知:Q=Cm(t2-t1),反應后溶液的比熱容C為4.18kJ·℃-1·kg-1,各物質的密度均為lg·cm-3。計算完成上表。△H=____________
(3)某研究小組將V1mL 1.0 mol/L HCl溶液和V2 mL未知濃度的NaOH溶液混合均勻后測量并記錄溶液溫度,實驗結果如下圖所示(實驗中始終保持V1+V2 =50mL)。此反應所用NaOH溶液的濃度應為__________mol/L。
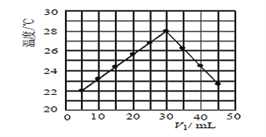
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組對一含有Al3+的未知溶液進行了如下分析:(1)滴入少量氫氧化鈉,無明顯變化;(2)繼續滴加NaOH溶液,有白色沉淀;(3)滴入過量的氫氧化鈉,白色沉淀明顯減少。實驗小組經定量分析,得出如圖所示沉淀與滴入氫氧化鈉體積的關系。下列說法正確的是( )

A. 該未知溶液中至少含有4種陽離子
B. 滴加的NaOH溶液的物質的量濃度為0.5 mol·L-1
C. 若另一種離子為二價陽離子,則a=10
D. 若將最終沉淀過濾、洗滌、灼燒,其質量一定為6g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】充分燃燒2.8g某有機物A,生成8.8g CO2和3.6g H2O,這種有機物蒸氣的相對密度是相同條件下N2的2倍。
(1)求該有機物的分子式。
(2)該有機物鏈狀同分異構體的結構簡式為: 。
(3)若在核磁共振氫譜中只有一個信號峰(即只有一種氫原子),則用鍵線式表示的結構簡式為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com