
分析 (1)每消耗1mol鋁能夠提供3mol電子,根據(jù)電子守恒,各金屬氧化物只能得到3mol電子,金屬的化合價越低,產生的金屬單質物質的量越多;
(2)氧化鐵溶于氫碘酸,滴加淀粉溶液,溶液變藍色,說明碘離子化合價升高,有碘單質產生,氧化鐵中+3價鐵的化合價降到+2價;氧化亞銅溶于稀硫酸,溶液變藍色,說明產生二價銅離子,有紅色固體生成,說明產生單質銅;
(3)①鋁作負極,失電子在堿性條件下產生AlO2-;
②活性鐵粉在堿性條件下,能將NO3-還原成NH3•H2O,本身被氧化成Fe3O4,根據(jù)得失電子守恒、電荷守恒、原子守恒寫出離子方程式;
(4)鐵器表面鍍一層性質不活潑的金屬可以提高耐腐蝕性;
(5)廢銅屑與濃硫酸反應制備硫酸銅,濃硫酸變稀后反應停止,為了使反應繼續(xù)進行,可加氧化劑將銅氧化成+2價,實現(xiàn)硫酸銅的制備,反應過程中不能產生有毒氣體;
(6)氧化銅與乙醇反應生成銅和乙醛,氧化銅中銅元素的化合價降低,單質銅是還原產物,則類推乙二醇與氧化銅反應的還原產物.
解答 解:(1)每消耗1mol鋁能夠提供3mol電子,根據(jù)電子守恒,各金屬氧化物只能得到3mol電子,金屬的化合價越低,產生的金屬單質物質的量越多,
V2O5→V,化合價變從+5變?yōu)?;MnO2→Mn,化合價由+4變?yōu)?;Cr2O3→Cr,化合價由+3變?yōu)?,則生成金屬物質的量最多的是Cr2O3,
故答案為:Cr2O3;
(2)氧化鐵溶于氫碘酸,滴加淀粉溶液,溶液變藍色,說明碘離子化合價升高,有碘單質產生,氧化鐵中+3價鐵的化合價降到+2價,離子方程式為:Fe2O3+2I-+6H+═2Fe2++3H2O+I2;氧化亞銅溶于稀硫酸,溶液變藍色,說明產生二價銅離子,有紅色固體生成,說明產生單質銅,氧化亞銅在稀硫酸中發(fā)歧化反應的方程式為:Cu2O+2H+=Cu+Cu2++H2O,
故答案為:Fe2O3+2I-+6H+═2Fe2++3H2O+I2;Cu2O+2H+=Cu+Cu2++H2O;
(3)①鋁作負極,失電子在堿性條件下產生AlO2-,電極反應式為:Al-3e-+4OH-=AlO2-+2H2O,故答案為:Al-3e-+4OH-=AlO2-+2H2O;
②活性鐵粉在堿性條件下,能將NO3-還原成NH3•H2O,氮的化合價降低8價,鐵本身被氧化成Fe3O4,鐵的化合價升高$\frac{8}{3}$價,則Fe與NO3-計量數(shù)之比為3:1,根據(jù)電荷守恒、原子守恒配平離子方程式為:3Fe+NO3-+3H2O=NH3•H2O+Fe3O4+OH-,故答案為:3Fe+NO3-+3H2O=NH3•H2O+Fe3O4+OH-;
(4)鐵器表面鍍一層性質不活潑的金屬可以提高耐腐蝕性,比如鐵上鍍銅等,故答案為:銅;
(5)廢銅屑與濃硫酸反應制備硫酸銅,濃硫酸變稀后反應停止,為了使反應繼續(xù)進行,可加氧化劑將銅氧化成+2價,
A.Fe2O3 與稀硫酸反應:產生三價鐵離子,三價鐵離子與銅反應產生二價銅離子,故A正確;
B.H2O2與銅在酸性條件下直接將銅氧化成銅離子,故B正確;
C.銅、硝酸根、氫離子可發(fā)生反應生成銅離子,同時硝酸根被還原成一氧化氮氣體,污染環(huán)境,故C錯誤;
D.通入空氣并加熱,銅與氧氣反應生成氧化銅,氧化銅與稀硫酸反應生成銅離子,故D正確;
故答案為:ABD;
(6)氧化銅與乙醇反應生成銅和乙醛,氧化銅中銅元素的化合價降低,單質銅是還原產物,則乙二醇與氧化銅反應的還原產物為銅,氧化產物是乙二醛,
故答案為:Cu.
點評 本題考查常見金屬元素的單質及其化合物的綜合應用,涉及鋁熱反應、氧化還原反應的計算及離子方程式的書寫等,注意氧化還原反應中得失電子守恒、離子守恒、原子守恒的應用,難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,5.6 L CCl4中含有的分子數(shù)目為0.25NA | |
| B. | 標準狀況下,體積為22.4L的物質所含微粒數(shù)是NA | |
| C. | 常溫常壓下,0.5 mol NH3中含有的原子數(shù)目為2NA | |
| D. | 500mL1 mol•L-1 K2SO4溶液中含有的k+數(shù)目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 甲、乙、丙、丁是四中含有同一元素的物質,其中甲是單質,丁是其最高化合物對應的水化物,它們之間有如圖所示的轉化關系,則丁不可能是( )
甲、乙、丙、丁是四中含有同一元素的物質,其中甲是單質,丁是其最高化合物對應的水化物,它們之間有如圖所示的轉化關系,則丁不可能是( )| A. | NaOH | B. | H2SiO3 | C. | HNO2 | D. | H2SO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
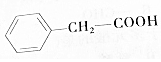 苯乙酸
苯乙酸 .
.查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=7的溶液中可能大量存在Fe3+、Cl-、Na+、S2- | |
| B. | 1 mol/L的FeCl3溶液滴入沸水中,得到分散質顆粒數(shù)為NA | |
| C. | 1 mol/L的Fe(NO3)2溶液中滴加鹽酸,溶液變?yōu)辄S色 | |
| D. | SO2與FeCl3溶液反應的離子方程式:2Fe3++SO2+4OH-=2Fe2++SO42-+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
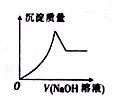 某水溶液X中只可能含有Al3+、CO32-、Cl-、SiO32-、SO42-、Fe2+中的若干種離子.某同學對該溶液進行了如下實驗:
某水溶液X中只可能含有Al3+、CO32-、Cl-、SiO32-、SO42-、Fe2+中的若干種離子.某同學對該溶液進行了如下實驗:查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com