
| A. | CaCl2 | B. | Ca(OH)2 | C. | 飽和Na2CO3溶液 | D. | Ca(ClO)2 |
分析 A.二氧化碳和氯化鈣溶液不發生反應;
B.二氧化碳與氫氧化鈣反應生成碳酸鈣;
C.二氧化碳與飽和碳酸鈉溶液反應,析出碳酸氫鈉;
D.發生反應:CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO.
解答 解:A.鹽酸是強酸,碳酸是弱酸,所以碳酸不能制取鹽酸,即二氧化碳和氯化鈣不反應,最終沒有沉淀析出,故A正確;
B.二氧化碳與氫氧化鈣反應生成碳酸鈣,碳酸鈣屬于難溶電解質,所以把少量CO2氣體通入Ca(OH)會生成碳酸鈣白色沉淀,故B錯誤;
C.二氧化碳與飽和碳酸鈉溶液反應,析出碳酸氫鈉,碳酸氫鈉的溶解度比碳酸鈉的小,故C錯誤;
D.發生反應:CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO,生成碳酸鈣沉淀,故D錯誤.
故選A.
點評 本題考查了離子反應發生的條件,題目難度不大,試題注重了基礎知識的考查,注意明確離子反應發生的條件、掌握常見元素化合物的化學性質.


科目:高中化學 來源: 題型:選擇題
| A. | Mg和Al | B. | Fe和Zn | C. | Fe和Cu | D. | Fe和Al |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向碘化亞鐵溶液中滴加溴的四氯化碳溶液2Br2+2Fe2++2I-═I2+4Br-+2Fe3+ | |
| B. | 向含等物質的量濃度AgNO3和Cu(NO3)2的溶液中緩慢加入鎂粉4Cu2++2Ag++5Mg═4Cu+2Ag+5Mg2+ | |
| C. | 氫氧化鐵溶于氫碘酸中:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O | |
| D. | 向0.3mol/LNaClO溶液中滴加等體積的0.2mol/LNaHSO3溶液:2HSO3-+4ClO-═2SO42-+2Cl-+2HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
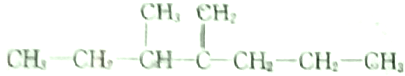 ,此烴名稱為3-甲基-2-丙基-1-戊烯
,此烴名稱為3-甲基-2-丙基-1-戊烯 ,可命名為1-甲基-3-乙基苯.
,可命名為1-甲基-3-乙基苯.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵釘放在濃硝酸中浸泡后,再用蒸餾水沖洗,然后放入CuSO4溶液中不反應,說明鐵釘表面形成了一層致密穩定的氧化膜 | |
| B. | 實驗室里吸入刺激性的氯氣、氯化氫氣體中毒時,吸入少量酒精或乙醚的混合蒸氣解毒 | |
| C. | SO2的水溶液和苯溶液中分別通入溴水褪色,兩者的原理一樣 | |
| D. | 在蛋白質溶液中加入氯化鋇有沉淀產生,是因為蛋白質變性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解質在固態時均為離子晶體 | |
| B. | CCl4、Cl2及HF中的原子都滿足最外層8電子穩定結構 | |
| C. | 用道爾頓的原子結構理論無法解釋同位素現象 | |
| D. | 晶體類型相同,則晶體中化學鍵也完全相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
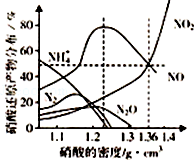 某些金屬與不同密度的硝酸反應時,往往生成多種不同價態的還原產物,如圖是在相同條件下,各種不同密度的硝酸和鐵反應時,還原產物的分布圖.通過圖象判斷下列說法錯誤的是( )
某些金屬與不同密度的硝酸反應時,往往生成多種不同價態的還原產物,如圖是在相同條件下,各種不同密度的硝酸和鐵反應時,還原產物的分布圖.通過圖象判斷下列說法錯誤的是( )| A. | 稀硝酸與鐵反應,一定有NO生成 | |
| B. | 密度小于1.1g•cm-3的硝酸與鐵反應,還原產物百分率最多的是NH4+ | |
| C. | 某硝酸試劑瓶的標簽注明:密度為1.26g•cm-3,質量分數50.0%;若取該試劑10ml配成100ml溶液,所得溶液C(H+)=0.1 | |
| D. | 當硝酸的密度為1.36g•cm-3時,過量鐵與硝酸反應,消耗的鐵與被還原的硝酸物質的量之比為1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com