
 奪冠訓練單元期末沖刺100分系列答案
奪冠訓練單元期末沖刺100分系列答案 新思維小冠軍100分作業本系列答案
新思維小冠軍100分作業本系列答案 名師指導一卷通系列答案
名師指導一卷通系列答案科目:高中化學 來源: 題型:
 (2011?鄭州二模)利用所學化學反應原理,解決以下問題:
(2011?鄭州二模)利用所學化學反應原理,解決以下問題:| H | + 4 |
| H | + 4 |
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 1mol H2、1mol I2 | 2 mol HI | 4 mol HI |
| HI的濃度(mol?L-1) | C1 | C2 | C3 |
| 反應的能量變化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 反應物轉化率 | a1 | a2 | a3 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
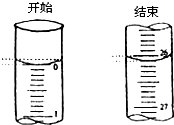 某學生欲用已知物質的量濃度的鹽酸來滴定測定未知物質的量濃度的氫氧化鈉溶液時,選擇酚酞作指示劑.請填寫下列空白:
某學生欲用已知物質的量濃度的鹽酸來滴定測定未知物質的量濃度的氫氧化鈉溶液時,選擇酚酞作指示劑.請填寫下列空白:| 滴定次數 | 待測氫氧化鈉 溶液的體積/mL |
0.1000mol/L鹽酸的體積(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液體/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
下列兩題分別對應于“物質結構與性質”和“實驗化學”兩個選修課程模塊的內容,請你選擇其中一題作答,如果兩題全做,則按A題評分。
A.已知A、B、C、D、E都是周期表中前四周期的元素,它們的核電荷數A<B<C<D<E。其中A、B、C是同一周期的非金屬元素。化合物DC的晶體為離子晶體,D的二價陽離子與C的陰離子具有相同的電子層結構。AC2為非極性分子。B、C的氫化物的沸點比它們同族相鄰周期元素氫化物的沸點高。E的原子序數為24,ECl3能與B、C的氫化物形成六配位的配合物,且兩種配體的物質的量之比為2∶1,三個氯離子位于外界。請根據以上情況,回答下列問題:(答題時,A、B、C、D、E用所對應的元素符號表示)
(1)A、B、C的第一電離能由小到大的順序為 。
(2)B的氫化物的分子空間構型是 。其中心原子采取 雜化。
(3)寫出化合物AC2的電子式 ;一種由B、C組成的化合物與AC2互為等電子體,其化學式為 。
(4)E的核外電子排布式是 ,ECl3形成的配合物的化學式為 。
(5)B的最高價氧化物對應的水化物的稀溶液與D的單質反應時,B被還原到最低價,該反應的化學方程式是 。
B.醇與氫鹵酸反應是制備鹵代烴的重要方法。實驗室制備溴乙烷和1-溴丁烷的反應如下:
NaBr+H2SO4![]() HBr+NaHSO4 ①
HBr+NaHSO4 ①
R-OH+HBr![]() R-Br+H2O ②
R-Br+H2O ②
可能存在的副反應有:醇在濃硫酸的存在下脫水生成烯和醚,Br―被濃硫酸氧化為Br2等。有關數據列表如下;
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g?cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸點/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
請回答下列問題:
(1)在溴乙烷和1-溴丁烷的制備實驗中,下列儀器最不可能用到的是 。(填字母)
a.圓底燒瓶 b.量筒 c.錐形瓶 d.布氏漏斗
(2)溴代烴的水溶性 (填“大于”、“等于”或“小于”)相應的醇;其原因是
。
(3)將1-溴丁烷粗產品置于分液漏斗中加水,振蕩后靜置,產物在 (填“上層”、“下層”或“不分層”)。
(4)制備操作中,加入的濃硫酸必須進行稀釋,起目的是 。(填字母)
a.減少副產物烯和醚的生成 b.減少Br2的生成
c.減少HBr的揮發 d.水是反應的催化劑
(5)欲除去溴代烷中的少量雜質Br2,下列物質中最適合的是 。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(6)在制備溴乙烷時,采用邊反應邊蒸出產物的方法,其有利于 ;但在制備1-溴丁烷時卻不能邊反應邊蒸出產物,其原因是 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年浙江省東陽市南馬高中高三下學期期中考試化學試卷 題型:填空題
(12分)利用所學化學反應原理,解決以下問題:
(1)某溶液含兩種相同物質的量的溶質,且其中只存在OH一、H+、NH4+、Cl一四種離子,
且c(NH4+)>c(Cl-)>c(OH-)>c(H+),則這兩種溶質是 。
(2)0.1 mol·L-1的氨水與0.05 mol·L-1的稀硫酸等體積混合,用離子方程式表示混合后溶液的酸堿性: 。
(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,則難溶鹽RX、RY和R2Z的飽和溶液中,R+濃度由大到小的順序是 。
(4)向20 mL硫酸和鹽酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量
如右圖所示,B點溶液的pH=7(假設體積
可以直接相加),則c(HCl)= mol·L-1.
(5)在溫度、容積相同的3個密閉容器中,
按下表投入反應物,發生反應(H2(g)+
I2(g) 2HI(g) △H=-14.9 kJ·mol-1),在恒溫、恒容條件下, 測得反應達
2HI(g) △H=-14.9 kJ·mol-1),在恒溫、恒容條件下, 測得反應達
到平衡時的數據如下表:
下列說法正確的是 。
A. + + =1 =1 | B.2 = = | C.a+b=14.9 | D.c1=c2=c3 |

查看答案和解析>>
科目:高中化學 來源:2012屆浙江省東陽市高三下學期期中考試化學試卷 題型:填空題
(12分)利用所學化學反應原理,解決以下問題:
(1)某溶液含兩種相同物質的量的溶質,且其中只存在OH一、H+、NH4+、Cl一四種離子,
且c(NH4+)>c(Cl-)>c(OH-)>c(H+),則這兩種溶質是 。
(2)0.1 mol·L-1的氨水與0.05 mol·L-1的稀硫酸等體積混合,用離子方程式表示混合后溶液的酸堿性: 。
(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,則難溶鹽RX、RY和R2Z的飽和溶液中,R+濃度由大到小的順序是 。
(4)向20 mL硫酸和鹽酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量
如右圖所示,B點溶液的pH=7(假設體積
可以直接相加),則c(HCl)= mol·L-1.

(5)在溫度、容積相同的3個密閉容器中,
按下表投入反應物,發生反應(H2(g)+
I2(g) 2HI(g) △H=-14.9 kJ·mol-1),在恒溫、恒容條件下, 測得反應達
2HI(g) △H=-14.9 kJ·mol-1),在恒溫、恒容條件下, 測得反應達
到平衡時的數據如下表:
下列說法正確的是 。
A. +
+ =1
B.2
=1
B.2 =
= C.a+b=14.9
D.c1=c2=c3
C.a+b=14.9
D.c1=c2=c3

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com