
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3+ |
| 含量/mg?L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |

| 序號 | 實驗方案 | 實驗現象 | 結論 |
| ① | 取少量稀釋后的溶液A加入淀粉溶液后再用硫酸酸化,分裝于試管Ⅰ、Ⅱ | 無現象 | |
| ② | 往試管Ⅰ中加入 | 無現象 | 灼燒后碘元素不是以IO3-形式存在 |
| ③ | 往試管Ⅱ中加入 | 灼燒后碘元素以I-形式存在 |
| m |
| M |
| ||
| 1L |


科目:高中化學 來源: 題型:
| A、Cu和濃硝酸反應:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| B、氫氧化鎂與稀硫酸反應:H++OH-=H2O |
| C、Ca(HCO3)2溶液與過量的NaOH溶液反應:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| D、等物質的量濃度、等體積的NH4HCO3溶液與NaOH溶液相混合:NH4++HCO3-+2OH-=NH3?H2O+CO32-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
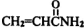 )具有中等毒性.A-K幾種有機物間的轉化關系如圖所示(部分條件和產物略去).已知:A為氣態烴,標準狀況下密度為2.5g/L,且核磁共振氫譜有4個吸收峰;G比丙烯酰胺多一個CH2原子團.
)具有中等毒性.A-K幾種有機物間的轉化關系如圖所示(部分條件和產物略去).已知:A為氣態烴,標準狀況下密度為2.5g/L,且核磁共振氫譜有4個吸收峰;G比丙烯酰胺多一個CH2原子團.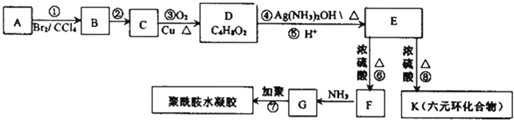
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
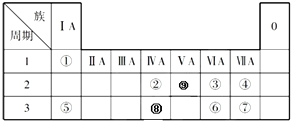
| A、①④⑤⑥ | B、③④⑤⑥ |
| C、只有①③ | D、全部 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com