
以氮化鎵(GaN)為代表的第三代半導體材料目前已成為全球半導體研究的前沿和熱點。回答下列問題:
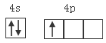
(1)鎵為元素周期表第31號元素,鎵原子價層電子排布圖為__________________。
(2)氮所在主族中第一電離能最大的元素是___________(填元素符號,下同),鎵所在主族中電負性最大的元素是_____________________。
(3)傳統的氮化鎵制備方法是采用CaCl3與NH3在一定條件下反應,該反應的化學方程式為_________________。
(4)氮化鎵與金剛石具有相似的晶體結構,氮化鎵中氮原子與鎵原子之間以__________相結合,氮化鎵屬于______________晶體。
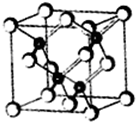
(5)下圖是氮化鎵的晶胞模型:
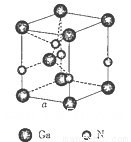
①氮化鎵中鎵原子的雜化方式為_______________,氮原子的配位數為__________________。
②氮化鎵為立方晶胞,氮化鎵的密度為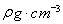 。列出計算氮化鎵晶胞邊長a的表達式:a=_______cm。
。列出計算氮化鎵晶胞邊長a的表達式:a=_______cm。
(1)
(2)N????? B?
(3)GaCl3+NH3=GaN+3HCl
(4)共價鍵???? 原子
(5)①sp3 ???? 4????? ②
【解析】
試題分析:(1)鎵為元素周期表第31號元素,在元素周期表中的位置是位于第四周期第ⅢA。鎵原子價層電子排布圖為 。(2)氮在第ⅤA.在第ⅤA的元素中,由于N原子半徑最小,原子核外的最外層電子處于半充滿的穩定狀態。所以其第一電離能最大。鎵在元素周期表第ⅢA。該主族中元素中電負性最大的元素是原子半徑最小的B元素。(3)用CaCl3與NH3在一定條件下反應制備氮化鎵,根據質量守恒定律可得該反應的化學方程式為GaCl3+NH3=GaN+3HCl。? (4)氮化鎵與金剛石具有相似的晶體結構,金剛石的C原子之間以共價鍵結合,是原子晶體。所以氮化鎵中氮原子與鎵原子之間以共價鍵相結合,氮化鎵屬于原子晶體。(5) ①每個鎵與4個N形成共價鍵,這四個N構成正四面體結構。每個N與4個Ga形成共價鍵,這四個Ga構成正四面體結構。所以氮化鎵中鎵原子的雜化方式為sp3。氮原子的配位數為4. ②在每個晶胞中含有Ga:8×1/8+1=2,含有N:4×1/4+1=2.即每個晶胞中含有2個GaN。氮化鎵晶胞邊長a。則
。(2)氮在第ⅤA.在第ⅤA的元素中,由于N原子半徑最小,原子核外的最外層電子處于半充滿的穩定狀態。所以其第一電離能最大。鎵在元素周期表第ⅢA。該主族中元素中電負性最大的元素是原子半徑最小的B元素。(3)用CaCl3與NH3在一定條件下反應制備氮化鎵,根據質量守恒定律可得該反應的化學方程式為GaCl3+NH3=GaN+3HCl。? (4)氮化鎵與金剛石具有相似的晶體結構,金剛石的C原子之間以共價鍵結合,是原子晶體。所以氮化鎵中氮原子與鎵原子之間以共價鍵相結合,氮化鎵屬于原子晶體。(5) ①每個鎵與4個N形成共價鍵,這四個N構成正四面體結構。每個N與4個Ga形成共價鍵,這四個Ga構成正四面體結構。所以氮化鎵中鎵原子的雜化方式為sp3。氮原子的配位數為4. ②在每個晶胞中含有Ga:8×1/8+1=2,含有N:4×1/4+1=2.即每個晶胞中含有2個GaN。氮化鎵晶胞邊長a。則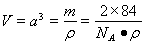 ,所以整理得:
,所以整理得: 。
。
考點:考查原子價層電子排布圖、電離能、電負性、晶體結構、晶體的邊長、化學方程式的書寫等知識。


科目:高中化學 來源: 題型:
 銦、鎵與氮、磷、硫、砷等元素形成的化合物是制備LED晶片的主要原料,材質基本以AlGaInP(磷化鋁鎵銦)、InGaN(氮化銦鎵)為主.
銦、鎵與氮、磷、硫、砷等元素形成的化合物是制備LED晶片的主要原料,材質基本以AlGaInP(磷化鋁鎵銦)、InGaN(氮化銦鎵)為主.查看答案和解析>>
科目:高中化學 來源: 題型:
| 兩性氫氧化物 | Al(OH)3 | Ga(OH)3 |
| 酸式電離常數Kia | 2×10-11 | 1×10-7 |
| 堿式電離常數Kib | 1.3×10-33 | 1.4×10-34 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com