
一定條件下,在體積一定的密閉容器中加入1mol N2和3mol H2發生反應:N2+3H2 2NH3(正反應是放熱反應).下列有關說法正確的是
2NH3(正反應是放熱反應).下列有關說法正確的是
A. 升高溫度能加快反應速率
B. 1mol N2和3mol H2的總能量低于2mol NH3的總能量
C. 達到化學反應限度時,生成2molNH3
D. 平衡時各組分含量之比一定等于3:1:2
科目:高中化學 來源:2017屆安徽省“江南十校”高三3月聯考理綜化學試卷(解析版) 題型:簡答題
Zn(OH)2可溶于氨水生成[Zn(NH3)4]2+: Zn(OH)2+4NH3·H2O=Zn(NH3)4]2++4H2O+2OH-
(1)原子序數比Zn元素小1的元素符號為____,該元素原子基態核外電子排布式為______。
(2)NH3、H2O的沸點均高于同族元素氫化物的沸點,是因為________。
(3)NH3中N原子軌道的雜化類型是______。
(4)與H2O分子互為等電子體的分子為_____。
(5)閃鋅礦是一種自然界含Zn元素的礦物,其晶體結構屬于立方晶體(如右圖所示),則在立方ZnS晶體結構中S2-的配位數為________。Zn2+的分數坐標為(l/4,l/4,l/4)、(3/4, 3/4,l/4)、(3/4,l/4,3/4)、(1/4,3/4,3/4),則S2-的分數坐標為______。

查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省揚州市寶應縣高二下學期學業水平測試(三)化學試卷(解析版) 題型:選擇題
我國首創的海洋電池以鋁板、鉑網為電極,以海水作為電解質溶液,電池總反應為:4Al+3O2+6H2O=4Al(OH)3,下列有關該電池說法正確的是
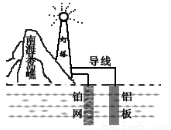
A. 該電池工作時將電能轉化為化學能
B. 通常一段時間后該電池只需更換鋁板就可繼續使用
C. 負極反應式是:O2 + 2H2O+ 4e- = 4OH-
D. 鋁片發生還原反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省揚州市寶應縣高二下學期學業水平測試(三)化學試卷(解析版) 題型:選擇題
常溫下,將銅片投入到下列溶液中,會產生氣體的是
A. 稀硫酸 B. 稀鹽酸 C. 濃硝酸 D. 濃硫酸
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省哈爾濱市高二3月月考化學試卷(解析版) 題型:選擇題
已知反應Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)為一自發進行的氧化還原反應,將其設計成如圖所示原電池。下列說法中正確的是(_____)
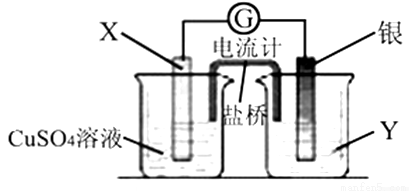
A.電極X是正極,其電極反應為Cu-2e-=Cu2+
B.銀電極質量逐漸減小,Y溶液中c(Ag+)增大
C.實驗過程中取出鹽橋,原電池仍繼續工作
D.當X電極質量減少0.64g時,外電路中有0.02mol電子轉移
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省哈爾濱市高二3月月考化學試卷(解析版) 題型:選擇題
實驗室用鋅粒與VmL濃度為10%的稀硫酸反應制取氫氣,若向反應混合物中加入下列物質,關于反應速率v說法正確的是
A. 少量Na2SO4固體,v(H2)減小 B. VmLBaCl2溶液,v(H2)不變
C. 加入細小的碳粒,v(H2)增大 D. 加入NH4HSO4固體,v(H2)不變
查看答案和解析>>
科目:高中化學 來源:2017屆天津市高三第四次月考化學試卷(解析版) 題型:實驗題
(17分)亞氯酸鈉(NaClO2)是重要漂白劑。探究小組開展如下實驗,回答下列問題:
實驗Ⅰ:制取NaClO2晶體按下圖裝置進行制取。
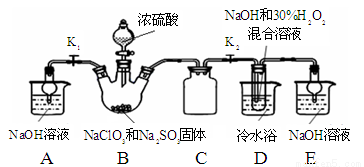
已知:NaClO2飽和溶液在低于38℃時析出NaClO2•3H2O,高于38℃時析出NaClO2,高于60℃時NaClO2分解成NaClO3和NaCl。
(1)用50%雙氧水配制30%的H2O2溶液,需要的玻璃儀器除玻璃棒、膠頭滴管、燒杯外,還需要 (填儀器名稱);
(2)裝置C的作用是 ;
(3)裝置B內生成的ClO2氣體與裝置D中混合溶液反應生成NaClO2,生成NaClO2的反應方程式為 。
(4)如果撤去D中的冷水浴,可能導致產品中混有的雜質是 ;
(5)反應后,經以下步驟可從裝置D的溶液獲得NaClO2晶體。請補充完整操作iii。
i.55℃蒸發結晶;
ii.趁熱過濾;
iii. ;
iv.低于60℃干燥,得到成品。
實驗Ⅱ:樣品雜質分析與純度測定
(6)上述實驗制得的NaClO2晶體中含少量Na2SO4。產生Na2SO4最可能的原因是 ;
a. B中有SO2氣體產生,并有部分進入D裝置內
b. B中濃硫酸揮發進入D中與NaOH中和
c. B中的硫酸鈉進入到D裝置內
(7)測定樣品中NaClO2的純度。測定時進行如下實驗:
準確稱一定質量的樣品,加入適量蒸餾水和過量的KI晶體,在酸性條件下發生如下反應:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-,將所得混合液稀釋成100mL待測溶液。取25.00mL待測溶液,加入淀粉溶液做指示劑,用c mol·L-1Na2S2O3標準液滴定至終點,測得消耗標準溶液體積的平均值為V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
①確認滴定終點的現象是 ;
②所稱取的樣品中NaClO2的物質的量為 (用含c、V的代數式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com