
【題目】納米級Fe粉是新型材料,具有超強磁性、高效催化性。某化學小組探究用氫氣和碳酸亞鐵制取納米級鐵粉。其實驗設計如圖(加熱、支持裝置省略):

(1)a的名稱是________________;濃硫酸的作用是________________。
(2)打開分液漏斗活塞,一段時間后再對C裝置加熱,這樣操作的目的是_______________;反應一段時間后D中變藍,E中溶液變渾濁,C中發(fā)生反應的化學方程式為______________。
(3)反應中若觀察到B裝置中氣泡產(chǎn)生過快,則應進行的操作是_____________________。
(4)反應一段時間后,B中產(chǎn)生氣泡太慢,再滴加硫酸,反應速率略有加快但不明顯;若向硫酸中加少量硫酸銅,再滴入硫酸與Zn反應,反應速率明顯加快,原因是__________________。
(5)檢驗碳酸亞鐵中含有鐵元素的實驗方法是____________________________。
【答案】(1)蒸餾燒瓶,吸收氫氣中的水蒸氣(或干燥氫氣);
(2)排除體系內(nèi)的空氣,防止干擾實驗,防止爆炸,FeCO3+H2![]() Fe+CO2+H2O;
Fe+CO2+H2O;
(3)調(diào)節(jié)A中分液漏斗活塞,減慢硫酸滴加速度
(4)鋅與硫酸銅反應生成銅,銅與鋅形成原電池(鋅為負極),加快了反應速率
(5)取少量FeCO3加適量鹽酸完全溶解,再加入少量K3[Fe(CN)3]溶液,產(chǎn)生藍色沉淀,則碳酸亞鐵中含有鐵元素。(溶解后加入氧化劑,檢驗Fe3+也可)
【解析】
試題分析:(1)根據(jù)儀器a的構(gòu)造可知a為蒸餾燒瓶;裝置A為氫氣的發(fā)生裝置,用氫氣還原裝置C中的碳酸亞鐵,氫氣必須干燥,故裝置B中濃硫酸的作用是吸收氫氣中的水蒸氣(或干燥氫氣)。
(2)打開分液漏斗活塞,一段時間后再對C裝置加熱,這樣操作的目的是排除體系內(nèi)的空氣,防止干擾實驗,防止爆炸;反應一段時間后D中變藍,E中溶液變渾濁,則C中氫氣和碳酸亞鐵反應生成鐵、二氧化碳和水,發(fā)生反應的化學方程式為FeCO3+H2![]() Fe+CO2+H2O 。
Fe+CO2+H2O 。
(3)反應中若觀察到B裝置中氣泡產(chǎn)生過快,則應調(diào)節(jié)生成氫氣的生成速率,進行的操作是調(diào)節(jié)A中分液漏斗活塞,減慢硫酸滴加速度。
(4)若向硫酸中加少量硫酸銅,再滴入硫酸與Zn反應,反應速率明顯加快,原因是鋅與硫酸銅反應生成銅,銅與鋅形成原電池(鋅為負極),加快了反應速率。
(5)檢驗碳酸亞鐵中含有鐵元素即為Fe2+,實驗方法是取少量FeCO3加適量鹽酸完全溶解,再加入少量K3[Fe(CN)3]溶液,產(chǎn)生藍色沉淀,則碳酸亞鐵中含有鐵元素(溶解后加入氧化劑,檢驗Fe3+也可)。


 學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案
學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案 芒果教輔暑假天地重慶出版社系列答案
芒果教輔暑假天地重慶出版社系列答案科目:高中化學 來源: 題型:
【題目】已知可逆反應:M(g)+N(g)![]() P(g)+Q(g),△H>0請回答下列問題:
P(g)+Q(g),△H>0請回答下列問題:
(1)在某溫度下,反應物的起始濃度分別為:c(M)= 1 mol·L-1,c(N)=2.4 mol·L-1,達到平衡后,M的轉(zhuǎn)化率為60%,此時N的轉(zhuǎn)化率為_____________;
(2)若反應在相同條件下進行達到平衡后,再向容器中充入M氣體,再次達到平衡時該反應的平衡常數(shù)K_________(填“增大”“減小”或“不變”下同)。
(3)若反應溫度不變,反應物的起始濃度分別為:c(M)= 4mol·L-1, c(N)=a mol·L-1,達到平衡后,c(P)=2 mol·L-1,則a=_________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述中,正確的是( )
A.鋼鐵腐蝕的負極反應為:Fe-3e- = Fe3+
B.堿性介質(zhì)甲烷燃料電池的正極反應為:O2+2H2O+4e-=4OH-
C.Mg — Al及NaOH溶液構(gòu)成的原電池中負極材料為Mg
D.氯堿工業(yè)中陽極上產(chǎn)生的氣體比陰極上產(chǎn)生的氣體多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關苯的敘述中錯誤的是( )
A.苯在催化劑作用下能與濃硝酸發(fā)生取代反應
B.在一定條件下苯能與氫氣氣發(fā)生加成反應
C.在苯中加入酸性高錳酸鉀溶液,振蕩并靜置后下層液體為紫紅色
D.在苯中加入溴水,振蕩并靜置后下層液體為橙色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某混合物A,含有Al2 (SO4)3、A12O3和Fe2O3,在一定條件下可實現(xiàn)下圖所示的變化.
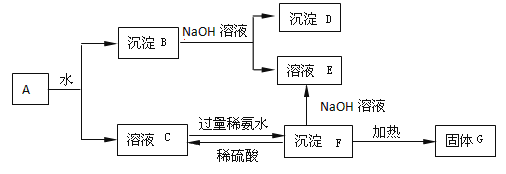
請回答下列問題:
(1)圖中分離沉淀B與溶液C的方法是____________________。
(2)D、E、F這3種物質(zhì)的化學式分別為:D:_______E:_______F:_________
(3)沉淀B與NaOH溶液反應的離子方式為__________;溶液C與過量稀氨水反應的離子方程式為_______________。
(4)檢驗溶液中是否含有Fe3+,最佳試劑是___________,現(xiàn)象為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Fe和Fe2O3的混合物共13.6g,加入150mL稀H2SO4,在標準狀況下收集到l.l2LH2,Fe和Fe2O3均無剩余.為中和過量的H2SO4,并使Fe元素全部轉(zhuǎn)化為Fe(OH)2沉淀,消耗了200mL3mol/L的NaOH溶液,則該H2SO4的物質(zhì)的量濃度為
A.2.25mol/L B.2mol/L C.4mol/L D.0.6mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子中,在堿性溶液中共存,且加入鹽酸過程中,會產(chǎn)生氣體和沉淀的是( )
A.Na+、NO3-、AlO2-、SO42-
B.Na+、NO3-、SiO32-、K+
C.K+、Cl-、AlO2-、CO32-
D.K+、Cl-、HCO3-、Ca2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三室式電滲析法處理含Na2SO4廢水的原理如圖所示,采用惰性電極,ab、cd均為離子交換膜,在直流電場的作用下,兩膜中間的Na+和SO42-可通過離子交換膜,而兩端隔室中離子被阻擋不能進入中間隔室。下列敘述正確的是
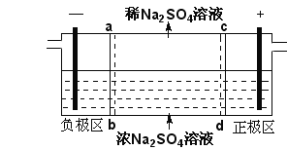
A.通電后中間隔室的SO42-離子向正極遷移,正極區(qū)溶液pH增大
B.該法在處理含Na2SO4廢水時可以得到NaOH和H2SO4產(chǎn)品
C.負極反應為2H2O–4e–=O2+4H+,負極區(qū)溶液pH降低
D.當電路中通過1mol電子的電量時,會有0.5mol的O2生成
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com