
| A. | X、M兩種元素只能形成X2M型化合物 | |
| B. | 元素Y、Z、W的單質晶體屬于同種類型的晶體 | |
| C. | 元素W和M的某些單質可作為水處理中的消毒劑 | |
| D. | 由于W、Z元素的氫氣化物還原性:W>Z |
分析 X、Y、Z、W、M五種短周期元素,Y的單質晶體熔點高、硬度大,是一種重要的半導體材料,可知Y為Si;X、Y、Z、W同周期,都處于第三周期,由X+與M2-具有相同的電子層結構,可知X為Na、M為O;Z、M同主族,則Z為S;離子半徑Z2->W(wǎng)-,則W為Cl,據(jù)此解答.
解答 解:X、Y、Z、W、M五種短周期元素,Y的單質晶體熔點高、硬度大,是一種重要的半導體材料,可知Y為Si;X、Y、Z、W同周期,都處于第三周期,由X+與M2-具有相同的電子層結構,可知X為Na、M為O;Z、M同主族,則Z為S;離子半徑Z2->W(wǎng)-,則W為Cl.
A.X、M兩種元素形成的化合物可以形成Na2O、Na2O2,故A錯誤;
B.硅晶體屬于原子晶體,硫及氯氣均形成分子晶體,故B錯誤;
C.Cl2和O3都具有強氧化性,則可以作為消毒劑,故C正確;
D.非金屬性:Cl>S,元素的非金屬性越強,對應的單質的氧化性越強,則對應氫化物還原性就越弱,故D錯誤,
故選C.
點評 本題考查位置結構性質的關系和應用,尋找本題的突破點為Y是解答本題的關鍵,然后利用元素化合物知識來解答即可.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | HCl | B. | CS2 | C. | H2S | D. | SO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學反應速率為0.8mol•L-1•s-1,是指在1s時某物質的濃度是0.8mol•L-1 | |
| B. | 化學反應速率是指在一段時間內任何一種反應物物質的量的減少或任何一種生成物物質的量的增加 | |
| C. | 化學反應速率可以衡量化學反應進行的快慢 | |
| D. | 對于任何化學反應來說,反應速率越快,反應現(xiàn)象越明顯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
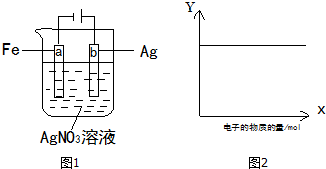
| A. | ①③ | B. | ③④ | C. | ①②④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3.2 | B. | 0.2 | C. | $\frac{1}{180}$ | D. | $\frac{4}{45}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 弱酸的化學式 | CH3COOH | HCN | H2S |
| 電離常數(shù)(25℃) | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
| A. | 等物質的量濃度的各溶液pH關系為:pH(CH3COONa)>pH(Na2S)>pH(NaCN) | |
| B. | NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) | |
| C. | a mol/LHCN溶液與b mol/LNaOH溶液等體積混合,所得溶液中c(Na+)>c(CN-),則a一定小于或等于b | |
| D. | 某濃度的NaCN溶液的pH=d,則其中由水電離出的c(OH-)=10-dmol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
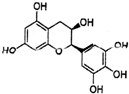 “茶倍健”牙膏中含有茶多酚,其中沒食子兒茶素(EGC)的結構如圖所示.關于EGC的下列敘述中正確的是( )
“茶倍健”牙膏中含有茶多酚,其中沒食子兒茶素(EGC)的結構如圖所示.關于EGC的下列敘述中正確的是( )| A. | 分子式為C15H13O7 | |
| B. | EGC可在強堿的醇溶液中發(fā)生消去反應 | |
| C. | 1molEGC最多消耗6molNaOH | |
| D. | 1molEGC加入溴水中,可與4molBr2發(fā)生取代反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
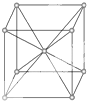
| A. | 是密置層的一種堆積方式 | B. | 晶胞是六棱柱 | ||
| C. | 每個晶胞內含2個原子 | D. | 每個晶胞內含6個原子 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com