
【題目】(1)下列原子或離子的電子排布的表示方法中,正確的是___,違反了能量最低原理的是___,違反洪特規則的是__。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:![]()
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:![]()
綠柱石被國際珠寶界公認為四大名貴寶石之一。主要成分為Be3Al2[Si6O18],因含適量的Cr2O3(0.15~0.6%),而形成祖母綠。試回答下列問題:
(2)基態Al原子中,電子填充的最高能級是___,基態Cr原子的價電子排布式是___。
(3)用“>”或“<”填空:
第一電離能 | 沸點 | 離子半徑 |
Be___B | H2S___H2O | Al3+___O2- |
(4)卟啉與Fe2+合即可形成血紅素,Fe2+的電子排布式為___,鐵在周期表中的位置為__。
【答案】①⑤⑥ ② ③④⑦ 3p 3d54s1 > < < 1s22s22p63s23p63d6 第四周期第Ⅷ族
【解析】
(1)根據構造原理確定核外電子排布式是否正確,能量最低原理:原子核外電子先占有能量較低的軌道.然后依次進入能量較高的軌道;泡利不相容原理:每個原子軌道上最多只能容納 2個自旋狀態 相反的電子;洪特規則:在等價軌道(相同電子層、電子亞層上的各個軌道)上排布的電子將盡可能分占不同的軌道,且自旋方向相同。
(2)根據核外電子排布規律可以寫出價電子排布式,根據充滿和半充滿狀態能量最低也是最穩定的狀態進行分析;
(3)Be、B同周期自左而右元素的第一電離能呈增大趨勢,ⅡA族反常;水分子間含有氫鍵;核外電子數相同的,原子序數越大,半徑越小;
(4)Fe是26號元素,其原子核外有26個電子,失去兩個最外層電子生成亞鐵離子,根據構造原理書寫其核外電子排布式;
(1)①正確;②違反了能力最低原子;③違反了洪特規則;④違反了洪特原則;⑤正確;⑥正確;⑦違反了洪特規則;故答案為:①⑤⑥;②;③④⑦;
(2)Al為13號元素,其電子排布式為1s22s22p63s23p1,最高能級為3p,根據核外電子排布規律可以寫出基態鉻價電子排布式為1s22s22p63s23p63s23p63d54s1,所以基態鉻(Cr)原子的價電子排布式是3d54s1,故答案為:3p;3d54s1;
(3)同周期自左而右元素的第一電離能呈增大趨勢,但ⅡA族最外層為ns能級容納2個電子,為全滿確定狀態,能量較低,第一電離能高于同周期相鄰元素,故第一電離能B<Be;水分子間含有氫鍵,使得水的分子間作用力大于硫化氫分子的,故水的沸點大;電子層數越多半徑越大,核外電子數相同的,原子序數越大,半徑越小,O2-、Al3+有2個電子層,O的原子序數小所以O2-半徑比Al3+大,所以離子半徑O2->Al3+,故答案為:>;<;<;
(4)Fe是26號元素,其原子核外有26個電子,失去兩個最外層電子生成亞鐵離子,根據構造原理書寫其核外電子排布式為1s22s22p63s23p63d6,鐵元素在元素周期表的位置為第四周期第Ⅷ族,故答案為:1s22s22p63s23p63d6;第四周期第Ⅷ族。


科目:高中化學 來源: 題型:
【題目】在![]() 時,在濃度為
時,在濃度為![]() 的
的![]() 、
、![]() 、
、![]() 的溶液中,已知醋酸的電離常數約等于一水合氨的電離常數,下列判斷正確的是
的溶液中,已知醋酸的電離常數約等于一水合氨的電離常數,下列判斷正確的是![]()
A.由水電離出的![]() 最大的是
最大的是![]()
B.三種溶液的pH值最小的![]()
C.三種溶液中![]() 最大的是
最大的是![]()
D.三種溶液中只有![]() 顯堿性
顯堿性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗方案能達到相應實驗目的的是
選項 | 實驗目的 | 實驗方案 |
A | 檢驗蔗糖水解生成葡萄糖 | 取適量蔗糖溶于盛有蒸餾水的試管中,滴入稀硫酸加熱一段時間,冷卻,滴入新制氫氧化銅懸濁液,加熱至沸騰,觀察有無磚紅色沉淀 |
B | 實驗室制備氫氧化鐵膠體 | 向盛有25mL蒸餾水的燒杯中滴入5-6滴氯化鐵飽和溶液,加熱煮沸至溶液呈紅褐色,停止加熱 |
C | 比較AgCl、AgI的Ksp大小 | 向盛有10滴0.1mol/LAgNO3 溶液的試管中滴加0.1mol/LNaCl溶液至不再有沉淀生成,再滴加0.1mol/lKI溶液 |
D | 比較Mg、Al的金屬性強弱 | 用導線連接鎂和鋁片,插入盛有氫氧化鈉溶液的燒杯中,觀察氣泡 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】融雪劑通過降低冰雪融化溫度的原理融化道路上的積雪。研究發現,一般融雪劑殘留物可腐蝕路面和汽車輪胎等。目前我國北方在冬季仍采用沙土和鏟雪車為主,融雪劑為輔的方式清除路面冰雪,保證道路通暢。
請回答下列問題:
(1)氯化鈣是常用融雪劑的主要成分之一,以工業碳酸鈣(含有少量Na+、Mg2+、Fe3+等雜質)生產氯化鈣的主要流程如下:

①流程中試劑W的名稱是 ________________。
②流程中濾渣的主要成分是________________(填化學式)。
③流程中操作Y的目的是_______________。
④如果用惰性電極電解用試劑W溶解后的溶液,則電解開始時陰極發生的電極反應式為_________。
(2)下列就融雪劑使用的有關原理的解釋正確的是_________________。
A.“會加快冰雪的融化”是因為提高了冰點
B.“會造成綠化植物死亡”是與鹽析有關
C.“會造成土壤板結貧瘠”是與物質的分解吸熱有關
D.“會加快路基上鐵的腐蝕”是與形成原電池有關
(3)某公司生產的融雪劑由NaCl、NaNO3、AlCl3、CuSO4、K2CO3中的幾種物質組成。某同學設計下列過程探究其組成:
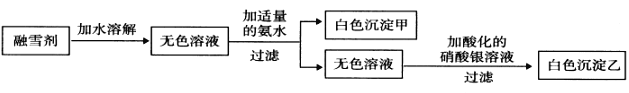
請回答下列問題:
①該融雪劑中一定不含的物質是_________________(填名稱)。
②若取融雪劑樣品a g,通過上述探究途徑得白色沉淀乙bmol,則該融雪劑中含氯元素的質量分數為 ____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某燒堿溶液中含有少量雜質(不與鹽酸反應),現用中和滴定測定其濃度。
(1)用___式滴定管盛裝cmol/L鹽酸標準液。配制c mol/L鹽酸標準液,必須使用的主要容器是___。如圖表示某次滴定時50mL滴定管中前后液面的位置。滴定管讀數時應注意___。用去的標準鹽酸的體積是___mL。
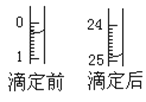
(2)該實驗應選用__(填“酚酞”或者“石蕊”)作指示劑;操作中如何確定終點?__。
(3)對下列兩種假定情況進行討論:(填“無影響”、“偏高”、“偏低”)
a.若滴定前用蒸餾水沖洗錐形瓶,則會使測定結果___;
b.若在滴定過程中不慎將數滴酸液滴在錐形瓶外,則會使測定結果___;
C,讀數時,若滴定前仰視,滴定后俯視,則會使最終測定結果___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】t ℃時,某平衡體系中含有X、Y、Z、W四種物質,此溫度下發生反應的平衡常數表達式為K=![]() 。有關該平衡體系的說法正確的是
。有關該平衡體系的說法正確的是
A. 當混合氣體的平均相對分子質量保持不變時,反應達平衡
B. 增大壓強,各物質的濃度不變
C. 升高溫度,平衡常數K增大
D. 增加X的量,平衡既可能正向移動,也可能逆向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NOx會造成大氣污染,在工業上采用多種方法進行處理。
I.氧化法:煙氣中的NO經O3預處理后轉化為NO2,再用CaSO3懸濁液吸收NO2。
已知:常溫下,CaSO4的沉淀溶解平衡常數數值為9.1×10-6,CaSO3的沉淀溶解平衡常數數值為3.1×10-7。
(1)NO與O3反應過程的能量變化如下:
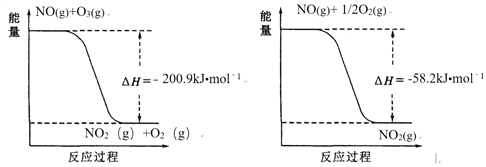
NO被O3氧化的總反應是化合反應,該反應的熱化學方程式為 ________。
(2)將CaSO3懸濁液靜置,取上層清液,測得pH約為8,用化學用語解釋其原因為________。
(3)用CaSO3懸濁液吸收NO2,將其轉化為HNO2,該反應的化學方程式為________。
(4)在實際吸收NO2的過程中,通過向CaSO3懸濁液中加入Na2SO4固體,提高NO2的吸收速率,從溶解平衡的角度解釋其原因:________。
II. 選擇性非催化還原法:該反應不使用催化劑,但必須在高溫有氧下利用NH3做還原劑與 NOx 進行選擇性反應:4NH3 + 4NO + O2 ![]() 3N2 + 6H2O,不同溫度(T)下,反應時間(t)與NO濃度的關系如右圖所示。
3N2 + 6H2O,不同溫度(T)下,反應時間(t)與NO濃度的關系如右圖所示。
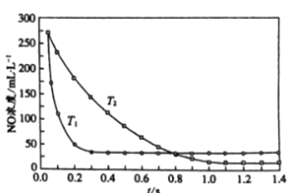
(5)判斷該反應為________(填“吸熱”或“放熱”)反應,說明理由:________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作與預期實驗目的或所得實驗結論一致的是![]()
選項 | 實驗操作 | 實驗目的或結論 |
A | 向含有少量 | 除去 |
B | 向某溶液中加入 | 證明溶液中含 |
C | 向某溶液中加入稀鹽酸,放出無色無味氣體,將氣體通入澄清石灰水,石灰水變渾濁 | 證明該溶液中存在 |
D | 向 | 證明 |
A.AB.BC.CD.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】微型紐扣電池在現代生活中應用廣泛。有一種銀鋅電池,其電極分別是Ag2O和Zn,電解質溶液為KOH溶液,總反應是Zn+Ag2O=ZnO+2Ag。

請回答下列問題。
(1)該電池屬于_________電池(填“一次”或“二次”)。
(2)負極是_________,電極反應式是__________________________。
(3)使用時,正極區的pH_________(填“增大”、“減小”或“不變”)。
(4)事實證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理論上可以設計成原電池的是_____。(填字母)
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2CO(g)+O2(g)=2CO2(1) △H<0
(5)以KOH溶液為電解質溶液,依據所選反應設計一個原電池,其負極的電極反應式為__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com