
【題目】下列物質中屬于有機物的是 ( )
A. 氯化鉀B. 二氧化碳C. 碳酸鈉D. 乙烷
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】Ⅰ.用固體燒堿配制480mL 0.1 mol·L-1的NaOH溶液,請回答以下問題:
(1)需稱量_______g燒堿固體,它應盛在_____中進行稱量。
(2)配制過程中,不需要使用的儀器是(填序號)_____________。
A、托盤天平 B、藥匙 C、燒杯 D、膠頭滴管 E、玻璃棒 F、1000mL容量瓶 G、500mL容量瓶
(3)若配制0.1 mol·L-1的NaOH溶液的其他操作均正確,但出現下列錯誤操作,其中將使配制的NaOH溶液濃度偏高的是___________(填序號)。
A.將NaOH溶液轉移至容量瓶后,未洗滌燒杯和玻璃棒
B.將燒杯內的NaOH溶液向容量瓶中轉移時,因操作不當使部分濺出瓶外
C.定容搖勻后,發現液面低于刻度線,又加水至液面與刻度線相切
D.定容時俯視容量瓶的刻度線
Ⅱ.欲用98% 的濃硫酸(ρ=1.84 g·cm-3 )配制成濃度為0.5 mol·L-1 的稀硫酸480mL。
(1)所需濃硫酸的體積為___mL。
(2)選用的主要儀器有:燒杯、量筒、膠頭滴管、玻璃棒和___。
(3)操作正確的順序為_____(填序號)。
A.用量筒量取濃硫酸 B.反復顛倒搖勻 C.用膠頭滴管加水至刻度
D.將配制好的溶液轉入試劑瓶中貼上標簽 E.稀釋濃硫酸 F.將溶液轉入容量瓶
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組為了探究一種有機鹽 X(僅含四種元素)的組成與性質,設計并完成如下實驗:

已知: A為兩種常見氣體的混合物, B、 C 均為常見物質。
(1)X中除含有氫、氧元素外,還含有的元素為:________________(寫元素名稱)。
(2)寫出 X 受熱分解的化學方程式:____________________________________________。
(3)設計實驗驗證“紅棕色固體”中金屬陽離子______________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以Na2SO3溶液和不同金屬的硫酸鹽溶液作為實驗對象,探究鹽的性質和鹽溶液間反應的多樣性。
實驗 | 試劑 | 現象 | |
滴管 | 試管 | ||
| 0.2 mol·L1Na2SO3溶液 | 飽和Ag2SO4溶液 | Ⅰ.產生白色沉淀 |
0.2 mol·L1CuSO4 | Ⅱ.溶液變綠,繼續滴加產生棕黃色沉淀 | ||
0.1 mol·L1Al2(SO4)3溶液 | Ⅲ.開始無明顯變化,繼續滴加產生白色沉淀 | ||
(1)經檢驗,現象Ⅰ中的白色沉淀是Ag2SO3。用離子方程式解釋現象Ⅰ:____________。
(2)經檢驗,現象Ⅱ的棕黃色沉淀中不含SO42,含有Cu+、Cu2+和SO32。
已知:Cu+![]() Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸證實沉淀中含有Cu+的實驗現象是_____________。
②通過下列實驗證實,沉淀中含有Cu2+和SO32。

a.白色沉淀A是BaSO4,試劑1是____________。
b.證實沉淀中含有Cu+和SO32的理由是___________。
(3)已知:Al2(SO3)3在水溶液中不存在。經檢驗,現象Ⅲ的白色沉淀中無SO42,該白色沉淀既能溶于強酸,又能溶于強堿,還可使酸性KMnO4溶液褪色。
①推測沉淀中含有亞硫酸根和________。
②對于沉淀中亞硫酸根的存在形式提出兩種假設:i.唄Al(OH)3所吸附;ii.存在于鋁的堿式鹽中。對假設ii設計了對比實驗,證實了假設ii成立。
a.將對比實驗方案補充完整。

步驟二:_____________(按上圖形式呈現)。
(4)根據實驗,亞硫酸鹽的性質有___________。鹽溶液間反應的多樣性與__________有關。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】丙烯腈(CH2=CHCN)是一種重要的化工原料,工業上可用“丙烯氨氧化法”生產,主要副產物有丙烯醛(CH2=CHCHO)和乙腈CH3CN 等,回答下列問題:
(1)以丙烯、氨、氧氣為原料,在催化劑存在下生成丙烯睛(C3H3N)和副產物丙烯醛(CH2=CHCHO)的熱化學方程式如下:
① C3H6(g)+NH3(g)+O2(g)=C3H3N(g)+3H2O(g)△H=-515kJ/mol
② C3H6(g)+O2(g)=C3H4O(g)+H2O(g) △H=-353kJ/mol
有利于提高丙烯腈平衡產率的反應條件是______;提高丙烯腈反應選擇性的關鍵因素是_____.
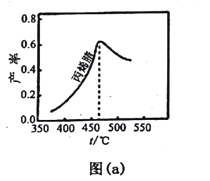
(2)圖(a)為丙烯腈產率與反應溫度的關系曲線,最高產率對應溫度為460℃。低于460℃時,丙烯腈的產率________(填“是”或者“不是”)對應溫度下的平衡產率,判斷理由是_____;高于460℃時,丙烯腈產率降低的可能原因是________(雙選,填標號)。
A.催化劑活性降低 B.平衡常數變大 C.副反應增多 D. 反應活化能增大
(3)丙烯腈和丙烯醛的產率與n(氨)/n(丙烯)的關系如圖(b)所示。由圖可知,最佳n(氨)/n(丙烯)約為_________ ,理由是_______。進料氨、空氣、丙烯的理論體積約為____________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某燒堿樣品中含有少量不與酸作用的可溶性雜質,為了測定其純度,進行以下滴定操作:
A.用250mL容量瓶等儀器配制成250mL燒堿溶液;
B.用移液管(或堿式滴定管)量取25mL燒堿溶液于錐形瓶中并加幾滴甲基橙指示劑;
C.在天平上準確稱取燒堿樣品W g,在燒杯中加蒸餾水溶解;
D.將物質的量濃度為M molL﹣1的標準HCl溶液裝入酸式滴定管,調整液面,記下開始刻度數V1 mL;
E.在錐形瓶下墊一張白紙,滴定到終點,記錄終點耗酸體積V2 mL。
回答下列問題:
(1)正確的操作步驟是(填寫字母)________→________→________→D→________;
(2)滴定時,左手握酸式滴定管的活塞,右手搖動錐形瓶,眼睛注視________________;
(3)終點時顏色變化是_____________________;
(4)在上述實驗中,下列操作(其他操作正確)會造成測定結果偏高的有_____(填字母序號);
A.滴定終點讀數時俯視 B.錐形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用鹽酸潤洗 D.酸式滴定管在滴定前有氣泡,滴定后氣泡消失
(5)該燒堿樣品的純度計算式是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表是一座開放的“元素大廈”,”元素大廈”尚未客滿。若發現120號元素,請在“元素大廈”中安排好它的“房間”
A.第七周期0族B.第七周期第IIA族C.第八周期第IIA族D.第八周期第IA族
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積不變的密閉容器中,一定條件下進行反應:NO(g)+CO(g)=1/2N2(g)+CO2(g) ΔH=-373.2 kJ/mol。如圖曲線a表示該反應過程中,NO的轉化率與反應時間的關系,若改變起始條件,使反應過程按照曲線b進行,可采取的措施是( )

A. 加催化劑 B. 向密閉容器中加入氬氣
C. 降低溫度 D. 增大反應物中NO的濃度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com