
| 氫氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 開始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 完全沉淀的pH | 5.2 | 3.7 | 9.7 | 6.7 |
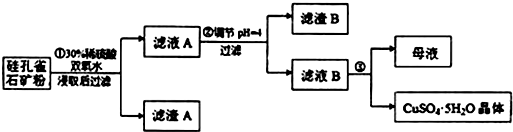
分析 硅孔雀石是一種含銅礦石,含銅形態為CuCO3•Cu(OH)2和CuSiO3•2H2O,同時含有SiO2、FeCO3、Fe2O3、A12O3等雜質,硅孔雀石礦粉加入稀硫酸溶解,加入過氧化氫氧化亞鐵離子浸取后過濾,得到濾渣主要為SiO2、H2SiO3,濾液A在含有Cu2+、Fe3+、Al3+、H+,加入銅的化合物調節溶液pH=4使鐵離子全部沉淀,此時鋁離子有部分沉淀,過濾得到濾液B主要是硫酸銅溶液,含有少量硫酸鋁和硫酸溶液,通過蒸發濃縮蒸發,冷卻結晶得到硫酸銅晶體,
(1)硅酸銅和硫酸反應生成硫酸銅、硅酸,雙氧水具有強氧化性,可氧化亞鐵離子;
(2)調節pH時注意不能引入新雜質;
(3)根據氫氧化物開始沉淀和完全沉淀的pH列表進行分析PH=4完全沉淀、不完全沉淀的離子;
(4)根據氫氧化鋁的溶度積以及溶液的pH=4,計算出鋁離子的濃度,再進行判斷是否有硫酸鋁析出.
解答 解:(1)利用質量守恒定律,可以判斷未知物是硅酸,利用觀察法配平反應方程式為:CuSiO3•2H2O+H2SO4═CuSO4+H4SiO4+H2O;雙氧水將亞鐵離子氧化成鐵離子的離子方程式為:2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案為:H4SiO4;2Fe2++H2O2+2H+═2Fe3++2H2O;
(2)由于濾液A顯示酸性,加入的試劑能夠中和溶液中的氫離子,還不能引進新的雜質,所以應該選用B氧化銅,故答案為:B;
(3)有表中數據可知,pH=4時,三價鐵離子完全生成了氫氧化鐵沉淀,而鋁離子完全沉淀需要的pH是5.2,所以鋁離子沒有完全沉淀,
故答案為:Fe3+;Al3+;
(4)pH=4時,溶液中的氫氧根離子的濃度為:1×10-10mol/L,溶液中鋁離子濃度為:$\frac{3.2×1{0}^{-34}}{({1×1{0}^{-10})}^{3}}$mol/L=3.2×10-4mol/L,濃縮后c(Al3+)=6.4×10-4mol/L<<2.25mol/L,所以不會有硫酸鋁晶體析出,
故答案為:該同學的觀點是錯誤的;通過計算可知,濾液B中,c(Al3+)=3.2×10-4mol/L,濃縮后c(Al3+)=6.4×10-4mol/L<<2.25mol/L,所以不會有硫酸鋁晶體析出.
點評 本題借助硅孔雀石為原料制取硫酸銅的工藝流程,為高考常見題型,側重于學生的分析能力、實驗能力和計算能力的熬成,題目側重考查了化學方程式書寫、誤差分析、化學計算等知識,難度中等.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相對分子質量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔點/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸點/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 與水互溶 | 可溶于水,乙醇 | 可溶于水,乙醇,三氯乙醛 | 微溶于水,可溶于乙醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
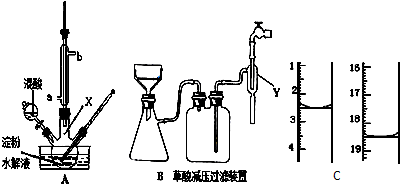
 200.00mL溶液(黃綠色)$→_{通入適量SO_{2}△}^{(2)還原}$CuCl(白色沉淀)
200.00mL溶液(黃綠色)$→_{通入適量SO_{2}△}^{(2)還原}$CuCl(白色沉淀)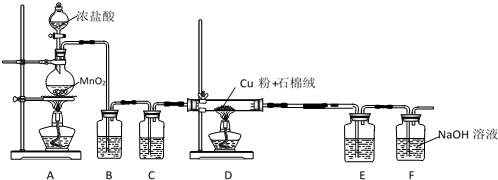
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
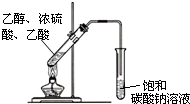 以乙烯為原料,可以制備乙酸乙酯
以乙烯為原料,可以制備乙酸乙酯查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=+534 kJ•L-1 | |
| B. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=-53.4 kJ•L-1 | |
| C. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=+53.4 kJ•L-1 | |
| D. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=-534 kJ•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
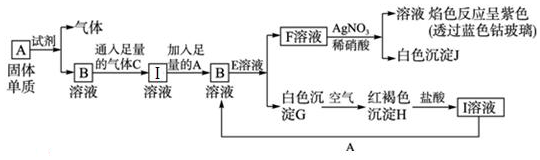
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com