
海水是一個巨大的化學資源寶庫,利用海水可以獲得很多化工產品。
(1)海水中制得的氯化鈉可用于生產燒堿及氯氣。反應的離子方程式是 。

(2)利用制鹽后的鹽鹵提取溴的工藝流程如下(部分操作和條件已略去):
將Br2與Na2CO3反應的化學方程式補充完整:
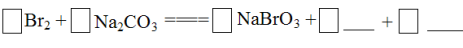
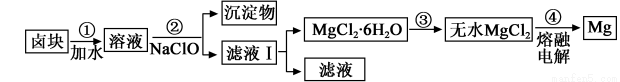
(3)鹽鹵蒸發冷卻后析出鹵塊的主要成分是MgCl2,此外還含Fe2+、Fe3+、Mn2+等離子。以鹵塊為原料制得鎂的工藝流程如下(部分操作和條件已略去):
生成氫氧化物沉淀的pH
物質 | 開始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH) 2 | 9.6 | 11.1 |
①步驟②中需控制pH=9.8,其目的是 。
② 用NaClO 氧化Fe2+得到Fe(OH)3沉淀的離子反應方程式是 。
③ 步驟③需在HCl保護氣中加熱進行,請用化學平衡移動原理解釋原因____________。
④ NaClO還能除去鹽鹵中的CO(NH2)2,生成鹽和能參與大氣循環的物質。除去0.1mol CO(NH2)2時消耗NaClO g。
 寶貝計劃期末沖刺奪100分系列答案
寶貝計劃期末沖刺奪100分系列答案 能考試全能100分系列答案
能考試全能100分系列答案科目:高中化學 來源:2016-2017學年河南省南陽市高一上學期期中化學試卷(解析版) 題型:推斷題
下圖表示的是A-E五種物質間的相互轉化關系,其中A為淡黃色固體,B為單質。試推出各物質的化學式,并寫出B→C、C→D、D→E、A→C反應的離子方程式。
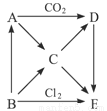
(1)A B C D
(2)B→C
(3)C→D
(4)D→E
(5)A→C
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上調研三化學卷(解析版) 題型:選擇題
下列各種情況下一定能大量共存的離子組為( )
A.pH=7的溶液中:Fe3+、Cl-、Na+、NO
B.由水電離出的c(H+)=1×10-13mol/L的溶液中:Na+、CO 、Cl-、K+
、Cl-、K+
C.pH=1的溶液中:NH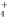 、Cl-、Cu2+、SO
、Cl-、Cu2+、SO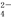
D.無色溶液中:Al3+、HCO 、、I-、K+
、、I-、K+
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省廣州市高三12月模擬化學試卷(解析版) 題型:實驗題
鎳及其化合物用途廣泛。某礦渣的主要成分是NiFe2O4(鐵酸鎳)、NiO、FeO、CaO、SiO2等,以下是從該礦渣中回收NiSO4的工藝路線:
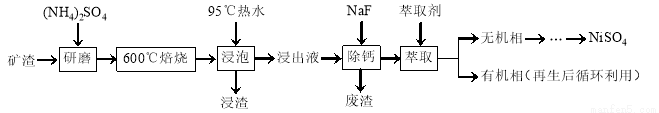
已知:(NH4)2SO4在350℃以上會分解生成NH3和H2SO4。NiFe2O4在焙燒過程中生成NiSO4、Fe2(SO4)3。錫(Sn)位于第五周期第ⅣA族。
(1)焙燒前將礦渣與(NH4)2SO4混合研磨,混合研磨的目的是______________。
(2)“浸泡”過程中Fe2(SO4)3生成FeO(OH)的離子方程式為______________,“浸渣”的成分除Fe2O3、FeO(OH)外還含有______________(填化學式)。
(3)為保證產品純度,要檢測“浸出液”的總鐵量:取一定體積的浸出液,用鹽酸酸化后,加入SnCl2將Fe3+還原為Fe2+,所需SnCl2的物質的量不少于Fe3+物質的量的________倍;除去過量的SnCl2后,再用酸性K2Cr2O7標準溶液滴定溶液中的Fe2+,還原產物為Cr3+,滴定時反應的離子方程式為______________。
(4)“浸出液”中c(Ca2+) = 1.0×10-3mol·L-1,當除鈣率達到99%時,溶液中c(F-) = ________ mol·L-1。[已知Ksp (CaF2)=4.0×10-11]
(5)本工藝中,萃取劑與溶液的體積比(V0/VA)對溶液中Ni2+、Fe2+的萃取率影響如圖所示,V0/VA的最佳取值是________。
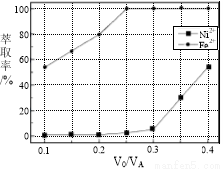
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省廣州市高三12月模擬化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的值。下列有關敘述正確的是( )
A.標準狀況下,22.4 L CH4含有的共價鍵數為NA
B.1 mol Fe與1mol Cl2充分反應,電子轉移數為3NA
C.常溫下,pH =2的醋酸溶液中含有的H+數目為0.02NA
D.常溫常壓下,46g的NO2和N2O4混合氣體含有的原子數為3NA
查看答案和解析>>
科目:高中化學 來源:2017屆北京市高三12月月考化學試卷(解析版) 題型:選擇題
W、X、Y、Z是四種常見的短周期元素,其原子半徑隨原子序數變化如右圖。已知W的一種核素的質量數為18,中子數為10;X和Ne原子的核外電子數相差1;Y的單質是一種常見的半導體材料;Z的非金屬性在同周期元素中最強,下列說法正確的是( )
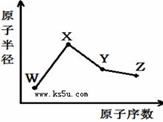
A. 最高化合價X>Y>Z>W
B. 氣態氫化物的穩定性Z>Y>W
C. Y的氧化物與X、Z的最高價氧化物對應的水化物均能反應
D. X、Z、W三種元素形成的化合物一定既含離子鍵又含共價鍵
查看答案和解析>>
科目:高中化學 來源:2017屆北京市高三12月月考化學試卷(解析版) 題型:選擇題
北京大學和中國科學院的化學工作者已成功研制出堿金屬與C60形成的球碳鹽K3C60,實驗測
知該物質屬于離子化合物,具有良好的超導性。下列有關分析正確的是( )
A.K3C60中只有離子鍵
B.K3 C60中不含共價鍵
C60中不含共價鍵
C.該晶體在熔融狀態下能導電
D.C60與12C互為同素異形體
查看答案和解析>>
科目:高中化學 來源:2017屆四川省高三12月月考化學試卷(解析版) 題型:實驗題
磷化鋁、磷化鋅、磷化鈣是目前常見的熏蒸殺蟲劑,都能與水或酸反應產生有毒氣體膦(PH3),PH3具有較強的還原性,能在空氣中自燃。衛生安全標準規定,糧食中磷化物(以PH3計)含量≤0.05mg/kg。某化學興趣小組的同學通過下列方法對糧食中殘留磷化物含量進行研究:
【操作流程】安裝吸收裝置→PH3的產生與吸收→轉移KMnO4吸收溶液→亞硫酸標準溶液滴定
【實驗裝置】
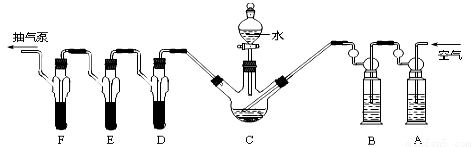
C中盛有200g原糧,D、E、F 各盛裝1.00mL濃度為1.00×10-3mol/L的KMnO4 溶液(H2SO4 酸化)。
請回答下列有關問題:
(1)儀器G的名稱是 。以磷化鋁為例,寫出磷化鋁與水反應的化學方程式 。
(2)檢查C裝置氣密性的方法是:用止水夾夾緊C裝置 ,取下上口活塞,漏斗中加入水,打開下口旋塞,觀察到 ,表明裝置氣密性良好。
(3)實驗過程中,用抽氣泵反復抽氣的目的是 。
(4)A中盛裝KMnO4溶液是為除去空氣中可能含有的 (填“還原”或“氧化”)性氣體;B中盛裝新制FeSO4溶液的作用是 ;
(5)已知 D、E、F 中發生同一反應,實驗中 PH3被氧化成磷酸,寫出所發生的化學反應方程式 ;收集裝置D、E、F所得吸收液,并洗滌D、E、F,將吸收液、洗滌液一并置于錐形瓶中,加水稀釋至25mL,用濃度為5×10-4 mol/LNa2SO3標準溶液滴定剩余的KMnO4溶液,消耗Na2SO3標準溶液11.00mL,則該原糧中磷化物(以PH3計)的含量為 mg/kg。
查看答案和解析>>
科目:高中化學 來源:2017屆福建省高三上學期階段考二化學試卷(解析版) 題型:選擇題
下列化學用語表達不正確的是 ( )
A.丙烷的分子結構球棍模型示意圖:
B.PCl5中各原子最外層均能達到8電子的穩定結構
C.二氧化碳的結構式: O=C=O
D.碳酸氫鈉的電離方程式:NaHCO3= Na+ + HCO3ˉ
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com