
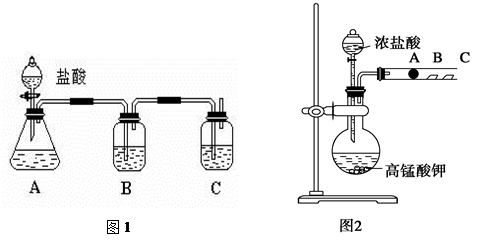


科目:高中化學 來源:不詳 題型:單選題
| X | Y | Z | |
| A | FeCl2溶液 | FeCl3 | KSCN溶液 |
| B | CO2 | HCl | 飽和Na2CO3溶液 |
| C | KCl溶液 | MgCl2 | 適量NaOH溶液 |
| D | FeCl2溶液 | CuCl2 | Fe粉 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題

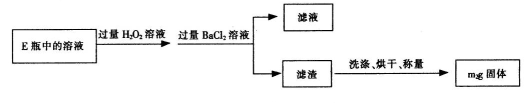
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.觀察法 | B.分類法 | C.實驗法 | D.比較法 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
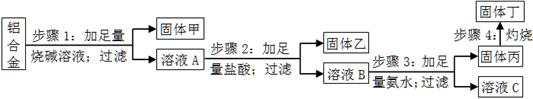
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
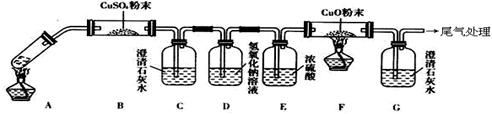
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
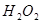 分解反應速率的影響,某同學在四支試管中分別加入
分解反應速率的影響,某同學在四支試管中分別加入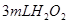 溶液,并測量收集
溶液,并測量收集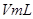 氣體所需的時間,實驗記錄如下:
氣體所需的時間,實驗記錄如下:| 實驗序號 | 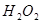 溶液濃度 溶液濃度 | 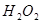 溶液溫度 溶液溫度 | 催化劑 | 所用時間 |
| ① | 5% | 20℃ | 2滴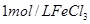 | 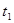 |
| ② | 5% | 40℃ | 2滴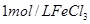 | 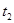 |
| ③ | 10% | 20℃ | 2滴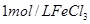 | 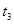 |
| ④ | 5% | 20℃ | 不使用 | 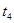 |
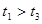 ,原因是__________。
,原因是__________。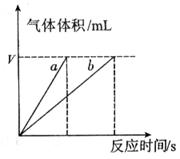
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
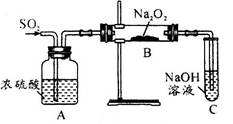
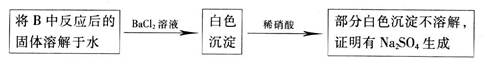
 CO2↑+CO↑+H2O
CO2↑+CO↑+H2O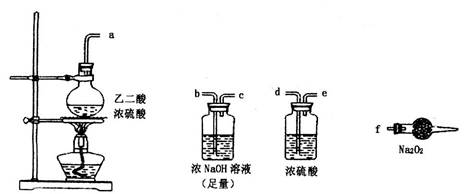
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com