
 已知反應X(g)+Y(g)═nZ(g)△H>0,將X和Y以一定比例混合通入密閉容器中進行反應,各物質的濃度隨時間的改變如圖所示.下列說法不正確的是( )
已知反應X(g)+Y(g)═nZ(g)△H>0,將X和Y以一定比例混合通入密閉容器中進行反應,各物質的濃度隨時間的改變如圖所示.下列說法不正確的是( )| A. | 反應方程式中n=1 | |
| B. | 10min時,曲線發生變化的原因是升高溫度 | |
| C. | 10min時,曲線發生變化的原因是增大壓強 | |
| D. | 該反應的△S<0 |
分析 A.10min時反應物和生成物濃度瞬間同時增大,說明是增大了壓強,反應物濃度逐漸減小,生成物濃度增加,平衡正向移動,則說明該反應是體積縮小的反應,即n=1,據此判斷;
B.根據圖象數據可知,10min時反應物和生成物濃度瞬間同時增大,則說明10min時增大了壓強,據此判斷;
C.根據圖象數據可知,10min時反應物和生成物濃度瞬間同時增大,則說明10min時增大了壓強,據此判斷;
D.達到平衡時,增大壓強后反應物濃度逐漸減小,生成物濃度增加,說明該反應是體積縮小的反應,即n=1,該反應是熵變減小的反應.
解答 解:A.10min時反應物和生成物濃度瞬間同時增大,說明是增大了壓強,反應物濃度逐漸減小,生成物濃度增加,平衡正向移動,則說明該反應是體積縮小的反應,即n=1,故A正確;
B.根據圖象數據可知,10min時反應物和生成物濃度瞬間同時增大,則說明10min時增大了壓強,故B錯誤;
C.根據圖象數據可知,10min時反應物和生成物濃度瞬間同時增大,則說明10min時增大了壓強,故C正確;
D.由于10min時增大壓強后,在重新達到平衡狀態過程中,反應物濃度逐漸減小,生成物濃度逐漸增加,說明平衡向著正向移動,根據增大壓強,平衡向著體積縮小的方向移動,所以該反應是體積縮小的反應,應該滿足n<1+1,則n=1,該反應是混亂度減小的反應,即△S<0,故D正確;
故選B.
點評 本題考查了化學平衡的影響因素、物質的量隨時間變化的曲線、化學反應速率的計算,題目難度中等,注意明確影響化學反應速率的因素,能夠正確分析物質的量隨時間變化的曲線是解題關鍵,還要明確化學反應速率的概念及計算方法.


 A加金題 系列答案
A加金題 系列答案 全優測試卷系列答案
全優測試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.2LCCl4中含有分子的數目為0.5NA | |
| B. | 標準狀況下,2.24LCl2通入水中生成NA個HClO | |
| C. | 1.6gO2與O3組成的混合物中所含O原子數為0.1NA | |
| D. | 25℃時pH=13的NaOH溶液中含有OH-的數目為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol MgCl2 | B. | 2mol KClO3 | C. | 1 mol AlCl3 | D. | 1.5 mol CaCl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol•L-1的硫酸銨溶液中:c(SO42->c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1 mol•L-1的硫化鈉溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 1.0×l0-3mol/L鹽酸的pH=3.0,1.0×10-8mol/L鹽酸的pH=8.0 | |
| D. | 常溫下,1mLpH=1的鹽酸與l00mL pH=11的NaOH溶液混合后,溶液的pH=7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 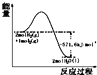 表示H2與O2發生反應過程中的能量變化,H2的燃燒熱為285.8 kJ/mol | |
| B. |  由圖得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入適量CuO,調節溶液的pH至4左右 | |
| C. |  表示用水稀釋pH相同的鹽酸和醋酸時溶液的pH變化曲線,其中Ⅰ表示醋酸,Ⅱ表示鹽酸,且溶液導電性:c>b>a | |
| D. |  表示常溫下向體積為10 mL 0.1 mol/LNaOH溶液中逐滴加入0.1 mol/L CH3COOH溶液后溶液的pH變化曲線,則b點處有:c(CH3COOH)+c(H+)=c(OH-) 表示常溫下向體積為10 mL 0.1 mol/LNaOH溶液中逐滴加入0.1 mol/L CH3COOH溶液后溶液的pH變化曲線,則b點處有:c(CH3COOH)+c(H+)=c(OH-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com