
分析 (1)元素原子質子數為17,主族元素周期數=電子層數、主族族序數=最外層電子數;
(2)該元素為Cl,原子序數12的元素為Mg,二者反應生成氯化鎂;
(3)發生反應:MgCl2+2AgNO3=2AgCl↓+Mg(NO3)2,生成AgCl白色沉淀,根據方程式計算消耗硝酸銀物質的量、生成AgCl的物質的量,根據V=$\frac{n}{c}$計算硝酸銀溶液體積,根據m=nM計算AgCl的質量.
解答 解:(1)元素原子質子數為17,原子核外有3個電子層,最外層電子數為7,處于周期表中第三周期ⅦA族,
故答案為:第三周期ⅦA族;
(2)該元素為Cl,原子序數12的元素為Mg,二者反應生成MgCl2,故答案為:MgCl2;
(3)設需要硝酸銀物質的量為x,生成AgCl的物質的量為y,則:
MgCl2+2AgNO3=2AgCl↓+Mg(NO3)2
1 2 2
0.05mol x y
所以x=y=0.05mol×2=0.1mol
故需要硝酸銀溶液體積為$\frac{0.1mol}{0.5mol/L}$=0.2L=200mL,
生成AgCl的質量為0.1mol×143.5g/mol=14.35g,
反應生成AgCl為白色沉淀,
故答案為:200;白;14.35.
點評 本題考查原子結構與元素性質、化學方程式的有關計算,比較基礎,有利于基礎知識的鞏固.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | Na、Mg、Al還原性依次減弱 | |
| B. | F2、Cl2、Br2、I2單質的氧化性依次減弱 | |
| C. | C、N、O原子半徑依次增大 | |
| D. | P、S、Cl最高正價依次升高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 相同條件下,NA個CO2分子和NA個H2O分子的體積一定相同 | |
| B. | 含NA個Na+的Na2O溶解于1L水中Na+的物質的量濃度為1mol/L | |
| C. | 電解58.5g熔融的NaCl能產生22.4L氯氣(標準狀況)和23.0g金屬鈉 | |
| D. | 一定條件下,2.3g的Na完全與O2反應生成3.6g產物時失去的電子書為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分類回收、利用垃圾,減少資源浪費 | |
| B. | 推廣使用一次性木筷,減少疾病傳染 | |
| C. | 減少公車使用,從而減少化石燃料的使用 | |
| D. | 研究煤和石油脫硫技術,減少酸雨發生 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
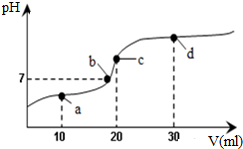 常溫下,向20mL 0.1mol•L-1醋酸溶液中不斷滴加0.05mol•L-1 Ba(OH)2(aq),在這個過程中,溶液的pH變化如圖所示(橫坐標為Ba(OH)2的體積),下列溶液中關于粒子濃度的敘述不正確的是( )
常溫下,向20mL 0.1mol•L-1醋酸溶液中不斷滴加0.05mol•L-1 Ba(OH)2(aq),在這個過程中,溶液的pH變化如圖所示(橫坐標為Ba(OH)2的體積),下列溶液中關于粒子濃度的敘述不正確的是( )| A. | a點:c(CH3COO-)>c(Ba2+)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | a至d點過程中:c(Ba2+)一定大于c(OH-) | |
| C. | c點:c(CH3COOH)+c(H+)=c(OH-) | |
| D. | d點:c(CH3COO-)>c(Ba2+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com