
X、Y、Z和W代表原子序數依次增大的四種短周期元素,它們滿足以下條件:
①元素周期表中,Z與Y相鄰,Z與W相鄰;
②X分別與Y、Z、W可組成化學式為YX3,X2Z和X2W三種共價化合物
請填空:
(1)X、Y、Z原子最外層電子數之和是________
(2)X2W的結構式是________
(3)X、Y和Z組成的一種化合物是強酸.寫出該酸的稀溶液與銅反應的離子方程式:
________________________________________________________________________
含Y、Z的氣體和一種只含X、Z的液體(在常溫、常壓下)反應可以生成一種離子化合物其化學式為________
(4)X、Y、Z和W組成一種化合物,其原子個數之比為5∶1∶3∶1;該化合物具有
還原性。
① 寫出該化合物與過量稀NaOH溶液反應的離子方程式:
________________________________________________________________________.
② 請設計實驗證明該化合物具有還原性:
________________________________________________________________________。
(9分) (1)12(1分)(2)H—??—H(1分)
(3)3Cu+ 8H++2NO=3Cu2++2NO↑+4H2O(2分) NH4NO3或NH4NO2(1分)
(4) ①NH+HSO+2OH-=NH3·H2O+H2O+SO(2分)
②取少許氯水,滴加該溶液,氯水褪色則說明該化合物具有還原性(KMnO4、溴水、
Fe3+等均可) (2分)
解析試題分析:X、Y、Z和W代表原子序數依次增大的四種短周期元素,它們滿足以下條件:
①元素周期表中,Z與Y相鄰,Z與W相鄰;②X分別與Y、Z、W可組成化學式為YX3,X2Z和X2W三種共價化合物。這說明Y、Z是第二周期元素,W是第三周期元素。因此X是H,則Y是N,Z是O、W是S。
(1)X、Y、Z原子最外層電子數之和是1+5+6=12。
(2)H2S的結構和水的結構相似,則H2S的結構式是H—??—H。
(3)X、Y和Z組成的一種化合物是強酸,則該強酸是硝酸。硝酸具有強氧化性,能和銅發生氧化還原反應,則硝酸的稀溶液與銅反應的離子方程式3Cu+ 8H++2NO=3Cu2++2NO↑+4H2O。含H、N、O三種元素的一種離子化合物的化學式為NH4NO3或NH4NO2。
(4)①X、Y、Z和W組成一種化合物,其原子個數之比為5∶1∶3∶1,則該化合物是NH4HSO3,與過量稀NaOH溶液反應的離子方程式是NH+HSO+2OH-=NH3·H2O+H2O+SO。
②+4價的S元素具有還原性,所以驗證其還原性的實驗方法是取少許氯水,滴加該溶液,氯水褪色則說明該化合物具有還原性。
考點:考查元素的推斷、結構式、方程式以及氧化性和還原性的檢驗等
點評:該題是中等難度的試題,試題貼近高考,基礎性強,在注重對學生基礎知識檢驗和訓練的同時,側重對學生能力的培養,有利于培養學生的邏輯推理能力和發散思維能力。準確判斷出元素是答題的關鍵。


科目:高中化學 來源: 題型:填空題
有X、Y、Z、W四種含14個電子的粒子,其結構特點如下:
| 粒子代碼 | X | Y | Z | W |
| 原子核數 | 單核 | 不同元素構成的兩核 | 同元素構成的兩核 | 同元素構成的兩核 |
| 粒子的電荷數 | 0 | 0 | 兩個負電荷 | 0 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
不同元素的原子在分子內吸引電子的能力大小可用一定數值x來表示, x越大,其原子吸引電子的能力越強。 下面是某些短周期元素的x值:
| 元素符號 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
X、Y、Z、M、G五種元素分屬三個不同短周期,且原子序數依次增大。X、Z同主族,可形成離子化合物ZX;Y、M同主族,可形成MY2、MY3兩種分子。Y2是空氣的主要成分之一。請回答下列問題:
(1)M在元素周期表中的位置為________________ 。
(2)Y、Z的單質或兩元素之間形成的化合物共有________種;Y、G的單質或兩元素之間形成的化合物可作水消毒劑的有 (寫出兩種物質的化學式)
(3)上述五種元素中兩元素形成的化合物之間可相互反應生成單質M的化學方程式為
。
(4)ZX與水反應放出氣體的化學方程式為___________________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
有原子序數依次增大的五種短周期元素A、B、C、D、E,已知 A、E同主族,A在所有元素中原子結構最簡單,B元素原子的最外層電子數是內層電子數的2倍,C元素的最高價氧化物的水化物X與其氫化物反應生成一種鹽Y;A、B、C、E四種元素都能與D元素分別形成原子個數比不相同的常見化合物,回答下列問題:
(1)B在周期表中的位置是 ,E的原子結構示意圖 。
(2)A與C形成化合物中含有的化學鍵屬于(填“極性鍵”或“非極性鍵”) 。
(3)用電子式表示化合物E2D的形成過程 。
(4)C元素的最高價氧化物的水化物與其氫化物反應的離子方程式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
1808年,英國化學家戴維用鉀還原氧化鎂,最早制得少量的鎂。鎂是航空工業的重要材料,鎂合金用于制造飛機機身、發動機零件等,一架超音速飛機約有5%的鎂合金構件,一枚導彈一般消耗100~200公斤鎂合金;鎂作為一種強還原劑,還用于鈦、鋯、鈹和鈾等的生產中;鎂是燃燒彈和照明彈不能缺少的組成物;鎂粉是節日煙花必需的原料。鎂及其合金是一種用途很廣泛的金屬材料,目前世界上60%的鎂是從海水中提取的。從海水(主要含NaCl和MgSO4)中提取金屬鎂的主要步驟如下:
回答下列問題:
(1)Mg在周期表中的位置______________________,試劑A可以選用_____________________,試劑C可選用_______________________;
(2)步驟①的離子方程式_________________________________________;
(3)用電子式表示氯化鎂的形成過程_______________________________;
(4)無水MgCl2在熔融狀態下,通電后會產生Mg和Cl2,該反應的化學方程式為:_____________________________________________________;
(5)戴維制鎂的化學方程式為_____________________________________;
(6)配平下列反應的方程式。
① 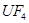 +
+ 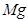 ——
——  +
+ 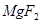
② 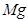 +
+ 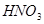 ——
—— 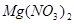 +
+ 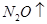 +
+ 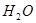
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(12分)下表為元素周期表的一部分,請參照元素①-⑨在表中的位置,用化學用語回答下列問題:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | | | ⑦ | ⑧ | ⑨ |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
金屬鎳及其化合物在合金材料以及催化劑等方面應用廣泛。請回答下列問題:
(1)Ni原子的核外電子排布式為______________________________;
(2)NiO、FeO的晶體結構類型均與氯化鈉的相同,Ni2+和Fe2+的離子半徑分別為69 pm和78 pm,則熔點NiO ________ FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位數分別為_______________、_______________;
(4)金屬鎳與鑭(La)形成的合金是一種良好的儲氫材料,其晶胞結構示意圖如左下圖所示。該合金的化學式為_______________;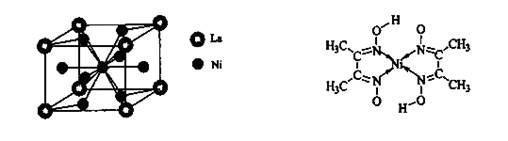
(5)丁二酮肟常用于檢驗Ni2+:在稀氨水介質中,丁二酮肟與Ni2+反應可生成鮮紅色沉淀,其結構如右上圖所示。
①該結構中,碳碳之間的共價鍵類型是 鍵,碳氮之間的共價鍵類型是______________,氮鎳之間形成的化學鍵是_______________;
鍵,碳氮之間的共價鍵類型是______________,氮鎳之間形成的化學鍵是_______________;
②該結構中,氧氫之間除共價鍵外還可存在_______________;
③該結構中,碳原子的雜化軌道類型有_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
某元素的核素為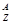 X,其氯化物XCl2 1.11 g配成溶液后,需用20 mL 1 mol·L-1的AgNO3溶液才能把氯離子完全沉淀下來。已知X核素中有20個中子。
X,其氯化物XCl2 1.11 g配成溶液后,需用20 mL 1 mol·L-1的AgNO3溶液才能把氯離子完全沉淀下來。已知X核素中有20個中子。
(1)計算X的質量數為多少?
(2)指出X元素在周期表中的位置。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com