
| 實 驗 操 作 | 現 象 | 實 驗 結 論 | |
| A | 向某溶液中加入硝酸酸化的氯化鋇溶液 | 生成白色沉淀 | 溶液中一定含有SO42- |
| B | 將某溶液蘸取少量放置于火焰上灼燒 | 火焰呈黃色 | 該溶液中一定含K+ |
| C | 往某溶液中加入KSCN溶液 | 顯血紅色 | 溶液中一定含有Fe3+ |
| D | 往某溶液中加入鹽酸 | 產生無色氣體 | 溶液中一定含有CO32- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.向某溶液中加入硝酸酸化的氯化鋇溶液,可能生成AgCl、BaSO4等沉淀;
B.根據鈉離子、鈉離子的焰色反應的火焰顏色判斷;
C.三價鐵離子遇到硫氰酸鉀顯示紅色;
D.能和鹽酸反應產生二氧化碳氣體的離子可以是碳酸根離子還可以是碳酸氫根離子.
解答 解:A.向某溶液中加入硝酸酸化的氯化鋇溶液,生成白色沉淀,不一定是SO42-,如果溶液中含有SO32-,能被氧化為SO42-,也不能排除生成AgCl沉淀,應先加鹽酸酸化,如無沉淀,再加入氯化鋇觀察,故A錯誤;
B.將某溶液蘸取少量放置于火焰上灼燒,火焰呈黃色,說明溶液中一定含有Na+,故B錯誤;
C.因Fe3+與SCN-發生反應:Fe3++3SCN-=Fe(SCN)3,溶液呈血紅色,所以溶液中滴入KSCN溶液后變紅,說明該溶液中含有Fe3+,故C正確;
D.某溶液加入足量鹽酸,放出的氣體能使澄清石灰水變渾濁,該氣體是二氧化碳或是二氧化硫,該溶液中含有CO32-、SO32-、HCO3-中的至少一種離子,故D錯誤;
故選C.
點評 本題考查了常見離子的檢驗方法,題目難度中等,明確常見離子的性質及檢驗方法為解答關鍵,注意檢驗離子的存在情況時,需要排除干擾離子,確保檢驗方案的嚴密性.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
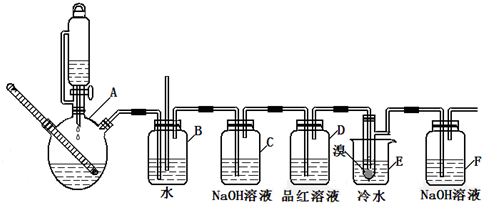
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 狀態 | 無色液體 | 無色液體 | 無色液體 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸點/℃ | 78.5 | 132 | 34.6 |
| 熔點/℃ | -l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com