
| 時間/s | 0 | 50 | 100 | 150 |
| c(N2O5)/mol.L-1 | 2.50 | 1.76 | 1.25 | 1.25 |
| A. | T1溫度下的平衡常數為K1,T2溫度下的平衡常數為K2,若T1>T2,則K1<K2 | |
| B. | 50s內N2O5分解速率為1.48×10-2mol.L-1.s-1 | |
| C. | T1溫度下的平衡常數為K1=15.625,平衡時N2O5的轉化率為50% | |
| D. | 達到平衡后其他 條件不變,將容器的體積壓縮到原來的$\frac{1}{2}$,則c(N2O5)>2.50mol.L-1 |
分析 A.平衡常數只受溫度影響,該反應正反應是吸熱反應,升高溫度,平衡向正反應移動,化學平衡常數增大;
B.根據v=$\frac{△c}{△t}$計算50s內N2O5分解速率;
C.100s、150s時,N2O5的濃度都是1.25mol/L,說明100s時反應到達平衡,利用三段式計算平衡時各組分的濃度、各物質的濃度變化量,代入平衡常數表達式K=$\frac{{c}^{4}(N{O}_{2})×c({O}_{2})}{{c}^{2}({N}_{2}{O}_{5})}$計算,N2O5的轉化率=$\frac{{N}_{2}{O}_{5}濃度變化量}{{N}_{2}{O}_{5}起始濃度}$×100%;
D.到平衡后其他條件不變,將容器的體積壓縮到原來的$\frac{1}{2}$,壓強增大一倍,平衡向逆反應方向移動.
解答 解:A.平衡常數只受溫度影響,該反應正反應是吸熱反應,升高溫度,平衡向正反應移動,若T1>T2,則K1>K2,故A錯誤;
B.50s內N2O5的濃度變化量為2.5mol/L-1.76mol/L=0.74mol/L,故N2O5分解速率為$\frac{0.74mol/L}{50s}$=1.48×10-2mol/(L•s),故B正確;
C.100s、150s時,N2O5的濃度都是1.25mol/L,說明100s時反應到達平衡,則:
2N2O5(g)?4NO2(g)+O2(g)
開始(mol/L):2.5 0 0
變化(mol/L):1.25 2.5 0.625
平衡(mol/L):1.25 2.5 0.625
故該溫度下,平衡常數k=$\frac{2.{5}^{4}×0.625}{1.2{5}^{2}}$=15.625,N2O5的轉化率=$\frac{1.25mol/L}{2.5mol/L}$×100%=50%,故C正確;
D.達到平衡后其他 條件不變,將容器的體積壓縮到原來的$\frac{1}{2}$,若平衡不移動,則c(N2O5)=2.50mol.L-1,但壓強增大一倍,平衡向逆反應方向移動,則c(N2O5)>2.50mol.L-1,故D正確,
故選A.
點評 本題考查化學反應速率計算、化學平衡影響因素、化學平衡平衡常數計算及影響因素等,難度中等,注意理解掌握外界條件對平衡移動的影響.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 恒溫下,將容器體積變為原來2倍,CO的平衡濃度變為原來的$\frac{1}{2}$ | |
| B. | 恒溫恒容下,增大壓強,H2濃度一定減小 | |
| C. | 升高溫度,正反應速率減小,逆反應速率增大 | |
| D. | 該反應化學方程式為CO2+H2?CO+H2O△H<0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AlCl3溶液中滴加足量氨水 | |
| B. | 向酚酞試液中通入過量Cl2 | |
| C. | 向紫色石蕊試液中通入過量SO2 | |
| D. | 向酚酞試液中加入Na2O2粉末至過量 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
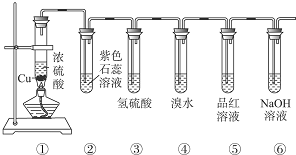
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
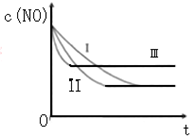 汽車尾氣中的主要污染物是NO和CO.為了減輕大氣污染,人們提出通過以下反應來處理汽車尾氣:
汽車尾氣中的主要污染物是NO和CO.為了減輕大氣污染,人們提出通過以下反應來處理汽車尾氣:| 時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
| C(CO)10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
| 實驗 編號 | T/°C | NO初始濃 度/10-3mol•L-1 | CO初始濃 度/10-3mol•L-1 | 催化劑的比 表面積/m2•g-1 |
| ① | 350 | 1.20 | 5.80 | 124 |
| ② | 280 | 1.20 | 5.80 | 124 |
| ③ | 280 | 1.20 | 5.80 | 82 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
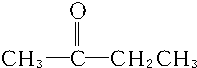 C:CH2═CH-CH2CH3或CH3CH═CH-CH3.
C:CH2═CH-CH2CH3或CH3CH═CH-CH3.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
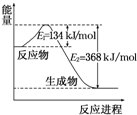 氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用.請回答下列問題:
氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用.請回答下列問題:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com