
【題目】如圖所示,水槽中試管內有一枚鐵釘,放置數天觀察:
(1)鐵釘在逐漸生繡。
(2)若試管內液面上升,發生___腐蝕,正極反應式:___。
(3)若試管內液面下降,正極反應式:___。
【答案】吸氧 O2+2H2O+4e-=4OH- 2H++2e-=H2↑
【解析】
(1)鐵在潮濕的空氣中易發生電化學腐蝕;
(2)中性條件下,鐵發生吸氧腐蝕,負極上鐵失電子,正極上氧氣得電子;
(3)酸性條件下,鐵發生析氫腐蝕,負極上鐵失電子,正極上氫離子得電子;
(1)鐵在潮濕的空氣中易發生電化學腐蝕,所以水槽中試管內有一枚鐵釘,鐵釘在逐漸生銹,則鐵釘的腐蝕屬于電化學腐蝕;
(2)若試管內液面上升,說明電解質環境是堿性或是中性,試管內氣體因和水反應而使其壓強減小,發生的是吸氧腐蝕,鐵作負極,負極上鐵失電子發生氧化反應,電極反應式為:Fe2e═Fe2+,正極上氧氣得電子發生還原反應,電極反應式為2H2O+O2+4e═4OH,
(3)若試管內液面下降,說明試管內氣體壓強增大,則鐵釘發生析氫腐蝕,酸性條件下、鐵釘發生析氫腐蝕,正極上氫離子得電子發生還原反應,電極反應式為2H++2e-=H2↑。


 學練快車道口算心算速算天天練系列答案
學練快車道口算心算速算天天練系列答案科目:高中化學 來源: 題型:
【題目】據報道,我國擁有完全自主產權的氫氧燃料電池車將在北京奧運會期間為運動員提供服務。某種氫氧燃料電池的電解液為KOH溶液,下列有關該電池的敘述不正確的是( )
A. 正極反應式為:O2+2H2O+4e-====4OH-
B. 工作一段時間后,電解液中KOH的物質的量不變
C. 該燃料電池的總反應方程式為:2H2+O2====2H2O
D. 用該電池電解CuCl2溶液,產生2.24 L Cl2(標準狀況)時,有0.1 mol電子轉移
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦酸鋇(BaTiO3)在工業上有重要用途,主要用于制作電子陶瓷、PTC熱敏電阻、電容器等多種電子元件。以下是生產鈦酸鋇的一種工藝流程圖:
![]()
已知:①草酸氧化鈦鋇晶體的化學式為BaTiO(C2O4)2·4H2O;
②25℃時,BaCO3的溶度積Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合價為:__________。
(2)用鹽酸酸浸時發生反應的離子方程式為: __________。
(3)流程中通過過濾得到草酸氧化鈦鋇晶體后,為提高產品質量需對晶體洗滌。
①過濾操作中使用的玻璃儀器有_____________________。
②如何證明晶體已洗凈?_______________________。
(4)TiO2具有很好的散射性,是一種有重要用途的金屬氧化物。工業上可用TiCl4水解來制備,制備時需加入大量的水,同時加熱,其目的是:_______________。
(5)某興趣小組取19.70gBaCO3模擬上述工藝流程制備BaTiO3,得產品13.98g,BaTiO3的產率為:________。
(6)流程中用鹽酸酸浸,其實質是BaCO3溶解平衡的移動。若浸出液中c(Ba2+)=0.1mol/L,則c(CO32-)在浸出液中的最大濃度為__________ mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】雙隔膜電解池的結構示意簡圖如圖所示,利用該裝置可以電解硫酸鈉溶液以制取硫酸和氫氧化鈉,并得到氫氣和氧氣。對該裝置及其原理判斷正確的是
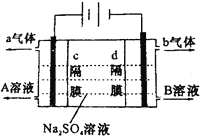
A.a氣體為氫氣,b氣體為氧氣
B.A溶液為氫氧化鈉,B溶液為硫酸
C.c隔膜為陽離子交換膜、d隔膜為陰離子交換膜
D.該電解反應的總方程式可以表示為:2Na2SO4+6H2O![]() 2H2SO4+4NaOH+O2↑+2H2↑
2H2SO4+4NaOH+O2↑+2H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列對化學平衡移動的分析中,不正確的是
①已達平衡的反應C(s)+H2O(g)![]() CO(g)+H2(g),當增加反應物物質的量時,平衡一定向正反應方向移動 ②已達平衡的反應N2(g)+3H2(g)
CO(g)+H2(g),當增加反應物物質的量時,平衡一定向正反應方向移動 ②已達平衡的反應N2(g)+3H2(g)![]() 2NH3(g),當增大N2的濃度時,平衡向正反應方向移動,N2的轉化率一定升高 ③有氣體參加的反應達到平衡時,若減小反應器容積時,平衡一定向氣體體積增大的方向移動 ④有氣體參加的反應達平衡時,在恒壓反應器中充入稀有氣體,平衡一定不移動
2NH3(g),當增大N2的濃度時,平衡向正反應方向移動,N2的轉化率一定升高 ③有氣體參加的反應達到平衡時,若減小反應器容積時,平衡一定向氣體體積增大的方向移動 ④有氣體參加的反應達平衡時,在恒壓反應器中充入稀有氣體,平衡一定不移動
A.①④B.①②③C.②③④D.①②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物M對霉菌有較好的抑制作用,結構簡式為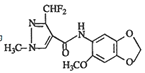 ,其合成路線如圖所示:
,其合成路線如圖所示:
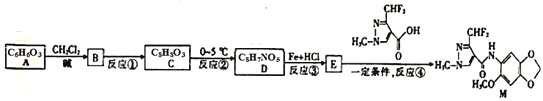
已知: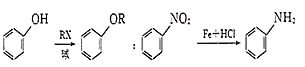
回答下列問題:
(1)化合物B的分子式為___;D中官能團的名稱為__。
(2)反應②的反應類型是__。
(3)化合物E的結構簡式為___。
(4)寫出A與足量溴水反應的化學方程式:__。
(5)寫出符合下列條件的D的同分異構體__(填結構簡式,寫出一種即可)。
①含有硝基和羰基,且分別和苯環直接相連;
②能與FeCl3溶液發生顯色反應;
③核磁共振氫譜顯示有3組峰,且峰面積之比為2:2:3。
(6)請以![]() 、
、![]() 為原料合成化合物
為原料合成化合物![]() ,寫出制備的合成路線流程圖。(無機試劑任用)__。
,寫出制備的合成路線流程圖。(無機試劑任用)__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在容積可變的容器中,反應2A(g)+B(g)![]() 2C(g)達到平衡時,A、B和C的物質的量分別為4mol,2mol和4mol。保持溫度和壓強不變,對平衡混合物中三者的物質的量做如下調整,可使平衡向左移動的是( )
2C(g)達到平衡時,A、B和C的物質的量分別為4mol,2mol和4mol。保持溫度和壓強不變,對平衡混合物中三者的物質的量做如下調整,可使平衡向左移動的是( )
A.均減半B.均加半C.均增加1molD.均減少1mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2L密閉容器中充有2molSO2和一定量的O2,發生反應2SO2(g)+O2(g)![]() 2SO3(g)。當反應進行到4min時,測得此時SO2為0.4mol,則2min時密閉容器中SO3的物質的量為( )
2SO3(g)。當反應進行到4min時,測得此時SO2為0.4mol,則2min時密閉容器中SO3的物質的量為( )
A.1.6molB.1.2molC.大于1.6molD.小于1.2mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦酸鋇被譽為“電子陶瓷工業的支柱”。工業制取方法如圖,先獲得不溶性草酸氧鈦鋇晶體[BaTiO(C2O4)24H2O],煅燒后可獲得鈦酸鋇粉體。
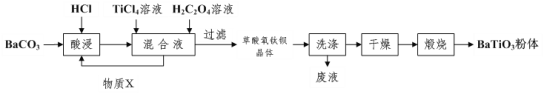
(1)酸浸時發生的反應的離子方程式為___。
(2)配制TiCl4溶液時通常將TiCl4固體溶于濃鹽酸再加水稀釋,其目的是___。
(3)加入H2C2O4溶液時,發生反應的化學方程式為___。可循環使用的物質X是___(填化學式),設計實驗方案驗證草酸氧鈦鋇晶體是否洗滌干凈:___。
(4)煅燒草酸氧鈦鋇晶體得到BaTiO3的同時,生成高溫下的氣態產物有CO、___。
(5)工業上用飽和Na2CO3溶液處理重晶石(主要成分是BaSO4),待達到平衡后,移走上層清液,重復多次操作,將其轉化為易溶于酸的BaCO3,再由BaCO3制備其它鋇鹽。已知常溫下:Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.59×10-9,請問至少需要___molL-1的碳酸鈉溶液浸泡才能實現上述轉化(忽略CO32-的水解)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com