
己知C8H11N的同分異構體中含有苯環的有很多種(不考慮立體異構),其中苯環上有一個側鏈、二個側鏈和三個側鏈的種數分別是
A.5、9、6 B.4、6、6 C.3、9、7 D.4、6、7
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2017屆湖北省老河口市高三10月月考化學卷(解析版) 題型:選擇題
將 4 mol A 氣體和 2 mol B 氣體在 2 L 的容器中混合并在一定條件下發生如下反應:2A(氣) + B(氣)  2C(氣)若經 2 s(秒)后測得 C 的濃度為 0.6 mol·L-1 ,現有下列幾種說法:① 用物質 A 表示的反應的平均速率為 0.3 mol·L-1·s-1 ② 用物質 B 表示的反應的平均速率為 0.6 mol·L-1·s-1 ③2 s 時物質 B 的濃度為 0.7 mol·L-1 ④2 s 時物質 A 的轉化率為70% 其中正確的是( )
2C(氣)若經 2 s(秒)后測得 C 的濃度為 0.6 mol·L-1 ,現有下列幾種說法:① 用物質 A 表示的反應的平均速率為 0.3 mol·L-1·s-1 ② 用物質 B 表示的反應的平均速率為 0.6 mol·L-1·s-1 ③2 s 時物質 B 的濃度為 0.7 mol·L-1 ④2 s 時物質 A 的轉化率為70% 其中正確的是( )
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化學 來源:2017屆福建省高三上聯考一化學卷(解析版) 題型:填空題
氯化鍶晶體在工業上常用作鋁的緩蝕劑。工業上一般用難溶于水的的碳酸鍶(SrCO3)為原料(含少量鋇和鐵的化合物等),制備高純六水氯化鍶晶體(SrCl2•6H2O)的過程為:

已知:Ⅰ.SrCl2•6H2O晶體在61℃時開始失去結晶水,100℃時失去全部結晶水;
Ⅱ.有關氫氧化物開始沉淀和完全沉淀的pH如下表:
氫氧化物 | Fe(OH)3 | Fe(OH)2 |
開始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
(1)操作①在 實際工業生產中常常把碳酸鍶粉碎并加以攪拌,其目的是 。碳酸鍶與鹽酸反應的化學方程式為__________________。
實際工業生產中常常把碳酸鍶粉碎并加以攪拌,其目的是 。碳酸鍶與鹽酸反應的化學方程式為__________________。
(2)操作②在 酸性條件下,加入30% H2O2溶液的目的是: 。
酸性條件下,加入30% H2O2溶液的目的是: 。
(3)操作③將溶液的pH值由1調節至 (填選項);所得濾渣的主要成分是 (填化學 式)。
式)。
A.1.5 B.4 C.7 D.9.7
(4)工業上用50~60℃熱風吹干六水氯化鍶,選擇該溫度的原因是 。
(5)操作⑥中,洗滌氯化鍶晶體最好選用___________。
A.水 B.稀硫酸 C.氫氧化鈉溶液 D.氯化鍶飽和溶液
(6)若濾液中Ba2+ 濃度為1×10-5mol/L,則濾液中Sr2+物質的量濃度不大于 mol/L。
(已知:Ksp[SrSO4]=3.3×10-7,Ksp[BaSO4]=1.1×10-10)
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省六校教育研究會高三上第一次聯考化學卷(解析版) 題型:填空題
某工廠用回收釩渣(含VOSO4、K2SO4、SiO2))制取V2O5時工藝流程如下:
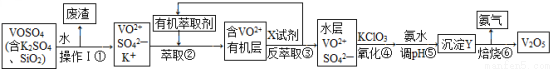
請回答下列問題:
(1)操作I的名稱 ,①中產生廢渣的主要成分是 。
(2)己知:VOSO4(水層)+2HA(有機層) VOA2(有機層)+H2SO4(水層)。步驟②中必須加入適量堿,其原因是 ;步驟③中反萃取所用的試劑X為 。
VOA2(有機層)+H2SO4(水層)。步驟②中必須加入適量堿,其原因是 ;步驟③中反萃取所用的試劑X為 。
(3)步驟④中的反應的離子方程式:□ClO3—+□VO2++□H+=□VO3++□ +□
(4)沉淀Y的摩爾質量為598g·mol—1,且僅含有四種元素。取59.8g沉淀Y的樣品充分焙燒,得到產品54.6g,將產生的氣體通過足量堿石灰,堿石灰增重1.8g,剩余的氣體再通入稀硫酸被完全吸收。通過計算確定沉淀Y的化學式為 。
(5)釩沉淀率和溶液pH之間關系如下
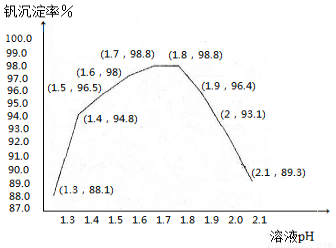
⑤中加入氨水,調節溶液的最佳pH為 ;若釩沉淀率為93.1%時不產生Fe(OH)3沉淀,則溶液中c(Fe3+)< 。(己知:25℃時,Ksp[Fe(OH)3]=2.6×l0—39)
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省六校教育研究會高三上第一次聯考化學卷(解析版) 題型:選擇題
N2O5是一種新型硝化劑,在一定溫度下可發生如下反應:2N2O5(g) 4NO2(g)+O2(g) △H>0。T1溫度時,向密閉容器中通入N2O5氣體,部分實驗數據見下表:
4NO2(g)+O2(g) △H>0。T1溫度時,向密閉容器中通入N2O5氣體,部分實驗數據見下表:
時間/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol·L—1) | 5.00 | 3.52 | 2.50 | 2.50 |
下列說法正確的是
A.500s內O2的平均生成速率為7.4×l0—4mol·L—1·s—1
B.T1溫度下該反應達到平衡時,平衡混合物中NO2的體積分數為50%
C.達到平衡后,其他條件不變,將容器體積壓縮到原來的1/2,則c(N2O5)>5.00mol·L—1
D.T1溫度下的平衡常數為K1,T2溫度下的平衡常數為K2,若K1<K2,則T1>T2
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省六校教育研究會高三上第一次聯考化學卷(解析版) 題型:選擇題
電解質在溶液中的行為是化學研究的重要內容。下列有關溶液的敘述不正確的是
A.加熱蒸干NaCl、MgCl2溶液時可以得到晶體NaCl、MgCl2
B.相同條件下,等物質的量濃度的溶液導電能力:HC1>NH3·H2O
C.溶液中離子結合質子(氫離子)的能力:C2O42—>HC2O4—>SO42—
D.海洋封存CO2會導致局部海洋水體酸性增強,會破壞海洋生態環境
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省江淮十校高三11月質檢化學試卷(解析版) 題型:實驗題
班級化學興趣小組做如下實驗,請你回答相關問題:


Ⅰ、甲組做單質鈉在空氣中燃燒實驗。問:實驗室如何取用單質鈉。單質鈉燃燒時會生成黑色固體,黑色固體可能來源是 、 、 。
某同學想用金屬鈉和空氣制備純度較高的Na2O2(不考慮空氣中N2),可利用的裝置如下。回答下列問題:

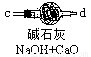
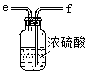
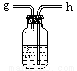
Ⅰ Ⅱ Ⅲ Ⅳ
(1)裝置Ⅳ中盛放的藥品是 ,若沒有該裝置可能導致生成的Na2O2中含有 ,其反應方程式為 。
(2)若規定氣體的氣流方向從左到右,各儀器接口的標號字母(a、b……)順序是:空氣進入 , 接 , 接 , 接 。
(3)裝置的Ⅱ作用是 。
Ⅱ、乙組用如圖所示的實驗裝置(夾持儀器略);并用其進行下述實驗: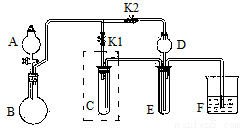
實驗Ⅰ:制取并收集NH3。
(1)制取并收集NH3,A中盛放 ,旋塞K1應該 (填“打開”或“關閉”),旋塞K2應該 (填“打開”或“關閉”)。
實驗2:用干、濕兩個有色布條驗證干燥Cl2無漂白性而潮濕的Cl2具有漂白性。
(2)用高錳酸鉀與濃鹽酸反應制取Cl2,實驗前先將裝置C改用如圖所示裝置,并應在D中加入 (填代號)。
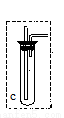
a.濃硫酸 b.無水氯化鈣 c.堿石灰 d.碳酸氫鈉
(3)潤濕的有色布條應放在 (填表示儀器的英文字母)中,干燥的有色布條應放在 (填表示儀器的英文字母)中。
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省江淮十校高三11月質檢化學試卷(解析版) 題型:選擇題
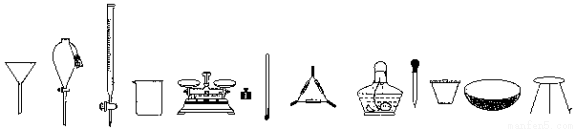
a b c d e f g h I j k l
A. 含砂粒的食鹽水過濾,選用a、d、f、l
B. 萃取水中碘,選用b、c、d、f
C. 將膽礬轉化為CuSO4固體,選用g、h、j、l
D. 檢驗濾液中的Fe3+,選用d、f、h、i
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省高二上期中化學卷(解析版) 題型:選擇題
25 ℃時,Ksp[Mg(OH)2] = 5.61×10-12,Ksp(MgF2)= 7.42×10-11。下列說法正確的是( )
A.25 ℃時,飽和Mg(OH)2溶液與飽和MgF2溶液相比,前者的c(Mg2+)大
B. 25 ℃時,Mg(OH)2固體在20 mL 0.01 mol/L氨水中的 Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小
Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小
C.25 ℃時,在Mg(OH)2的懸濁液加入少量的NH4Cl固體,c(Mg2+)增大
D.25 ℃時,在Mg(OH)2的懸濁液加入NaF溶液后,Mg(OH)2不可能轉化成為MgF2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com