
【題目】北京市場銷售的某種食用精制鹽包裝袋上有如下說明:
產品標準 | GB5461 |
產品等級 | 一級 |
配 料 | 食鹽、碘酸鉀、抗結劑 |
碘含量(以I計) | 20~50mg/kg |
分裝時期 | |
分裝企業 |
(1)碘酸鉀與碘化鉀在酸性條件下發生如下反應,配平化學方程式(將化學計量數填于空白處)
____KIO3+___KI+___H2SO4=___K2SO4+___I2+___H2O
(2)上述反應生成的I2可用四氯化碳檢驗。向碘的四氯化碳溶液中加入Na2SO3稀溶液,將I2還原,以回收四氯化碳。
①Na2SO3稀溶液與I2反應的離子方程式是_________________________________。
②某學生設計回收四氯化碳的操作步驟為:
a.將碘的四氯化碳溶液置于分液漏斗中;
b.加入適量Na2SO3稀溶液;
c.分離出下層液體。
以上設計中遺漏的操作及在上述步驟中的位置是______________________。
(3)已知:I2+2S2O32-=2I-+S4O62-。某學生測定食用精制鹽的碘含量,其步驟為:
a. 準確稱取wg食鹽,加適量蒸餾水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3與KI反應完全;
c.以淀粉為指示劑,逐滴加入物質的量濃度為2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反應完全。
①判斷c中反應恰好完全依據的現象是______________________。
②b中反應所產生的I2的物質的量是___________mol。
③根據以上實驗和包裝袋說明,所測精制鹽的碘含量是(以含w的代數式表示)
_______________________mg/kg。
【答案】1 5 3 3 3 3 I2+SO32-+H2O![]() 2I-+SO42-+2H+ 在步驟b后,增加操作:將分液漏斗充分振蕩后靜置 溶液由藍色恰好變為無色 1.0×10-5 4.2 ×102/w
2I-+SO42-+2H+ 在步驟b后,增加操作:將分液漏斗充分振蕩后靜置 溶液由藍色恰好變為無色 1.0×10-5 4.2 ×102/w
【解析】
(1)該反應中,KIO3中I元素化合價由+5價變為0價、KI中I元素化合價由-1價變為0價,根據轉移電子相等配平方程式;
(2)①I2具有氧化性,能將SO32-氧化為SO42-,自身被還原為I-;
②如果不振蕩,二者反應不充分;
(3)①二者恰好反應時,溶液由藍色恰好變為無色;
②根據I2+2S2O32-=2I-+S4O62-中碘和硫代硫酸鈉之間的關系式計算但的物質的量;
③根據碘和食鹽質量之比進行計算。
(1)該反應中,KIO3中I元素化合價由+5價變為0價、KI中I元素化合價由-1價變為0價,轉移電子總數為5,再結合原子守恒配平方程式為KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,故答案為:1;5;3;3;3;3;
(2)①I2具有氧化性,能將SO32-氧化為SO42-,自身被還原為I-,離子方程式為I2+SO32-+H2O=2I-+SO42-+2H+,故答案為:I2+SO32-+H2O=2I-+SO42-+2H+;
②如果不振蕩,二者反應不充分,所以在步驟b后,增加操作:將分液漏斗充分振蕩后靜置,故答案為:在步驟b后,增加操作:將分液漏斗充分振蕩后靜置;
(3)①碘遇淀粉試液變藍色,如果碘完全反應,則溶液會由藍色轉化為無色,所以當溶液由藍色轉化為無色時說明反應完全,故答案為:溶液由藍色恰好變為無色;
②設碘的物質的量為x,
I2+2S2O32-=2I-+S4O62-
1mol 2mol
x 1.00×10-3molL-1×0.024L
1mol:2mol=x:(1.00×10-3molL-1×0.024L)
x=![]()
=1.2×10-5mol,
故答案為:1.2×10-5;
③根據KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O得![]() n(I2)=(KIO3)=4×10-6mol,碘酸鉀中碘的質量=4×10-6mol×127g/mol=0.508mg,
n(I2)=(KIO3)=4×10-6mol,碘酸鉀中碘的質量=4×10-6mol×127g/mol=0.508mg,
設每kg食鹽中碘的質量為y,
則y:1000g=0.508mg:wg,
y=![]() =
=![]() mg或
mg或![]() mg。
mg。


 暑假作業海燕出版社系列答案
暑假作業海燕出版社系列答案科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 恒容密閉容器中進行的反應:A(s)+3B(g)![]() 2C(g)+D(g),如果氣體密度保持不變,說明反應已經達到平衡
2C(g)+D(g),如果氣體密度保持不變,說明反應已經達到平衡
B. C ( s) + H2O (g) ![]() CO ( g) + H2 (g),其他條件不變,縮小容器體積,正速率減小,逆速率增大
CO ( g) + H2 (g),其他條件不變,縮小容器體積,正速率減小,逆速率增大
C. N2(g) + 3H2(g)![]() 2NH3(g) △H=—93kJ·mol—1,往恒容密閉容器中充入0.4 molN2(g)和2 mol H2(g)達到平衡時,可以放出37.2 kJ的熱量
2NH3(g) △H=—93kJ·mol—1,往恒容密閉容器中充入0.4 molN2(g)和2 mol H2(g)達到平衡時,可以放出37.2 kJ的熱量
D. A(g)+ 3B (g) ![]() 2C (g) + D (g),在兩種不同情況下的反應速率分別為:①
2C (g) + D (g),在兩種不同情況下的反應速率分別為:①![]() ,②
,②![]() ,則前者比后者快
,則前者比后者快
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在2 L密閉容器中,A、B、C三種氣體的物質的量隨時間變化的曲線如圖所示。下列說法正確的是
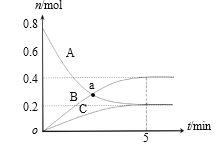
A.a點時,υ(A) =υ(B)
B.反應開始到5min,B的物質的量增加了0.2 mol
C.反應的化學方程式為:3A![]() 2B+C
2B+C
D.反應開始到5min,υ(C) =0.04 mol/(L·min)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學院科研團隊研究表明,在常溫常壓和可見光下,基于![]() (一種固體催化劑)合成
(一種固體催化劑)合成![]() 的原理示意圖如下。試回答下列問題:
的原理示意圖如下。試回答下列問題:
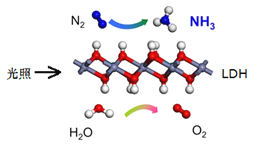
(1)從能量轉換的角度,該過程將______轉化成為__________;
(2)該反應的化學方程式為:________________,氧化劑與還原劑的物質的量之比為__________;
(3)關于該反應的說法,正確的是_______
A.催化劑能增大化學反應速率,縮短反應時間,從而提高產氨效率
B.該反應過程中涉及極性鍵和非極性鍵的斷裂和形成
C.可以通過分離液態空氣的方法獲得氮氣
D.基于![]() 合成
合成![]() 的過程屬于人工固氮
的過程屬于人工固氮
(4)現代工業常以氯化鈉、二氧化碳和氨氣為原料制備純堿。加入原料的順序是:在氯化鈉溶液,通入_________至飽和,再通入足量的_________可制得![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】R、W、X、Y、M是原子序數依次增大的五種主族元素。R最常見同位素的原子核中不含中子。W與X可形成兩種穩定的化合物:WX和WX2。工業革命以來,人類使用的化石燃料在燃燒過程中將大量WX2排入大氣,在一定程度導致地球表面平均溫度升高。Y與X是同一主族的元素,且在元素周期表中與X相鄰。
(1)W的原子結構示意圖是__________________________。
(2)WX2的電子式是_______________________。
(3)R2X、R2Y中,穩定性較高的是____(填化學式),請從原子結構的角度解釋其原因:_____。
(4)Se與Y是同一主族的元素,且在元素周期表中與Y相鄰。
①根據元素周期律,下列推斷正確的是________(填字母序號)。
a.Se的最高正化合價為+7價
b.H2Se的還原性比H2Y強
c.H2SeO3的酸性比H2YO4強
d.SeO2在一定條件下可與NaOH溶液反應
②室溫下向SeO2固體表面吹入NH3,可得到兩種單質和H2O,該反應的化學方程式為_____________。
(5)科研人員從礦石中分離出一種氧化物,化學式可表示為M2O3。為確定M元素的種類,進行了一系列實驗,結果如下:
①M的相對原子質量介于K和Rb(銣)之間;
②0.01 mol M2O3在堿性溶液中與Zn充分反應可得到M的簡單氫化物,反應完全時,被M2O3氧化的Zn為0.06 mol;
綜合以上信息推斷,M可能位于元素周期表第_________________族。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室備有質量分數為98%,密度為1.84 g·cm-3的硫酸,據此下列說法錯誤的是 ( )
A. 該硫酸的物質的量濃度為18.4 mol·L-1
B. 該硫酸50 mL與足量的銅反應可得到標準狀況下SO2 0.46 mol
C. 某同學用該硫酸配制稀硫酸時,未洗滌燒杯和玻璃棒,會造成最終配制的稀硫酸濃度偏低
D. 等質量的水與該硫酸混合所得溶液的物質的量濃度小于9.2 mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素Q、R、T、W在元素周期表中的位置如圖所示,其中T所處的周期序數與主族序數相等,下列敘述錯誤的是
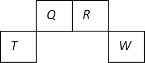
A. T的氧化物能與堿反應
B. 元素的非金屬性:Q強于W
C. W的單質共熱時,能與其最高價氧化物的水化物濃溶液反應
D. 原子序數比R多1的元素的一種氫化物能分解為它的另一種氫化物
查看答案和解析>>
科目:高中化學 來源: 題型:
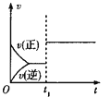
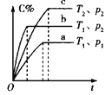
【題目】下列對圖像的敘述正確的是
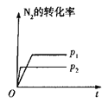

甲 乙 丙 丁
A.圖甲可表示壓強對反應:![]()
![]() 的影響
的影響
B.圖乙中,![]() 時刻改變的條件一定是加入了催化劑
時刻改變的條件一定是加入了催化劑
C.若圖丙表示反應:![]() ,則
,則![]() 、
、![]()
D.圖丁表示水中![]() 和
和![]() 的關系,ABC所在區域總有
的關系,ABC所在區域總有![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究減少CO2排放是一項重要課題。CO2經催化加氫可以生成低碳有機物,主要有以下反應:
反應Ⅰ:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol
反應Ⅱ:CH3OCH3(g)+H2O(g) ![]() 2CH3OH(g) △H2=+23.4 kJ/mol
2CH3OH(g) △H2=+23.4 kJ/mol
反應Ⅲ:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3
(1)△H3=________kJ/mol。
(2)恒溫恒容條件下,在密閉容器中通入等物質的量的CO2和H2,發生反應I。下列描述能說明反應I達到平衡狀態的是_______(填序號)。
A.反應體系總壓強保持不變
B.容器內的混合氣體的密度保持不變
C.水分子中斷裂2NA個H-O鍵,同時氫分子中斷裂3NA個H-H鍵
D.CH3OH和H2O的濃度之比保持不變
(3)反應II在某溫度下的平衡常數為0.25,此溫度下,在密閉容器中加入等物質的量的CH3OCH3(g)和H2O(g),反應到某時刻測得各組分濃度如下:
物質 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
濃度/mol·L-1 | 1.8 | 1.8 | 0.4 |
此時v正___v逆(填“>”、“<”或“=”),當反應達到平衡狀態時,混合氣體中CH3OH體積分數(CH3OH)% =___%。
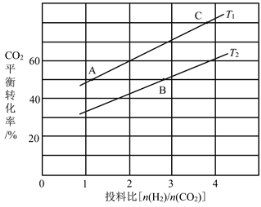
(4)在某壓強下,反應III在不同溫度、不同投料比時,CO2的平衡轉化率如圖所示。T1溫度下,將6mol CO2和12mol H2充入2 L的密閉容器中,5min后反應達到平衡狀態,則0~5min內的平均反應速率v(CH3OCH3)=____;KA、KB、KC三者之間的大小關系為____。
(5)恒壓下將CO2和H2按體積比1:3混合,在不同催化劑作用下發生反應I和反應III,在相同的時間段內CH3OH的選擇性和產率隨溫度的變化如圖。其中:CH3OH的選擇性=![]() ×100%
×100%

在上述條件下合成甲醇的工業條件是____。
A.210℃ B.230℃ C.催化劑CZT D.催化劑CZ(Zr-1)T
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com