

分析 (1)泡騰片成份中有檸檬酸和碳酸氫鈉,兩者反應生成二氧化碳氣體,所以有大量氣泡產生;
(2)配成100mL溶液,需用100ml的容量瓶;
(3)因為精確度達0.01ml,所以步驟2中準確量取出10.00mL酸性溶液用移液管或者酸性滴定管;滴定管刻度值從上到下刻度逐漸增大,滴定前液面處的讀數是V1ml,滴定后液面處的讀數是V2ml,消耗溶液的體積為(V2-V1)mL,而V1=2.4ml,而V2=27.4ml,所以消耗溶液的體積為27.4ml-2.4ml=25ml,根據關系式C6H8O6+I2═C6H6O6+2HI,計算維生素C的質量;
(4)應根據維生素C(C6H8O6)具有強還原性,可能極易被空氣中的氧氣氧化,還可能與碘水發生氧化還原反應.
解答 解:(1)泡騰片成份中有檸檬酸和碳酸氫鈉,兩者反應生成二氧化碳氣體,所以有大量氣泡產生,故答案為:檸檬酸與碳酸氫鈉反應產生CO2;
(2)配成100mL溶液,需用100ml的容量瓶,故答案為:100 ml容量瓶;
(3)步驟2中準確量取出10.00mL酸性溶液用移液管或者酸性滴定管,滴定管刻度值從上到下刻度逐漸增大,滴定前液面處的讀數是V1ml,滴定后液面處的讀數是V2ml,消耗溶液的體積為(V2-V1)mL,而V1=2.4ml,而V2=27.4ml,所以消耗溶液的體積為27.4ml-2.4ml=25ml,
根據關系式C6H8O6+I2═C6H6O6+2HI,
維生素C的質量25ml×2.00×10-3mol•L-1×10-3L/mL×180g/mol═5×10-5mol×180g/mol=9mg,所以每片維C泡騰片中含維生素C:9mg×$\frac{10mL}{50mL}$=1.8mg,
故答案為:移液管或酸式滴定管;25;1.8;
(4)應根據維生素C(C6H8O6)具有強還原性,可能極易被空氣中的氧氣氧化,還可能與碘水發生氧化還原反應,所以問題2維生素C被空氣中的氧氣氧化,問題1,請設計實驗方案向葡萄糖與少量碘水的混合體系中加入淀粉,觀察溶液是否變藍,
故答案為:維生素C被空氣中的氧氣氧化;向葡萄糖與少量碘水的混合體系中加入淀粉,觀察溶液是否變藍.
點評 本題為實驗習題,考查物質性質的實驗探究方法和實驗設計和分析判斷,滴定實驗分析、計算應用,實驗數據的分析判斷和目的分析,綜合性較強,有一定的難度.


 同步輕松練習系列答案
同步輕松練習系列答案 課課通課程標準思維方法與能力訓練系列答案
課課通課程標準思維方法與能力訓練系列答案科目:高中化學 來源: 題型:填空題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 開始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 解釋或實驗結論 |
| (1)取9.0g有機物A加熱使其氣化,測得其密度是相同條件下H2的45倍 | (1)由此可知A的相對分子質量為90. |
| (2)將9.0gA在足量O2中充分燃燒,其產物依次緩緩通過濃硫酸、堿石灰,兩者分別增重5.4g和13.2g. | (2)由此可知A的分子式為C3H6O3. |
| (3)另取A9.0g,跟足量的NaHCO3粉末反應,生成CO2氣體2.24L;9.0gA若與足量金屬鈉反應生成H2也是2.24L(氣體體積皆為標準狀況下測得). | (3)由此可知A中含有官能團有.(填結構簡式)-COOH、-OH |
(4)A的核磁共振氫譜如下圖: | (4)由此可知A中含有4種不同性質的氫原子 (5)綜上,A的結構簡式為  . . |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
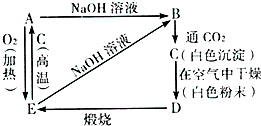 根據如圖反應及其變化,回答有關問題.
根據如圖反應及其變化,回答有關問題.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com