
SiO2、SO2和CO2都是酸性氧化物,它們的化學性質具有一定的相似性;Mg和Na的化學性質也具有一定相似性。
某興趣小組用如圖所示裝置進行Mg與SO2反應的實驗。

(1)選擇制取SO2的合適試劑________(填編號)。
①濃HCl ②濃H2SO4 ③Na2SO3固體 ④CaSO3固體
(2)上述裝置還可優化,優化的方法是________________________________________,裝置C中NaOH溶液的作用是___________________________________________________________
(3)甲同學推測Mg與SO2的反應和Mg與CO2的反應相似,則該反應方程式為_________________________________________;
乙同學的推測是:2Mg+3SO2 2MgSO3+S;丙同學的推測是:3Mg+SO2
2MgSO3+S;丙同學的推測是:3Mg+SO2 2MgO+MgS,要驗證甲、乙、丙三位同學的推測是否正確,丁同學作如下實驗探究:
2MgO+MgS,要驗證甲、乙、丙三位同學的推測是否正確,丁同學作如下實驗探究:
已知:MgSO3和MgS都微溶于水,能與鹽酸發生復分解反應放出氣體;H2S氣體通入CuSO4溶液中出現黑色沉淀。
限選試劑:2 mol·L-1鹽酸、2 mol·L-1硝酸、蒸餾水、2 mol·L-1 NaOH溶液、品紅溶液、澄清石灰水、2 mol·L-1 CuSO4溶液;儀器和用品自選。
序號 | 實驗步驟 | 預期現象和結論 |
① | 取少量反應后所得固體于試管中 |
|
② | 向試管中的固體慢慢滴加____________,試管口塞上帶導管的單孔塞,并將導管通入盛有________的試管中 | 若試管中的________,則丙同學推測正確,若試管中的固體未完全溶解,且________,則乙同學推測正確 |
根據上述實驗探究,能證明甲同學推測正確的操作和預期現象是
_____________________________________________________________。
(4)上述實驗需要100 mL 2 mol·L-1的鹽酸,配制時選用________(選填10 mL、25 mL、50 mL或100 mL)量筒量取36.5%密度為1.19 g·mL-1的濃鹽酸的體積為________mL。
 金牌課堂練系列答案
金牌課堂練系列答案 三新快車金牌周周練系列答案
三新快車金牌周周練系列答案科目:高中化學 來源:2013-2014學年高考化學二輪復習 專題2常用化學計量--物質的量練習卷(解析版) 題型:選擇題
一定體積的溶質質量分數為14%的氫氧化鉀溶液,若將其蒸發掉50 g水后,其溶質的質量分數恰好增大1倍,溶液體積變為62.5 mL。則濃縮后溶液的物質的量濃度為( )。
A.2.2 mol·L-1 B.4 mol·L-1C.5 mol·L-1 D.6.25 mol·L-1
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習 專題12化學實驗基礎練習卷(解析版) 題型:選擇題
下列敘述中不正確的是( )。
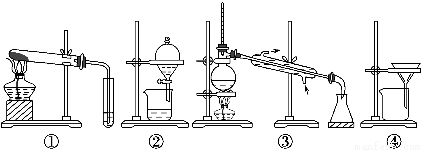
A.可用裝置①除去碳酸鈉中的碳酸氫鈉
B.可用裝置②分離汽油和水的混合物
C.可用裝置③從海水中蒸餾得到淡水
D.可用裝置④把膠體粒子從分散系中分離出來
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習 專題11有機化學基礎練習卷(解析版) 題型:填空題
鈀(Pd)催化偶聯反應是近年來有機合成的研究熱點之一。例如:

化合物Ⅰ可由以下合成路線獲得:

(1)化合物Ⅰ與Br2發生加成反應所得產物的結構簡式為______________。
(2)化合物Ⅱ的分子式為________。
(3)化合物Ⅲ與化合物Ⅱ在酸催化下發生酯化反應的化學方程式為_____________________________________________________ (注明條件)。
(4)化合物Ⅳ的結構簡式為______________。
(5)Ⅴ是化合物Ⅱ的同分異構體。Ⅴ的分子中苯環上有三個取代基,能發生銀鏡反應,且苯環上的一氯代物有2種。Ⅴ的結構簡式可能是______________。
(6)1分子 與1分子
與1分子 在一定條件下可發生類似反應①的反應,生成有機化合物Ⅵ,Ⅵ的結構簡式為________________。
在一定條件下可發生類似反應①的反應,生成有機化合物Ⅵ,Ⅵ的結構簡式為________________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習 專題11有機化學基礎練習卷(解析版) 題型:選擇題
下列說法正確的是( )。
A.乙烯和聚乙烯都可與溴水發生加成反應
B.用酸性KMnO4溶液能鑒別乙烷和乙烯
C.(NH4)2SO4、CuSO4都能使蛋白質變性
D.葡萄糖、蔗糖都能與新制的Cu(OH)2反應
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習 專題10常見非金屬元素及其重要化合物練習卷(解析版) 題型:選擇題
下列化學實驗事實及其結論都正確的是( )。
選項實驗事實結論
A將SO2通入含HClO的溶液中生成H2SO4HClO的酸性比H2SO4強
B鋁箔在酒精燈火焰上加熱熔化但不滴落鋁箔表面氧化鋁熔點高于鋁
CSiO2可以和NaOH溶液及HF溶液反應SiO2屬于兩性氧化性
D將SO2通入溴水中,溴水褪色SO2具有漂白性
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪沖刺非選擇題增分專練 綜合實驗設計練習卷(解析版) 題型:實驗題
某小組取一定質量的FeSO4固體,利用下圖裝置進行實驗。

實驗 | 實驗過程 | 實現現象 |
① | 通入一段時間N2,加熱 | A中固體變為紅棕色,B中有白色沉淀,D試管中有無色液體 |
② | 用帶有火星的木條靠近裝置D的導管口 | 木條復燃 |
③ | 充分反應,停止加熱,冷卻后,取A中固體,加鹽酸 | 固體溶解,溶液呈黃色 |
④ | 將③所得溶液滴入D試管中 | 溶液變為淺綠色 |
已知:SO2熔點-72℃,沸點-10℃;SO3熔點16.8℃,沸點44.8 ℃。
(1)實驗③反應的離子方程式是_____________________________________________。
(2)分解過程除產生使木條復燃的氣體外,僅由A中固體顏色變化推測,還一定有________氣體,依據是____________________________________________________
(3)實驗④反應的離子方程式是_____________________________________________。
(4)某同學依據B中的現象,認為FeSO4分解一定有SO3生成。你認為是否正確,并說明原因:____________________________________________(用必要的文字和化學方程式解釋)。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪沖刺非選擇題增分專練 基本概念、基本理論練習卷(解析版) 題型:填空題
為了提高資源利用率,減少環境污染,化工集團將鈦廠、氯堿廠和甲醇廠組成產業鏈,如圖所示。
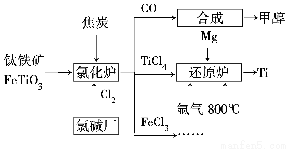
請填寫下列空白。
(1)鈦鐵礦進入氯化爐前通常采取洗滌、粉碎、烘干、預熱等物理方法處理,請從原理上解釋粉碎的作用:_______________________________________
已知氯化爐中氯氣和焦炭的理論用料物質的量之比為7∶6,則氯化爐中還原劑的化學式是___________________________。
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s)ΔH=-641 kJ/mol
②2Mg(s)+TiCl4(s)= 2MgCl(s)+Ti(s)ΔH=-512 kJ/mol
則Ti(s)+2Cl2(g)=TiCl4(s) ΔH=________。
(3)氬氣通入還原爐中并不參與反應,通入氬氣的作用是___________________________
(4)以甲醇、空氣、氫氧化鉀溶液為原料,石墨為電極可構成燃料電池。已知該燃料電池的總反應式為2CH3OH+3O2+4OH-=2CO32—+6H2O,該電池中正極上的電極反應式為_________________________________________。
工作一段時間后,測得溶液的pH________(填“減小”、“增大”或“不變”)。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪專題復習 離子反應、氧化還原反應練習卷(解析版) 題型:實驗題
某小組查文獻得知:氧化性I >Fe3+>I2,3Br2+6FeCl2
>Fe3+>I2,3Br2+6FeCl2 2FeBr3+4FeCl3;I2+2S2
2FeBr3+4FeCl3;I2+2S2
 S4
S4 +2I-;CuI是一種白色沉淀(Ksp=1.3×1
+2I-;CuI是一種白色沉淀(Ksp=1.3×1 )。
)。
Ⅰ.該小組為確定一份加碘鹽(可能含有KIO3、KI、Mg2+、Fe3+)的成分,設計定性實驗加以猜想和驗證。
(1)實驗過程如下:
實驗步驟 | 實驗過程和現象 | 對應結論 | |
步驟1 | 取一定量碘鹽,用適量蒸餾水溶解,并加稀鹽酸酸化,將所得試液分為3份 |
_____________ | |
步 驟 2 | 第①份 試液 |
| 碘鹽中肯定含 |
第②份 試液 |
|
_____________ | |
第③份 試液 |
| X為 (填化學式) | |
(2)該碘鹽中肯定不含的物質是 (用化學式或離子符號表達)。
(3)根據信息推斷Fe3+、S4 、I2、Br2的氧化性由強到弱的順序是 。
、I2、Br2的氧化性由強到弱的順序是 。
(4)第③份試液中加入足量KI固體后,反應的離子方程式為 、 。
Ⅱ.用“間接碘量法”測定含有CuCl2·2H2O晶體的試樣(不含能與I-發生反應的氧化性雜質)的純度,過程如下:
取0.40 g試樣溶于水,加入過量KI固體,充分反應,生成白色沉淀。加入淀粉作滴定指示劑,用0.100 0 mol·L-1 Na2S2O3標準溶液滴定,到達滴定終點時,消耗Na2S2O3標準溶液20.00 mL。
(1)滴定終點的現象是 。
(2)CuCl2溶液與KI反應的化學方程式為 。
(3)該試樣中CuCl2·2H2O的質量分數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com