
【題目】(1)下列變化中①NaCl 溶于水 ②HCl 溶于水 ③ 葡萄糖溶于水
④Na2O2溶于水 ⑤ I2升華 ⑥固體NaOH熔化。
未發生化學鍵破壞的是_____,僅發生離子鍵破壞的是________,僅發生共價鍵破壞的是_______,既發生離子鍵破壞,又發生共價鍵破壞的是____________(填序號)。
(2)對于下列物質:(填序號)
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤ ⑥
⑥![]()
⑦ ⑧一氯甲烷 ⑨ CCl4 ⑩ CH3-CH2-CH2-Cl
⑧一氯甲烷 ⑨ CCl4 ⑩ CH3-CH2-CH2-Cl
屬于同一物質的是___________________;
互為同位素的是______________________;
互為同分異構體的是_____________________;
互為同系物的是⑩和______________________;
【答案】 ③、⑤ ①、⑥ ② ④ ④、④ ①、⑥ ⑦、⑩ ⑧
【解析】(1)①NaCl溶于水電離出鈉離子和氯離子,破壞離子鍵;②HCl溶于水電離出氫離子和氯離子,破壞共價鍵;③葡萄糖溶于水破壞分子間作用力,化學鍵不變;④Na2O2溶于水生成氫氧化鈉和氧氣,破壞離子鍵和共價鍵;⑤I2升華破壞分子間作用力,化學鍵不變;⑥固體NaOH熔化電離出鈉離子和氫氧根離子,離子鍵被破壞;
(2)![]() 和
和 的結構完全相同,屬于同一物質;
的結構完全相同,屬于同一物質; ![]() 與
與![]() 的質子數相同,中子數不同,互為同位素;分子式相同、結構不同的化合物互為同分異構體,
的質子數相同,中子數不同,互為同位素;分子式相同、結構不同的化合物互為同分異構體,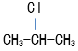 和CH3-CH2-CH2-Cl互為同分異構體;結構相似,分子組成相差若干個CH2原子團的有機物互為同系物,則1-氯丙烷和一氯甲烷互為同系物。
和CH3-CH2-CH2-Cl互為同分異構體;結構相似,分子組成相差若干個CH2原子團的有機物互為同系物,則1-氯丙烷和一氯甲烷互為同系物。


 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:
【題目】密閉容器中充入一定量N2和H2,在一定條件下發生反應:N2+3H2![]() 2NH3。下列說法錯誤的是
2NH3。下列說法錯誤的是
A.使用合適催化劑可以加快反應速率
B.升高溫度可以增大反應速率
C.達到化學平衡時,N2、H2和NH3物質的量濃度一定相等
D.若反應在密閉容器中進行,N2和H2不可能100%轉化為NH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在四個不同容器中,不同條件下進行合成氨反應。根據在相同時間內測定的結果判斷生成氨的速率最快的是 ( )
A.v(N2)=0.1mol·L-1·s-1 B.v(H2)=0.1mol·L-1·min-1
C.v(NH3)=0.15mol·L-1·min-1 D.v(H2)=0.3mol·L-1·min-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1) 2016中國首艘國產航母即將竣工,8艘052D驅逐艦下水,加快了我國海軍邁向“藍水海軍”的步伐。

①艦艇底部涂有含Cu2O的防腐蝕涂料。Cu2O屬于________(填字母)。
a. 復合材料
b. 無機非金屬材料
c. 有機高分子材料
②核動力航母中,鈉鉀合金(常溫下呈液態)可用于快中子反應堆導熱劑,是利用了鈉鉀合金性質的________(填字母)。
a. 熔點低、沸點高 b. 導電性好 c. 在空氣中性質不穩定
③航母中供水管道多采用PE(聚乙烯)材料,聚乙烯的化學式為________________。
(2)西蘭花營養豐富,含蛋白質、淀粉、油脂、葉酸、維生素C和葉綠素,營養成份位居同類蔬菜之首,被譽為“蔬菜皇冠”。

①維生素C俗名為________。在一支盛有2 mL 2%淀粉溶液的試管中滴入2滴碘 水,溶液呈藍色,再滴入維生素C的水溶液,溶液顏色變為________,該實驗說明維生素C具有________性。
②油脂在人體內水解的最終產物是________(寫名稱)和甘油。
③西蘭花成分中可做天然著色劑的是________,屬于糖類的是________。
(3) 2016年9月4日,G20峰會召開,揚州天空呈現出干凈的藍色,云彩隨意地鋪散在天空,純凈透明,出現了持續的“水晶天”。
①目前我國空氣質量檢測體系包括:PM2.5、SO2、NO2、O3、CO等指標。其中________被認為是引起霧霾天氣的元兇;會引起硫酸型酸雨的氣體為________。
②NH3催化還原氮氧化合物轉化為無污染物質是目前應用最廣泛的煙氣氮氧化合物脫除技術,寫出NH3催化還原NO2反應的化學方程式________________。
③減少CO2的排放對于環境保護具有重要意義。在海洋碳循環中,可通 過如圖所示的途徑固碳。寫出鈣化作用的離子方程式:________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、W、Z為四種短周期主族元素,在周期表中的位置如圖所示。W原子的最外層電子數與電子層數相同,下列說法正確的是
![]()
A. X只能形成一種氫化物
B. W、X、Y的原子半徑依次增大
C. X的簡單氫化物的熱穩定性比Y的小
D. W的最高價氧化物對應的水化物能溶于稀氨水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物H(分子式為C10H16O2)用于生產涂料、光學材料、黏合劑等,可通過下列路線合成:

已知:①A是一種相對分子質量為42的鏈狀烴;
②羰基合成反應:RCH=CH2+CO+H2![]() RCH2CH2CHO或RCH(CH3)CHO。
RCH2CH2CHO或RCH(CH3)CHO。
請回答下列問題:
(1)A的名稱是__________(系統命名);B的結構簡式是____________。
(2)D中官能團的名稱是__________;D![]() E的反應類型是________。
E的反應類型是________。
(3)寫出E+G![]() H的化學方程式:____________。
H的化學方程式:____________。
(4)I是C的同分異構體,具有下列特征:
①能發生銀鏡反應,也能與鈉反應;②分子中不含甲基。則I的結構簡式為_________。
(5)下列有關F和G的說法正確的是__________。
a.均能與酸性高錳酸鉀溶液反應 b.均能與NaOH溶液發生反應
c.均能發發生消去反應 d.在空氣中完全燃燒的產物相同
(6)參照上述合成路線信息,以乙烯為原料(無機試劑任選),設計制備丙酸乙酯的合成路線:__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】S2Cl2是一種重要的化工產品,常溫時是一種有毒并有惡臭的金黃色液體,熔點-76℃,沸點138℃,易與水反應,進一步氯化可得SCl2。SCl2是櫻桃紅色液體,易揮發,熔點-122℃,沸點59℃。SCl2與S2Cl2相似,有毒并有惡臭,但更不穩定。S2Cl2可用下列裝置制備。

請回答下列問題:
(1)寫出S2Cl2的電子式_____________________;裝置a中的試劑為________________。
(2)寫出實驗室制取Cl2的離子方程式___________________。
(3)裝置b中的反應開始前,需進行的操作是_______________________。
(4)裝置e的作用是______________________________ 。
(5)將d中獲得的S2Cl2提純,需要進行的操作是___________________。
(6) 若將S2Cl2放入水中同時產生沉淀和氣體,寫出S2Cl2與水反應的方程式______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各物質:①6.02×1023個CH4②2.5molH2S③1.5molNH3所含氫原子數目由多到少的順序是( )
A.②③①
B.②①③
C.①②③
D.③②①
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【2017屆遼寧省莊河市高級中學高三上學期期末考試理綜化學試卷】利用反應6NO2+8NH3=7N2+12H2O構成電池的方法,既能實現有效消除氮氧化物的排放,減輕環境污染,又能充分利用化學能,裝置如圖所示。下列說法不正確的是

A. 電流從右側電極經過負載后流向左側電極
B. 為使電池持續放電,離子交換膜需選用陰離子交換膜
C. 電極A極反應式為2NH3-6e-=N2+6H+
D. 當有4.48LNO2(標準狀況) 被處理時,轉移電子為0.8mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com