
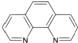
 ),它能與Fe2+形成紅色配合物(如圖1),該配離子中Fe2+與氮原子形成配位鍵共有6個.
),它能與Fe2+形成紅色配合物(如圖1),該配離子中Fe2+與氮原子形成配位鍵共有6個.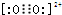 .已知CaC2晶體密度為ag•cm-3,NA表示阿伏加德羅常數,則CaC2晶胞體積為$\frac{256}{a{N}_{A}}$cm3.
.已知CaC2晶體密度為ag•cm-3,NA表示阿伏加德羅常數,則CaC2晶胞體積為$\frac{256}{a{N}_{A}}$cm3.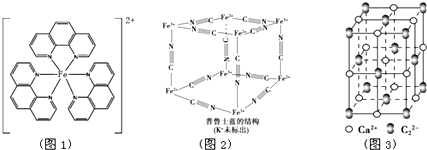
分析 (1)基態C原子核外有6個電子,根據構造原理書寫其基態原子核外電子排布式;
(2)根據價層電子對互斥理論確定C原子雜化方式;
(3)C原子價層電子對個數是3且不含孤電子對,據此判斷其空間構型;
(4)根據圖1分析,Fe與N原子之間的鍵為配位鍵;
(5)利用均攤法計算以及電荷守恒來分析;
(6)等電子體結構和性質相似,根據C22-的結構書寫O22+的電子式;利用均攤法計算出晶胞中含有CaC2的數目,再根據V=$\frac{m}{ρ}$計算.
解答 解:(1)基態C原子核外有6個電子,根據構造原理知C元素基態原子核外電子排布式為1s22s22p2,
故答案為:1s22s22p2;
(2)二氧化碳分子中C原子價層電子對個數是2且不含孤電子對,所以C原子采用sp雜化,故答案為:sp;
(3)C原子價層電子對個數是3且不含孤電子對,所以其空間構型為平面三角形,故答案為:平面三角形;
(4)Fe與N原子之間的鍵為配位鍵,由圖1可知,該配離子中Fe2+與氮原子形成配位鍵共有6個,故答案為:6;
(5)Fe3+離子的個數為:4×$\frac{1}{8}$=$\frac{1}{2}$;Fe2+離子的個數為:4×$\frac{1}{8}$=$\frac{1}{2}$;CN一離子的個數為:12×$\frac{1}{4}$=3,
根據電荷守恒:N(K+)+N(Fe3+)×3+N(Fe2+)×2=N(CN一),得N(K+)=$\frac{1}{2}$,
普魯士藍中 n(K+):n(Fe3+):n(Fe2+):n(CN一)=1:1:1:6,
故答案為:1:1:1:6;
(6)等電子體結構和性質相似,根據C22-的結構知O22+的電子式為 ;CaC2晶胞含有Ca2+數目為12×$\frac{1}{4}$+1=4,含有C22-的數目為8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,則每個晶胞的質量為$\frac{4×64}{{N}_{A}}$g,晶胞的體積為V=$\frac{m}{ρ}$=$\frac{\frac{256}{{N}_{A}}}{{a}^{3}}$=$\frac{256}{a{N}_{A}}$cm3;
;CaC2晶胞含有Ca2+數目為12×$\frac{1}{4}$+1=4,含有C22-的數目為8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,則每個晶胞的質量為$\frac{4×64}{{N}_{A}}$g,晶胞的體積為V=$\frac{m}{ρ}$=$\frac{\frac{256}{{N}_{A}}}{{a}^{3}}$=$\frac{256}{a{N}_{A}}$cm3;
故答案為: ;$\frac{256}{a{N}_{A}}$.
;$\frac{256}{a{N}_{A}}$.
點評 本題考查物質結構和性質,涉及晶胞計算、核外電子排布式的書寫、微粒空間構型判斷、等電子體等知識點,根據等電子體特點、晶胞、價層電子對互斥理論等知識點分析解答即可,題目難度中等.


 培優好卷單元加期末卷系列答案
培優好卷單元加期末卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化鈉的晶體模型: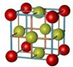 | |
| B. | 鈹原子最外層的電子云圖: | |
| C. | 次氯酸的結構式:H-O-Cl | |
| D. | CH3CHOHCH(CH3)2名稱:2-3-二甲基丙醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,10L pH=1的硫酸溶液中含有的H+數為NA | |
| B. | 將58.5g NaCl溶于1.00L水中,所得NaCl溶液的濃度為1.00mol•L-1 | |
| C. | 1molCl2與足量的鐵反應,轉移的電子數為3NA | |
| D. | 1molAl3+含有的核外電子數為3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 28g N2、N2O、N2O4的混合氣體含有氮原子數為2NA | |
| B. | 質量均為7.8 g Na2S、Na2O2的固體中含有的陰離子數均為0.1NA | |
| C. | 0.5 mol•L-1的乙酸溶液中,乙酸分子的數目小于0.5NA | |
| D. | 78g苯分子中含有碳碳雙鍵數為3 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | D氫化物的穩定性比B氫化物的穩定性強 | |
| B. | 5種元素中,E元素氧化物的水合物的酸性最強 | |
| C. | A與B、D分別可形成AB2、AD2的化合物 | |
| D. | B和C可形成離子化合物,且C離子的半徑大于B離子的半徑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -1131.2 | B. | -647.6 | C. | -507.8 | D. | -323.8 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com