中國政府承諾,到2020年,單位GDP二氧化碳排放比2005年下降40%~50%.
(1)有效“減碳”的手段之一是節能,下列制氫方法最節能的是
C
C
A.電解水制氫:2H
2O
2H
2↑+O
2↑
B.高溫使水分解制氫:2H
2O
2H
2↑+O
2↑
C.太陽光催化分解水制氫:2H
2O
2H
2↑+O
2↑
D.天然氣制氫:CH
4+H
2O
CO+3H
2(2)CO
2可轉化成有機物實現碳循環.在體積為1L的密閉容器中,充入1mol CO
2和3mol H
2,一定條件下反應:
CO
2(g)+3H
2(g)?CH
3OH(g)+H
2O(g)△H=-49.0kJ?mol
-1,測得CO
2和CH
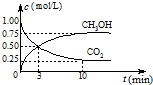
3OH(g)的濃度隨時間變化如圖所示.
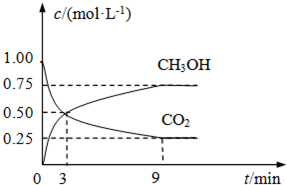
①從3min到9min,v(H
2)=
0.125
0.125
mol?L
-1?min
-1.
②能說明上述反應達到平衡狀態的是
D
D
(填編號).
A.反應中CO
2與CH
3OH的物質的量濃度之比為1:1(即圖中交叉點)
B.混合氣體的密度不隨時間的變化而變化
C.單位時間內消耗3mol H
2,同時生成1mol H
2O
D.CO
2的體積分數在混合氣體中保持不變
(3)工業上,CH
3OH也可由CO和H
2合成.參考合成反應CO(g)+2H
2(g)?CH
3OH(g)的平衡常數:
| 溫度/℃ |
0 |
100 |
200 |
300 |
400 |
| 平衡常數 |
667 |
13 |
1.9×10-2 |
2.4×10-4 |
1×10-5 |
下列說法正確的是
AC
AC
.
A.該反應正反應是放熱反應
B.該反應在低溫下不能自發進行,高溫下可自發進行,說明該反應△S<0
C.在T℃時,1L密閉容器中,投入0.1mol CO和0.2mol H
2,達到平衡時,CO轉化率為50%,則此時的平衡常數為100
D.工業上采用稍高的壓強(5Mpa)和250℃,是因為此條件下,原料氣轉化率最高.