
已知:⑴Al(OH)3的電離方程式為:AlO2-+H++H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH-;⑵無水AlCl3晶體的沸點為182.9℃,溶于水的電離方程式為:AlCl3=Al3++3Cl-;⑶PbSO4難溶于水,易溶于醋酸鈉溶液,反應的化學方程式為:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb。下列關于Al(OH)3、AlCl3和(CH3COO)2Pb的說法中正確的是
Al3++3OH-;⑵無水AlCl3晶體的沸點為182.9℃,溶于水的電離方程式為:AlCl3=Al3++3Cl-;⑶PbSO4難溶于水,易溶于醋酸鈉溶液,反應的化學方程式為:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb。下列關于Al(OH)3、AlCl3和(CH3COO)2Pb的說法中正確的是
A.均為強電解質 B.均為弱電解質
C.均為離子化合物 D.均為共價化合物
科目:高中化學 來源: 題型:
PbSO4+2CH3COONa====Na2SO4+(CH3COO)2Pb下列關于Al(OH)3、AlCl3和(CH3COO)2Pb的說法正確的是( )
A.均為強電解質 B.均為弱電解質
C.均為離子化合物 D.均為共價化合物
查看答案和解析>>
科目:高中化學 來源:2012-2013學年安徽省泗縣二中高二下學期期末考試化學試卷(帶解析) 題型:單選題
已知Ba[Al(OH)4]2可溶于水。右圖表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液時,生成沉淀的物質的量y與加入Ba(OH)2的物質的量x的關系。下列有關敘述正確的是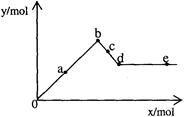
A a-b時沉淀的物質的量:A1(OH)3比BaSO4多
B d-e時溶液中離子的物質的量:Ba2+可能等于OH-
C a-d時沉淀的物質的量:BaSO4可能小于A1(OH)3
D c-d時溶液中離子的物質的量:[Al(OH)4]-比Ba2+少
查看答案和解析>>
科目:高中化學 來源:2011屆福建省四地六校高三畢業班考前模擬考試(理綜)化學部分 題型:填空題
(15分)我國鈦鐵礦(主要成分為FeTiO3,還含有Al2O3、SiO2等)的儲量居世界首位,用鈦鐵礦制取TiO2和副產品硫酸亞鐵晶體的的流程如下:
已知:Al(OH)3的Ksp= 1.3ⅹ10-33,Fe(OH)2的Ksp= 1.6ⅹ10-14。
(1)濾液I主要含有TiO2+、SO42—、Fe2+、 (填離子符號);
(2)調節PH應最好使用 ;
| A.Fe | B.Ca(OH)2 | C.NH3?H2O | D.NaOH |
 生的反應為:
生的反應為: 92),則產品中硫酸亞鐵銨晶體純度的計算式可表達為:w%= 。
92),則產品中硫酸亞鐵銨晶體純度的計算式可表達為:w%= 。查看答案和解析>>
科目:高中化學 來源:2013-2014學年河北省高三上學期第四次月考化學試卷(解析版) 題型:選擇題
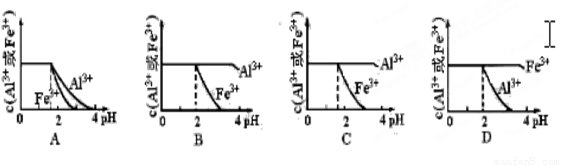
已知Ksp[Al(OH)3]=1.3×10-33 mol4·L-4, Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4。現向pH=0濃度均為0.04mol·L-1的Al3+、Fe3+溶液中加入NaOH溶液,以調節pH(設溶液體積不變),該過程中Al3+、Fe3+的濃度與pH關系正確的是( )
查看答案和解析>>
科目:高中化學 來源:浙江省2010-2011學年高三第一次質量檢測 題型:填空題
閱讀下表中短周期主族元素的相關信息。
|
元素代號 |
相關信息 |
|
A |
A的單質能與冷水劇烈反應,得到強堿性溶液 |
|
B |
B的原子最外層電子數是其內層電子數的三倍 |
|
C |
在第3周期元素中,C的簡單離子半徑最小 |
|
D |
A、B、D組成的36電子的化合物X是家用消毒劑的主要成分 |
|
E |
所有有機物中都含有E元素 |
請回答:(1)、在一定條件下,B2與C的單質在海水中可形成原電池,為新型海水航標燈提供能源。寫出該原電池正極的電極反應式 。
(2)、用惰性電極電解化合物AD的水溶液,該反應的化學方程式為:
其中,陰極產物是
(3)、常溫下,0.1 mol·L-1X溶液的pH 7(填“>”、“=”或“<”),原因是 (用離子方程式說明)。
(4)、已知Ksp[Al(OH)3]=1.3×10-33,Ksp[Fe(OH)3]=4.0×10-38。
現向pH=0,濃度均為0.04mol·L-1的Al3+、Fe3+溶液中加入A的最高價氧化物對應水化物的溶液,以調節pH(設溶液體積不變),該過程中Al3+、Fe3+的濃度與pH關系正確的是
(填字母代號)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com