
【題目】A、B、C、D四種短周期元素,其原子序數依次增大,其中B與C同周期,A與D同主族,C元素的原子最外層電子數是次外層電子數的三倍,又知四種元素所形成的常見單質在常溫常壓下有三種是氣體,一種是固體.請回答下列問題.
(1)固體甲是由元素B、A形成的化合物BA5 , 它的所有原子的最外層都符合相應的稀有氣體原子的最外層電結構,固體甲溶解于水有氣體放出.則固體甲屬于晶體,它的電子式為 . 固體甲溶于水后,溶液呈(酸、堿或中性),寫出甲與水反應的化學方程式 .
(2)由C和D形成的化合物乙溶于水能生成一種氣體,寫出乙與水反應的化學方程式 .
【答案】
(1)離子晶體;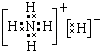 ;堿;NH5+H2O=NH3?H2O+H2↑
;堿;NH5+H2O=NH3?H2O+H2↑
(2)2Na2O2+2H2O=4NaOH+O2↑
【解析】解:(1)N、H在化合物BA5中形成了稀有氣體原子的最外層電結構,一個H原子得到一個電子形成H﹣離子,故此化合物為 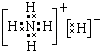 ,屬于離子晶體,
,屬于離子晶體, 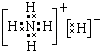 溶于水反應生成一水合氨使溶液呈堿性,反應方程式為NH5+H2O=NH3H2O+H2↑,所以答案是:離子晶體;
溶于水反應生成一水合氨使溶液呈堿性,反應方程式為NH5+H2O=NH3H2O+H2↑,所以答案是:離子晶體; 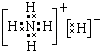 ;堿; NH5+H2O=NH3H2O+H2↑;(2)由O和Na形成的化合物Na2O2溶于水能生成一種氣體,Na2O2與水反應的化學方程式為2Na2O2+2H2O=4NaOH+O2↑, 所以答案是:2Na2O2+2H2O=4NaOH+O2↑.
;堿; NH5+H2O=NH3H2O+H2↑;(2)由O和Na形成的化合物Na2O2溶于水能生成一種氣體,Na2O2與水反應的化學方程式為2Na2O2+2H2O=4NaOH+O2↑, 所以答案是:2Na2O2+2H2O=4NaOH+O2↑.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】可充電電池在現代生活中有廣泛應用.已知某鎳鎘電池的電解質溶液為KOH溶液,其充、放電按下式進行:Cd+2NiOOH+2H2O ![]() Cd(OH)2+2Ni(OH)2有關該電池的說法正確的是( )
Cd(OH)2+2Ni(OH)2有關該電池的說法正確的是( )
A.放電時負極附近溶液的堿性不變
B.充電過程是化學能轉化為電能的過程
C.充電時陽極反應:Ni(OH)2﹣e﹣+OH﹣═NiOOH+H2O
D.放電時電解質溶液中的OH﹣向正極移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋酸鎳[(CH3COO)2Ni]是一種重要的化工原料。一種以含鎳廢料(含NiS、Al2O3、FeO、CaO、SiO2)為原料,制取醋酸鎳的工藝流程圖如下:

相關離子生成氫氧化物的pH 和相關物質的溶解性如下表:
金屬離子 | 開始沉淀的pH | 沉淀完全的pH | 物質 | 20℃時溶解性(H2O) |
Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 |
Fe2+ | 5.8 | 8.8 | NiF | 可溶 |
Al3+ | 3.0 | 5.0 | CaF2 | 難溶 |
Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.60×10-6 |
(1)調節pH 步驟中,溶液pH的調節范圍是________。
(2)濾渣1和濾渣3 主要成分的化學式分別是________、________。
(3)寫出氧化步驟中加入H2O2 發生反應的離子方程式________。
(4)酸浸過程中,1molNiS失去6 NA個電子,同時生成兩種無色有毒氣體。寫出該反應的化學方程式________。
(5)沉鎳過程中,若c(Ni2+)=2.0 mol·L-1,欲使100 mL該濾液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol·L-1],則需要加入Na2CO3固體的質量最少為________g。(保留小數點后1位有效數字)
(6)保持其他條件不變,在不同溫度下對含鎳廢料進行酸浸,鎳浸出率隨時間變化如圖。酸浸的最佳溫度與時間分別為________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() He可作為核聚變材料,以下關于
He可作為核聚變材料,以下關于 ![]() He的敘述正確的是( )
He的敘述正確的是( )
A.![]() He原子核內中子數為2
He原子核內中子數為2
B.![]() He和
He和 ![]() H是同一元素的不同原子
H是同一元素的不同原子
C.![]() He核外電子數為2
He核外電子數為2
D.![]() He代表原子核內有2個質子和3個中子的氦原子
He代表原子核內有2個質子和3個中子的氦原子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于焰色反應的說法不正確的是( )
A.只有金屬化合物才有焰色反應
B.只有某些金屬或其化合物才有焰色反應
C.透過藍色鈷玻璃觀察鉀元素焰色反應的顏色為紫色
D.每次焰色反應實驗后都要將鉑絲用稀鹽酸洗凈并灼燒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖所示裝置可間接氧化工業廢水中含氮離子(NH4+)。下列說法不正確的是
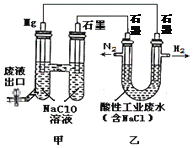
A. 乙是電能轉變為化學能的裝置
B. 含氮離子氧化時的離子方程式為:3Cl2 + 2NH4+=N2 + 6Cl-+8H+
C. 若生成H2和N2的物質的量之比為3:1,則處理后廢水的pH減小
D. 電池工作時,甲池中的Na+移向Mg電極
【答案】D
【解析】A、甲中活潑金屬鎂作原電池的負極,石墨為正極形成原電池,乙是連接原電池的電解池,電解酸性工業廢水,電解池是將電能轉變為化學能的裝置,選項A正確;B、酸性條件下含氮離子氧化時轉化為氮氣,反應的離子方程式為:3Cl2 + 2NH4+=N2 + 6Cl-+8H+,選項B正確;C、若生成H2和N2的物質的量之比為3:1,根據電極反應6H++6e-=3H2↑、3Cl2 + 2NH4+=N2 + 6Cl-+8H+,則處理后廢水的H+濃度增大,pH減小,選項C正確;D、電池工作時,甲池是原電池,原電池中陽離子Na+移向正極石墨電極,選項D不正確。答案選D。
【題型】單選題
【結束】
7
【題目】已知某透明澄清的溶液中可能含有NO3- 、Cl- 、SO42-、CO32-、NH4+、Fe3+、Al3+和K+中的幾種,且所含陰離子的物質的量相等。為確定該溶液的成分,某學習小組做了如下實驗:①取該溶液100mL,加入過量NaOH溶液,加熱得到0.02mol氣體,同時產生紅褐色沉淀; ②將沉淀過濾、洗滌、灼燒,得到1.6 g固體; ③向上述濾液中加入足量BaCl2溶液,得到4.66 g不溶于鹽酸的沉淀。下列說法正確的是
A. 不能確定原溶液中是否含有Al3+和K+
B. 原溶液中含有的離子只有:Cl- 、SO42-、NH4+、Fe3+
C. 原溶液中c(NO3-)=0.2 mol·L-1 c(Fe3+)=0.2 mol·L-1
D. 在原溶液中加入足量的鐵粉所得溶液中陽離子所帶正電荷數減少
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的數值,下列說法中正確的是( )
A. 標準狀況下,1molSO3的體積為22.4L
B. 1mol 二氧化氮與足量的水反應電子轉移總數為3NA
C. 標準狀況下,將22.4LSO2通入水中形成1L溶液,得到H2SO3的濃度為1mol/L
D. 常溫下,23gNO2和N2O4的混合氣體中含有NA個氧原子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機化合物說法正確的是
A. 有機物![]() 的名稱是2,3,5,5-四甲基-4-乙基己烷
的名稱是2,3,5,5-四甲基-4-乙基己烷
B. 乙酸乙酯在堿性條件下的水解反應稱為皂化反應
C. 有機物![]() 中可能共面的原于數最多有17個
中可能共面的原于數最多有17個
D. 乙醛和丙烯醛(![]() )不是同系物,分別與足量H2反應后的產物也不是同系物
)不是同系物,分別與足量H2反應后的產物也不是同系物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為驗證還原性:SO2>Fe2+>C1-,三組同學分別進行了下圖實驗,并對溶液1和溶液2中所含離子進行了檢驗,能證明上述還原性順序的實驗組有
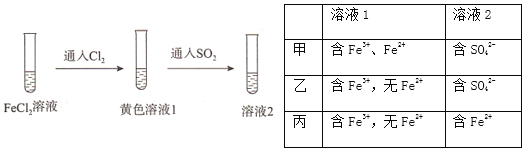
A. 只有甲 B. 甲、乙 C. 甲、丙 D. 甲、乙、丙
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com