
| 1g |
| 2g/mol |
| 1mol |
| 0.5mol |
| 1 |
| 2 |
| 1 |
| 2 |



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A��һ���]���Ƅ� | B��һ�����������Ƅ� |
| C��һ�����淽���Ƅ� | D���o���_�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| A��c��X2��=0.15mol/L | B��c��Y2��=0.7mol/L |
| C��c��Z2��=0.3mol/L | D��c��Q2��=0.6mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
| 1 |
| 2 |
| A��196.64kJ | B����196.64kJ/mol |
| C����196.64kJ | D����196.64kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
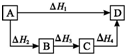
| A����H1=��H2=��H3=��H4 | B����H1+��H2=��H3+��H4 |
| C����H1+��H2+��H3=��H4 | D����H1=��H2+��H3+��H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ������}
| ��(sh��)�M | �ض�/�� | ��ʼ��/mol | ƽ����/mol | �_(d��)��ƽ���� ��r�g/min | ||
| H2O | CO | CO2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}
A����H=��H1+
| B����H=��H1+
| ||||||||
| C����H=��H1+2��H2+2��H3 | D����H=2��H1+��H2+��H3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ����Ԕ �}�ͣ����x�}

| A��ˮ����늽��|(zh��) | B����ȼ���ǿ���ȼ����ˮ |
| C�������ɷNԪ��ֻ�ܽM��ˮ | D��0��r�����ܶȱ�Һ�B(t��i)ˮ���ܶȴ� |
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com