
【題目】已知可逆反應aA2 +bB2![]() xX(反應物、生成物都是氣體)。回答下列問題:
xX(反應物、生成物都是氣體)。回答下列問題:
I.將一定量的兩種反應物置于恒容絕熱反應器中(與外部環(huán)境無熱量交換的反應器),反應器內(nèi)的溫度與時間的關系如圖:

(1)該反應是___ (填“吸”或“ 放”)熱反應。
(2)下列關于該反應的敘述正確的是____ (填字母)。
a A點反應停止 b A點速率不為零
c 反應物的總能量大于生成物的 d B點正反應速率大于逆反應速率
II.將一定量的上述反應的反應物與生成物置于容積為2L的恒溫恒容反應器中,反應器中各物質的物質的量與時間的關系如圖:

(3)①反應前4 min物質x的物質的量的變化為_____mol. .
②反應前4 min物質A2反應速率為_______
③該可逆反應的化學方程式為______(物質X用A、B表示)。
④如果在4 min時升高反應體系的溫度.則反應速率___ ( 填“增大“減小”或“不變")。
⑤如果在4min時加入2.4 mol Ne(Ne不參與該反應),則反應速率___ (填“增大”“減小”或“不變”)。
【答案】吸 b d 0.4 0.025mol·L-1·min-1 A2+3B2 ![]() 2AB3 增大 不變
2AB3 增大 不變
【解析】
I.(1)由圖可知,隨著反應不斷進行,溫度逐漸下降,說明該反應為吸熱反應,故本題答案為:吸;
(2)a.由圖可知,A點是平衡狀態(tài),是動態(tài)平衡,反應未停止,a錯誤;
b.由圖可知,A點是平衡狀態(tài),是動態(tài)平衡,反應仍在進行,A點速率不為零,b正確;
c.該反應為吸熱反應,反應物的總能量小于生成物的總能量,c錯誤;
d.B點未達到平衡狀態(tài),反應在正向進行,所以正反應速率大于逆反應速率,d正確;
故本題答案為:bd ;
II.(3)①由圖可知,反應前4 min物質x的物質的量的變化為0.8mol-0.4mol=0.4mol,故本題答案為:0.4;
②反應前4 min物質A2的變化量為0.2mol,反應速率為![]() =0.025mol·L-1·min-1,故本題答案為:0.025mol·L-1·min-1;
=0.025mol·L-1·min-1,故本題答案為:0.025mol·L-1·min-1;
③在0-4min時,A2的化學反應反應速率為![]() =0.025mol·L-1·min-1,B2的化學反應反應速率為
=0.025mol·L-1·min-1,B2的化學反應反應速率為![]() =0.075mol·L-1·min-1,X的化學反應反應速率為
=0.075mol·L-1·min-1,X的化學反應反應速率為![]() =0.05mol·L-1·min-1,化學反應速率之比等于化學計量數(shù)之比,即化學計量數(shù)之比為:A2:B2:X=1:3:2,根據(jù)原子守恒,則該可逆反應的化學方程式為A2+3B2
=0.05mol·L-1·min-1,化學反應速率之比等于化學計量數(shù)之比,即化學計量數(shù)之比為:A2:B2:X=1:3:2,根據(jù)原子守恒,則該可逆反應的化學方程式為A2+3B2![]() 2AB3,故本題答案為:A2+3B2
2AB3,故本題答案為:A2+3B2![]() 2AB3;
2AB3;
④升高反應體系的溫度,活化分子數(shù)增多,反應速率增大,故本題答案為:增大;
⑤在4min時加入2.4 mol Ne,Ne不參與該反應,由于是恒容體系,對反應物濃度無影響,對反應速率也無影響,所以反應速率不變,故本題答案為:不變。


科目:高中化學 來源: 題型:
【題目】某烴A的相對分子質量為84。回答下列問題:
(1)烴A的分子式為__。下列物質與A以任意比例混合,若總物質的量一定,充分燃燒消耗氧氣的量不變的是_____;若總質量一定,充分燃燒消耗氧氣的量不變的是_____。
A.C7H8 B.C6H14 C.C7H14 D.C8H8
(2)若烴A分子中所有的碳原子在同一平面上,且該分子的一氯取代物只有一種。則A的結構簡式為__。若A不能使溴水褪色,且其一氯代物只有一種,則A的結構簡式為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列做法符合原子經(jīng)濟性原理的是
A.SO3與H2O反應制取硫酸:SO3+H2O=H2SO4
B.用氫氧化鈉溶液吸收SO2:SO2+2NaOH=Na2SO3+H2O
C.CO2與H2反應制取甲醇:CO2+3H2 CH3OH+H2O
CH3OH+H2O
D.H2還原氧化銅:H2+CuO![]() Cu+H2O
Cu+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知溶液中存在平衡:Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq) ΔH<0,下列有關該平衡體系的說法正確的是( )
Ca2+(aq)+2OH-(aq) ΔH<0,下列有關該平衡體系的說法正確的是( )
①升高溫度,平衡逆向移動 ②向溶液中加入少量碳酸鈉粉末能增大鈣離子的濃度
③除去氯化鈉溶液中混有的少量鈣離子,可以向溶液中加入適量的NaOH溶液
④恒溫下,向溶液中加入CaO,溶液的pH升高
⑤向溶液中加入少量NaOH固體,Ca(OH)2固體質量不變
⑥向溶液中加入Na2CO3溶液,其中固體質量增加
A.①⑥B.①⑤⑥C.②③④⑥D.①②⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學進行影響草酸溶液與高錳酸鉀酸性溶液反應速率因素的研究。室溫下,實驗數(shù)據(jù)如下:
實驗序號 | ① | ② | ③ |
加入試劑 | 4mL 0.01mol/L KMnO4 2mL 0.1mol/L H2C2O4 | 4mL 0.01mol/L KMnO4 2mL 0.1mol/L H2C2O4 少量MnSO4固體 | 4mL 0.01mol/L KMnO4 2mL 0.1mol/L H2C2O4 少量Na2SO4固體 |
褪色時間/s | 116 | 6 | 117 |
(1)草酸溶液與高錳酸鉀酸性溶液反應的離子方程式為___________________。
(2)該實驗結論是_______________________。
(3)進行上述三個實驗后,該同學進行反思,認為實驗①的現(xiàn)象可以證明上述結論。請寫出實驗①的現(xiàn)象為____________________。
(4)實驗②選用MnSO4固體而不是MnCl2固體的原因是_________________。
(5)該同學擬采用如下圖所示的實驗方案繼續(xù)探究外界條件對反應速率的影響。

a.該同學擬研究的影響因素是___________________。
b.你認為該同學的實驗方案_______________(填“合理”或“不合理”),理由是____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業(yè)上可用一氧化碳合成可再生能源甲醇。
(1)已知:Ⅰ.3CO(g)+6H2(g)![]() CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
Ⅱ.3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
則CO與H2合成氣態(tài)甲醇的熱化學方程式為___________________________________
(2)某科研小組在Cu2O/ZnO作催化劑的條件下,在500℃時,研究了n(H2):n(CO)分別為2:1、5:2時CO的轉化率變化情況(如圖1所示),則圖中表示n(H2):n(CO)=2:1的變化曲線為___________(填“曲線a”或“曲線b”),原因是_______________________________。
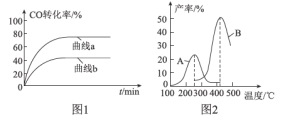
(3)某科研小組向密閉容器中充入一定量的CO和H2合成氣態(tài)甲醇,分別在A、B兩種不同催化劑作用下發(fā)生反應,一段時間后測得CH3OH的產(chǎn)率與溫度的關系如圖2所示。下列說法正確的是____________(填選項字母)。
a.使用催化劑A能加快相關化學反應速率,但催化劑A并未參與反應
b.在恒溫恒壓的平衡體系中充入氬氣,CH3OH的產(chǎn)率降低
c.當2v(CO)正=v(H2)逆時,反應達到平衡狀態(tài)
(4)一定溫度下,在容積均為2L的兩個恒容密閉容器中,按如下方式加入反應物,一段時間后達到平衡。

若甲容器平衡后氣體的壓強為開始時的![]() ,則該溫度下,該反應的平衡常數(shù)K=______,要使平衡后乙容器與甲容器中相同組分的體積分數(shù)相等,且起始時維持化學反應向逆反應方向進行,則乙容器中c的取值范圍為_____________________________________。
,則該溫度下,該反應的平衡常數(shù)K=______,要使平衡后乙容器與甲容器中相同組分的體積分數(shù)相等,且起始時維持化學反應向逆反應方向進行,則乙容器中c的取值范圍為_____________________________________。
(5)CO與日常生產(chǎn)生活相關。
①檢測汽車尾氣中CO含量,可用CO分析儀,工作原理類似于燃料電池,其中電解質是氧化釔(Y2O3)和氧化鋯(ZrO2)晶體,能傳導O2-。則負極的電極反應式為__________________。
②碳酸二甲醋[(CH3O)2CO]毒性小,是一種綠色化工產(chǎn)品,用CO合成(CH3O)2CO,其電化學合成原理為4CH3OH+2CO+O2![]() 2(CH3O)2CO+2H2O,裝置如圖3所示:
2(CH3O)2CO+2H2O,裝置如圖3所示:
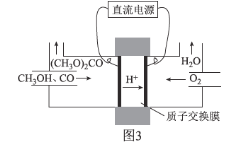
寫出陽極的電極反應式:________________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋅是一種常用金屬,工業(yè)上利用鋅焙砂(主要含ZnO、ZnFe2O4,還含有少量CaO、FeO、CuO、NiO 等)濕法制取金屬鋅的流程如圖所示,回答下列問題。

已知:Fe的活潑性強于Ni。
(1)ZnFe2O4可寫成ZnOFe2O3,則ZnFe2O4與H2SO4反應的化學方程式___。
(2)“凈化Ⅰ”操作分為兩步:
①將溶液中少量的 Fe2+氧化,下列試劑中可選用的是_____(填字母標號)。
A.新制氯水 B.30 % H2O2溶液 C.FeC13溶液 D.KMnO4溶液
②加入ZnO,調節(jié)溶液pH為3.3~6.7;加熱到60℃左右并不斷攪拌,加熱攪拌主要目的是___。
(3)“凈化Ⅰ”生成的沉淀中還含有溶液中的懸浮雜質,溶液中的懸浮雜質被共同沉淀的原因是____。
(4)“凈化Ⅱ”中加入過量Zn的目的是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W、Q、R均為前四周期元素,且原子序數(shù)依次增大。其相關信息如下表所示:
X元素的基態(tài)原子中電子分布在三個不同的能級中,且每個能級中的電子總數(shù)相同 |
Y元素的氣態(tài)氫化物與其最高價氧化物對應的水化物能發(fā)生化合反應 |
Z元素的族序數(shù)是其周期數(shù)的三倍 |
W原子的第一至第六電離能分別為:I1=578KJ·mol-1I2=1817KJ·mol-1I3=2745KJ·mol-1 I4=11575KJ·mol-1I5=14830KJ·mol-1I6=18376KJ·mol-1 |
Q為前四周期中電負性最小的元素 |
元素R位于周期表的第10列 |
回答下列問題:
(1)Y元素的基態(tài)原子中未成對電子數(shù)為______;X、Y、Z三種元素原子的第一電離能由小到大的順序為____________(用元素符號表示)。
(2)W的氯化物的熔點比Q的氯化物的熔點__________(填“高”或“低”),理由是__________________________________________________。
(3)光譜證實元素W的單質與強堿性溶液反應有[W(OH)4]-生成,則[W(OH)4]-中存在(填字母)_____________。
a.極性共價鍵 b.非極性共價鍵 c.配位鍵 d.氫鍵
(4)含有X、R和鎂三種元素的某種晶體具有超導性,其結構如下圖所示。則該晶體的化學式為_______;晶體中每個鎂原子周圍距離最近的R原子有_______個。
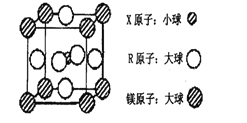
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有A、B、C、D、E、F六種元素,已知:
①它們位于三個不同短周期,核電荷數(shù)依次增大
②E元素的電離能數(shù)據(jù)見下表(kJ·mol-1):
I1 | I2 | I3 | I4 | … |
496 | 4562 | 6912 | 9540 | … |
③B與F分別同主族
④A、E分別都能與D按原子個數(shù)比1﹕1或2﹕l形成化合物
⑤B、C分別都能與D按原子個數(shù)比1﹕1或1﹕2形成化合物
(1)寫出只含有A、B、D、E四種元素的兩種無水鹽的化學式_____________、______________
(2)B2A2分子中存在____個σ鍵,____個π鍵
(3)E2D2電子式____________
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com