
【題目】用酸性氫氧燃料電池電解硫酸鈉飽和溶液的裝置如圖所示(a、b為銅電極)。下列說法中不正確的是( )
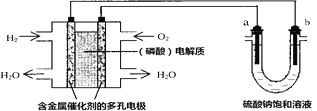
A. 電池工作時,正極反應式為:O2+4H++4e-=2H2O
B. 電解時,當陰極逸出a mol氣體,同時有W克Na2SO410H2O 析出,保持溫度不變,剩余溶中的硫酸鈉的質量分數是![]()
C. 電解時,電子流動路徑是:負極→外電路→陰極→陽極→正極
D. 若忽略能量損耗,當電池中消耗0.01mol O2 時,b 極周圍會產生0.02mol H2
【答案】C
【解析】
左邊裝置是氫氧燃料電池,左邊裝置是原電池,原電池放電時,燃料H2失電子發生氧化反應,所以投放燃料的電極為負極,投放氧化劑O2的電極為正極,正極上氧化劑得電子發生還原反應;右邊裝置有外接電源,右邊裝置是電解池,連接負極的b電極是陰極,連接正極的a電極是陽極,陽極上失電子發生氧化反應,陰極上得電子發生還原反應;兩電池工作時,電子的流動路徑是:負極→外電路→陰極b;陽極→正極。
A.左邊裝置是氫氧燃料電池,所以是原電池;原電池放電時,正極上氧化劑得電子發生還原反應,即氧氣得電子和溶液的H+結合生成水,電極反應式為O2+4H++4e-=2H2O,A正確;
B.電解時,陰極上H+獲得電子變為氫氣逸出,電極反應式為2H++2e-=H2↑,當陰極逸出amol氣體電解的水的質量為:2H2O![]() O2↑+2H2↑,根據方程式的關系可知每有2mol水即36g水反應,會反應產生2molH2,若反應產生amolH2,則反應需要電解18ag水,所以當陰極逸出amol氣體電解的水的質量為18ag,電解后的溶液仍為飽和溶液,溶液的質量分數為:
O2↑+2H2↑,根據方程式的關系可知每有2mol水即36g水反應,會反應產生2molH2,若反應產生amolH2,則反應需要電解18ag水,所以當陰極逸出amol氣體電解的水的質量為18ag,電解后的溶液仍為飽和溶液,溶液的質量分數為:![]() ×100%=
×100%=![]() ×100%,B正確;
×100%,B正確;
C.電子在導線中移動,不能在溶液中移動,C錯誤;
D.燃料電池和電解池中轉移的電子數是相等的,當電池中消耗0.01mol O2 時,根據電極反應:O2+4e-+4H+=2H2O,所以轉移電子0.04mol,在b極的電極反應為:2H++2e-=H2↑,轉移電子0.04mol,會產生0.02molH2,D正確;
故合理選項是C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】下列化學方程式中,不能正確表達反應顏色變化的是
A. 向CuSO4溶液中加入足量Zn粉,溶液藍色消失Zn+CuSO4![]() Cu+ZnSO4
Cu+ZnSO4
B. 澄清的石灰水久置后出現白色固體Ca(OH)2+CO2![]() CaCO3↓+H2O
CaCO3↓+H2O
C. Na2O2在空氣中放置后由淡黃色變為白色2Na2O2![]() 2Na2O+O2↑
2Na2O+O2↑
D. 向Mg(OH)2懸濁液中滴加足量FeCl3溶液出現紅褐色沉淀3Mg(OH)2+2FeCl3![]() 2Fe(OH)3+3MgCl2
2Fe(OH)3+3MgCl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I、為了研究化學反應A+B=C+D的能量變化情況,某同學設計了如圖所示裝置。當向盛有A的試管中滴加試劑B時,看到U形管中甲處液面下降乙處液面上升。試回答下列問題:
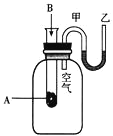
(1)該反應為________反應(填“放熱”或“吸熱”)。
(2)A和B的總能量比C和D的總能量_________(填“高”或“低”)。
(3)該反應的物質中的化學能通過化學反應轉化成________釋放出來。
(4)該反應的反應物化學鍵斷裂吸收的能量________(填“高”或“低”)于生成物化學鍵形成放出的能量。
(5)Ⅱ、同素異形體相互轉化的反應熱相當小,而且轉化速率較慢,有時還很不完全,測定反應熱很困難。現在可根據蓋斯提出的“不管化學過程是一步完成還是分幾步完成,這個總過程的熱效應是相同的”觀點來計算反應熱。
已知:
①P4(白磷,s)+5O2(g)= P4O10(s) ΔH=-2983.2 kJ·mol1
②P(紅磷,s)+5/4O2(g)=1/4P4O10(s) ΔH=-738.5 kJ·mol1
則白磷轉化為紅磷的熱化學方程式為__________。相同狀況下,能量狀態較低的是________;白磷的穩定性比紅磷_________(填“高”或“低”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法錯誤的是
A. 電解飽和食鹽水可制取燒堿、氯氣、氫氣
B. 從海水中可提取鎂、溴、碘等物質
C. 粗銅(含少量Zn、Fe、Pt等)電解精煉后,溶液中金屬陽離子只有Fe2+、Zn2+
D. 在鍍件上鍍銅,鍍件作陰極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學技術名詞審定委員會已確定第116號元素Lv的名稱為鉝。關于![]() 的敘述錯誤的是( )
的敘述錯誤的是( )
A. 原子序數116B. 中子數177
C. 核外電子數116D. 相對原子質量293
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)1.7g氨氣在標準狀況下的體積是_____________升,共含有_____________mol電子;0.1mol硫化氫共含有_____________個質子,同質量的氨氣和硫化氫氣體中分子個數比為_____________,含氫原子的個數比為_____________。在標準狀況下硫化氫的密度為_____________。
(2)在標準狀況下,18gCO和CO2的混合氣體完全燃燒后得到11.2LCO2,則原混合氣體的密度是_____________,原混合氣體中,CO的質量是_____________,CO2的體積是_____________碳原子和氧原子的個數比為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究物質的合成或制備是有機化學、無機化學的重要任務之一。
(1)某實驗小組探究實驗室制備無水氯化鎂的方法,設計了如下圖裝置。
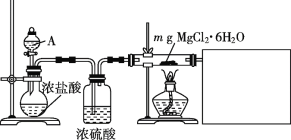
①分液漏斗中的A物質是___________ (填試劑名稱)。
②利用中學常見的儀器,某同學在空白方框內補充完整實驗裝置,他選擇的試劑有____ (填序號)
A.稀NaOH溶液 B.無水氯化鈣 C.稀硫酸 D.濃硫酸
(2)實驗室制備并收集純凈乙烯。
①有的同學通過乙醇制備乙烯,寫出相關化學方程式:_______________;該實驗除乙醇外,所需的試劑或用品(不包括儀器)有_______________________。
②有的同學探究其他制備乙烯的方法,他設計了下圖裝置制備乙烯。實驗結果是量筒內壁附著較多無色油狀液體,且得到很少量的氣體。請分析氣體產率很低的原因主要是_______。
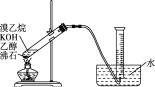
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是利用陰離子交換膜和過濾膜制備高純度的Cu的裝置示意圖,下列有關敘述不正確的是
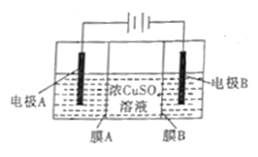
A. 電極A是粗銅,電極B是純銅
B. 電路中通過1mol電子,生成32g銅
C. 溶液中SO42-向電極A遷移
D. 膜B是過濾膜,阻止陽極泥及雜質進入陰極區
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)含11.2 g KOH的稀溶液與1 L0.1mol/L的H2SO4溶液反應放出11.46 kJ的熱量,該反應表示中和熱的熱化學方程式為___________________。
(2)將0.40 mol N2O4氣體充入2 L的恒容密閉容器中發生如下反應:N2O4(g) ![]() 2NO2(g)ΔH。在T1℃和T2℃時,測得NO2的物質的量隨時間變化如圖所示:
2NO2(g)ΔH。在T1℃和T2℃時,測得NO2的物質的量隨時間變化如圖所示:
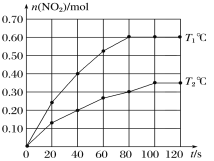
①T1℃,40~80 s內用N2O4表示該反應的平均反應速率為________mol/(L·s)。
②ΔH________0(填“>”、“<”或“=”)。
(3)向甲、乙兩個容積均為1 L的恒容容器中,分別充入2 mol A、2 mol B和1 mol A、1 mol B。相同條件下(溫度T ℃),發生下列反應:A(g)+B(g)![]() xC(g) ΔH<0。測得兩容器中c(A)隨時間t的變化如圖所示:
xC(g) ΔH<0。測得兩容器中c(A)隨時間t的變化如圖所示:
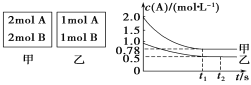
①甲容器平衡后物質B的轉化率為_______;
②T℃ 時該反應的平衡常數為________。
(4)在25 ℃下,將a mol/L的氨水與0.01mol/L的鹽酸等體積混合,反應平衡時溶液中c(NH4+)=c(Cl-)。
①則溶液顯________性(填“酸”“堿”或“中”);
②用含a的代數式表示NH3·H2O的電離常數Kb=__________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com