
一定溫度下的密閉容器中存在如下反應:
CO(g)+H2O(g) CO2(g)+
H2(g),已知CO(g)和H2O(g)的起始濃度均為2 mol·L-1,經測定該反應在該溫度下的平衡常數K =1,試判斷:
CO2(g)+
H2(g),已知CO(g)和H2O(g)的起始濃度均為2 mol·L-1,經測定該反應在該溫度下的平衡常數K =1,試判斷:
(1)當CO轉化率為25%時,該反應是否達到平衡_______,若未達到平衡,向哪個方向進行______。
(2)達到平衡時,CO的轉化率____________________。
(3)當CO的起始濃度仍為2 mol·L-1,H2O(g)的起始濃度為6 mol·L-1,求平衡時CO的轉化率_______。
(1)反應未達平衡 Q=1∕9<K=1,平衡向正反應方向進行。(2)50℅ (3) 75℅。
【解析】
試題分析:(1)當CO轉化率為25%時則{C(CO2)C(H2)}∕{C(CO)C(H2O)}=(0.5×0.5)∕(1.5×1.5)=1∕9<1.所以反應未達到平衡。反應向正反應方向進行。當反應達到平衡時,假設消耗的CO濃度為x,根據反應方程式中各物質的關系可得X2∕(2-X)2=1.解得X=1, CO轉化率為(1∕2)×100℅=50℅。(3)假設在這種條件下,達到平衡時CO消耗了a mol·L-1,則平衡時各物質的濃度為C(CO)=(2- a)mol·L-1 C(H2O)=(6-a)mol·L-1C(CO2)=amol·L-1C(H2)=amol·L-1. a2∕{(2- a)×(6-a)}=1解得a=1.5.所以CO的轉化率為: (1.5∕2) ×100℅=75℅。
考點:考查化學平衡的判斷及反應物轉化率的計算等的知識。


 暑假銜接教材期末暑假預習武漢出版社系列答案
暑假銜接教材期末暑假預習武漢出版社系列答案 假期作業暑假成長樂園新疆青少年出版社系列答案
假期作業暑假成長樂園新疆青少年出版社系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 H2CO3+OH-
H2CO3+OH- H2CO3+OH-
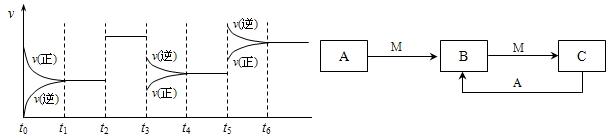
H2CO3+OH- 2SO3△H<0,下圖表示該反應的速率(v)隨時間(t)變化的關系,t2、t3、t5時刻外界條件有所改變,但都沒有改變各物質的初始加入量.下列說法中正確的是
2SO3△H<0,下圖表示該反應的速率(v)隨時間(t)變化的關系,t2、t3、t5時刻外界條件有所改變,但都沒有改變各物質的初始加入量.下列說法中正確的是 2SO3達到平衡后,SO3的體積分數為 a%,SO2的轉化率為m.
2SO3達到平衡后,SO3的體積分數為 a%,SO2的轉化率為m. 查看答案和解析>>
科目:高中化學 來源: 題型:
| A、A的質量不再發生變化 | B、混合氣體的總物質的量不再發生變化 | C、C的分子數目不再發生變化 | D、D的物質的量濃度不再發生變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 催化 |
| t/s | 0 | 500 | 1 000 |
| [H2]/mol?L-1 | 5.00 | 3.52 | 2.48 |
| [CO]/mol?L-1 | 2.50 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com