
【題目】實驗室用下圖所示裝置模擬石灰石燃煤煙氣脫硫實驗:

(1)實驗中為提高石灰石漿液脫硫效率采取的措施是____,寫出通入SO2和空氣發生反應生成石膏(CaSO4·2H2O)的化學方程式____。
(2)將脫硫后的氣體通入KMnO4溶液,可粗略判斷煙氣脫硫效率的方法是____。
(3)研究發現石灰石漿液的脫硫效率受pH和溫度的影響。煙氣流速一定時,脫硫效率與石灰石漿液pH的關系如圖所示,在為5.7時脫硫效果最佳,石灰石漿液5.7<pH<6.0時,煙氣脫硫效果降低的可能原因是____,煙氣通入石灰石漿液時的溫度不宜過高,是因為____。

(4)石灰石煙氣脫硫得到的物質中的主要成分是CaSO4和CaSO3,實驗人員欲測定石灰石漿液脫硫后的物質中CaSO3的含量,以決定燃煤煙氣脫硫時通入空氣的量。請補充完整測定CaSO3含量的實驗方案:取一定量石灰石煙氣脫硫后的物質,____。[漿液中CaSO3能充分與硫酸反應。實驗中須使用的藥品:75%的硫酸、標準濃度的(NH4)2Fe(SO4)2溶液,標準濃度的酸性KMnO4溶液]
【答案】 不斷攪拌、制成漿液 2CaCO3 + 2SO2 + O2 + 4H2O=2 CaSO4·2H2O + 2CO2 高錳酸鉀溶液顏色褪去的快慢 石灰石的溶解度減小,減慢了與SO2的反應 溫度升高SO2的溶解度小 加入足量的75%的硫酸,加熱,將生成的SO2氣體通入一定體積過量的標準濃度的酸性KMnO4溶液,記錄加入KMnO4溶液的體積,充分反應后,用標準濃度的(NH4)2Fe(SO4)2溶液滴定(過量酸性KMnO4溶液),記錄達到滴定終點時消耗(NH4)2Fe(SO4)2溶液的體積,計算得出結果
【解析】分析:(1)根據加快反應速率的條件分析;利用電子守恒、原子守恒寫出化學方程式;(2)用高錳酸鉀溶液檢測SO2的含量;(3)根據影響化學反應速率的因素分析;(4)利用氧化還原滴定的方法測定CaSO3含量。
詳解:(1)實驗中為提高石灰石漿液脫硫效率采取的措施是不斷攪拌、制成漿液;根據電子守恒和原子守恒,寫出通入SO2和空氣發生反應生成石膏(CaSO4·2H2O)的化學方程式2CaCO3 + 2SO2 + O2 + 4H2O=2 CaSO4·2H2O + 2CO2 。
(2)脫硫后的氣體含有少量SO2氣體,通入KMnO4溶液能使高錳酸鉀溶液顏色,因此根據顏色褪去的快慢,可粗略判斷煙氣脫硫效率,本題答案為:高錳酸鉀溶液顏色褪去的快慢。
(3)由脫硫效率與石灰石漿液pH的關系圖知,在為5.7時脫硫效果最佳,pH增大石灰石的溶解度減小,減慢了與SO2的反應;溫度升高SO2的溶解度小,因此,本題正確答案為:石灰石的溶解度減小,減慢了與SO2的反應;溫度升高SO2的溶解度小。
(4)欲測定CaSO3的含量,根據所給實驗藥品,先向樣品中加入足量的75%的硫酸,加熱,將生成的SO2氣體通入一定體積過量的標準濃度的酸性KMnO4溶液,記錄加入KMnO4溶液的體積,充分反應后,用標準濃度的(NH4)2Fe(SO4)2溶液滴定(過量酸性KMnO4溶液),記錄達到滴定終點時消耗(NH4)2Fe(SO4)2溶液的體積,計算得出結果。


科目:高中化學 來源: 題型:
【題目】CH4-CO2催化重整不僅可以得到合成氣(CO和H2),還對溫室氣體的減排具有重要意義。回答下列問題:
(1)CH4-CO2催化重整反應為:CH4(g)+CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol1
C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol1
C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ·mol1
該催化重整反應的ΔH==______ kJ·mol1。有利于提高CH4平衡轉化率的條件是____(填標號)。
A.高溫低壓 B.低溫高壓 C.高溫高壓 D.低溫低壓
某溫度下,在體積為2 L的容器中加入2 mol CH4、1 mol CO2以及催化劑進行重整反應,達到平衡時CO2的轉化率是50%,其平衡常數為_______mol2·L2。
(2)反應中催化劑活性會因積碳反應而降低,同時存在的消碳反應則使積碳量減少。
相關數據如下表:
積碳反應 CH4(g)=C(s)+2H2(g) | 消碳反應 CO2(g)+C(s)=2CO(g) | ||
ΔH/(kJ·mol1) | 75 | 172 | |
活化能/ (kJ·mol1) | 催化劑X | 33 | 91 |
催化劑Y | 43 | 72 | |
①由上表判斷,催化劑X____Y(填“優于”或“劣于”),理由是_________________。在反應進料氣組成、壓強及反應時間相同的情況下,某催化劑表面的積碳量隨溫度的變化關系如圖所示。升高溫度時,下列關于積碳反應、消碳反應的平衡常數(K)和速率(v)的敘述正確的是________填標號)。

A.K積、K消均增加 B.v積減小,v消增加
C.K積減小,K消增加 D.v消增加的倍數比v積增加的倍數大
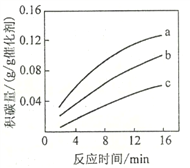
②在一定溫度下,測得某催化劑上沉積碳的生成速率方程為v=k·p(CH4)·[p(CO2)]-0.5(k為速率常數)。在p(CH4)一定時,不同p(CO2)下積碳量隨時間的變化趨勢如圖所示,則pa(CO2)、pb(CO2)、pc(CO2)從大到小的順序為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.在一定條件下aA+bB![]() cC+dD達到平衡時,請填寫:
cC+dD達到平衡時,請填寫:
(1)若A、B、C、D都是氣體,在加壓后平衡向逆反應方向移動,則a、b、c、d關系是__________________。
(2)已知B、C、D是氣體,現增加A的物質的量,平衡不移動,說明A是__________________(填狀態)。
(3)若容器容積不變,加入氣體B,氣體A的轉化率__________________(填“增大”“減小”或“不變”)。
(4)若加熱后,C的百分含量減小,則正反應是__________________反應(填“放熱”或“吸熱”)。
(5)若保持容器壓強不變,且A、B、C、D都是氣體,向容器中充入稀有氣體,則化學平衡正向移動,則a、b、c、d關系是__________________。
Ⅱ.工業上一般采用下列反應合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g)。
CH3OH(g)。
(1)在一定溫度下,將2 mol CO和6 mol H2充入2 L的密閉容器中,充分反應后,達到平衡時測得c(CO)=0.5mol·L-1。該反應的平衡常數K=__________________。
(2)若在一體積可變的容器中充入l molCO、 2mol H2和1mol CH3OH,達到平衡吋測得混合氣體的密度是同溫同壓下起始的1.6倍,則該反應向__________________(填“正”、“逆”)反應方向移動。
(3)若在溫度和容積相同的三個密閉容器中,按不同方式投人反應物,測得反應達到平衡吋的有關數據如下表:
容器 | 反應物投入的量 | 反應物的轉化率 | CH3OH的濃度(mol/L) | 能量變化(Q1、Q2、Q3均大于0) |
1 | 2molCO和4molH2 | a1% | c1 | 放出Q1kJ熱量 |
2 | 2molCH3OH | a2% | c2 | 吸收Q2kJ熱量 |
3 | 4molCO和8molH2 | a3% | c3 | 放出Q3kJ熱量 |
則下列關系正確的是 __________________。
A. c1=c2 B.2Q1=Q3 C.2a1=a3 D.a1 +a2 =1 E.該反應若生成2mol CH3OH,則放出(Q1+Q2)kJ熱量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外活動小組的同學,在實驗室做鋅與濃硫酸反應的實驗中,甲同學認為產生的氣體是二氧化硫,而乙同學認為除二氧化硫氣體外,還可能產生氫氣。為了驗證甲、乙兩位同學的判斷是否正確,丙同學設計了如圖所示實驗裝置(鋅與濃硫酸共熱時產生的氣體為X,且該裝置略去),試回答下列問題:

(1)配平反應的化學方程式為:___Zn + ___H2SO4(濃) = ___ZnSO4 ___SO2 ↑+ ___H2O。
(2)丙同學在安裝好裝置后,必不可少的一步操作是_________________________。
(3)A中加入的試劑可能是___________溶液;
B中加入的試劑可能是____________;
C中發現黑色固體變成紅色,加入的試劑可能是____________。
D中加入的試劑可能是____________。
E中加入的試劑可能是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】抗菌藥奧沙拉秦鈉可通過下列路線合成:

(1)化合物B中的含氧官能團為____、____(寫官能團名稱)。
(2)由D→E的反應類型為____。
(3)寫出C的結構簡式____。
(4)寫出C同時滿足下列條件的一種同分異構體的結構簡式____。
Ⅰ.能發生銀鏡反應; Ⅱ.能與FeCl3溶液發生顯色反應;
Ⅲ.分子中有4中化學環境不同的氫
(5)已知![]() 易被氧化。請寫出以甲醇、苯酚和
易被氧化。請寫出以甲醇、苯酚和![]() 為原料制備
為原料制備![]() 的合成路線流程圖(無機試劑任選,合成路線流程圖示例見本題干)____。
的合成路線流程圖(無機試劑任選,合成路線流程圖示例見本題干)____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國化工專家侯德榜的“侯氏制堿法”為世界制堿工業做出了突出的貢獻,如圖所示是某廠應用“侯氏制堿法”生產純堿的工藝流程圖,據圖回答:
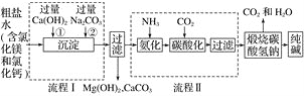
(1)上述流程圖中,可循環利用的物質是____________。
(2)流程Ⅰ后過濾所得濾液中含有的溶質有__________。
(3)流程Ⅱ先通入氨氣,再通入二氧化碳,如果反過來,二氧化碳的吸收率會降低,這是因為___________。
(4)用一個化學反應方程式表示出流程Ⅱ中發生的總反應____。
(5)工業生產純堿的流程中,碳酸化時溶液中先析出碳酸氫鈉而沒有析出氯化銨的原因是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】原子序數依次遞增的A、B、C、D、E五種元素,其中只有E是第四周期元素,A的一種核素中沒有中子,B原子基態時最外層電子數是其內層電子數的2倍,D原子基態時2p原子軌道上有2個未成對的電子,E元素的原子結構中3d能級上未成對電子數是成對電子數的2倍。回答下列問題:
(1)E的+2價離子基態核外電子排布式為____。
(2)A、B、C、D原子中,電負性最大的是____(填元素符號)。
(3)1 mol B2A4分子中σ鍵的數目為____。B4A6為鏈狀結構,其分子中B原子軌道的雜化類型只有一種,則雜化類型為____。
(4)元素B的一種氧化物與元素C的一種氧化物互為等電子體,元素C的這種氧化物的分子空間構型為____。
(5)E和C形成的一種化合物的晶胞結構如圖所示,該化合物的化學式為____。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮元素形成的酸有硝酸、亞硝酸(HNO2)等,其中HNO2為一元弱酸。
(1)寫出HNO2溶液與NaOH溶液反應的離子方程式:___________________。
(2)亞硝酸鈉(NaNO2)像食鹽一樣有咸味,但有很強的毒性,誤食NaNO2會使人中毒。已知亞硝酸鈉能發生如下反應:2NaNO2 + 4HI ═ 2NO↑ + 2NaI + I2 + 2H2O
①用雙線橋標出該反應的電子轉移方向及個數。______
②該反應被氧化的元素是_____,其中被氧化的元素占該元素總量的______(填百分數)。
(3)硝酸鹽可作為煙幕彈。如反應:NH4NO3+Zn=ZnO+N2↑+2H2O,反應中NH4NO3作為_____(填選項)
A.氧化劑 B.還原劑 C.既做氧化劑又做還原劑
(4)實驗室需配制0.1molL﹣1的NH4NO3溶液500mL。
①配制時,應用托盤天平稱取NH4NO3的質量為_________。
②配制中已有托盤天平(帶砝碼和鑷子)、燒杯、藥匙、玻璃棒,還需要的玻璃儀器有_________。
③定容時俯視刻度線,所配得溶液的濃度_____________(填“偏高”、“偏低”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組為認識鐵及其化合物的性質、分散系的性質做了如下一組綜合實驗,根據實驗流程回答相關問題:

(1)請寫出Fe2O3與①反應的離子方程式______________________________。
(2)物質②為_______________。
(3)請寫出FeCl3與鐵粉反應的化學方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最終生成Fe(OH)3濁液,該過程的現象為____________ ,此過程中發生的氧化還原反應為(用化學方程式表達)_________________________。
(5)將FeCl3飽和溶液滴入沸水中,并繼續煮沸至紅褐色,制得分散系③為__________________,它與FeCl3溶液、Fe(OH)3濁液的本質區別是_________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com