
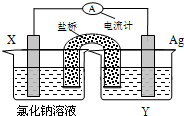
 依據氧化還原反應:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)設計的原電池如圖所示.
依據氧化還原反應:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)設計的原電池如圖所示.

 開心試卷期末沖刺100分系列答案
開心試卷期末沖刺100分系列答案 雙基同步導航訓練系列答案
雙基同步導航訓練系列答案 黃岡小狀元同步計算天天練系列答案
黃岡小狀元同步計算天天練系列答案科目:高中化學 來源: 題型:
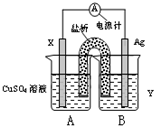 化學科學的重要責任在于認識自然界里存在的各種各樣的、奇妙的化學反應,探索紛繁的化學反應的本質和規律.通過化學反應原理模塊的學習,我們可以比較深刻地理解化學科學的精髓,提高化學學科素養.請根據所學化學反應原理,解決以下問題.
化學科學的重要責任在于認識自然界里存在的各種各樣的、奇妙的化學反應,探索紛繁的化學反應的本質和規律.通過化學反應原理模塊的學習,我們可以比較深刻地理解化學科學的精髓,提高化學學科素養.請根據所學化學反應原理,解決以下問題.| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 根據所學化學反應原理,解決以下問題:
根據所學化學反應原理,解決以下問題:| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:
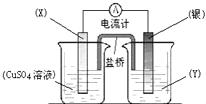 依據氧化還原反應:2Ag+(aq)+Cu(s)?Cu2+(aq)+2Ag(s)設計的原電池如圖所示.下列說法不正確的是( )
依據氧化還原反應:2Ag+(aq)+Cu(s)?Cu2+(aq)+2Ag(s)設計的原電池如圖所示.下列說法不正確的是( )| A、電極X的材料是銅 | B、電解質溶液Y是硝酸銀溶液 | C、銀電極為電池的正極,發生的電極反應為:Ag++e-?Ag | D、鹽橋中的陽離子向硫酸銅溶液中運動 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com