
 =0.3 mol,
=0.3 mol, =0.1mol,所以NO體積是:0.1 mol×22.4 L/mol=2.24 L;
=0.1mol,所以NO體積是:0.1 mol×22.4 L/mol=2.24 L; =0.3mol,所以NO2體積是:0.3 mol×22.4 L/mol=6.72 L;因為得到是混合氣體,因此體積在二者之間,選項B符合.
=0.3mol,所以NO2體積是:0.3 mol×22.4 L/mol=6.72 L;因為得到是混合氣體,因此體積在二者之間,選項B符合.

科目:高中化學 來源: 題型:閱讀理解
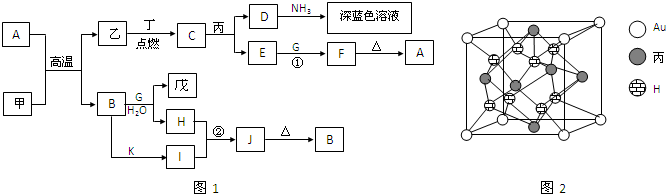




查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2012-2013學年上海市普陀區高三下學期二模化學試卷(解析版) 題型:計算題
金屬及其化合物變化多,用途廣。請完成下列計算:
(1)等物質的量的鎂在氧氣中充分灼燒,產物質量為a g,比它在空氣中灼燒所得產物增重b g。它在空氣中灼燒后的產物中Mg3N2的質量分數是 (用a、b表示,只考慮空氣中氮氣、氧氣參與反應)。
(2)硬鋁(因其主要成分,在此僅看作Al-Cu合金)常用于建筑裝潢。1.18g某種硬鋁恰好與10mL某濃度的硝酸完全反應,生成的混合氣體(其中NO2與NO的體積比為2:1)再與448mL氧氣(標準狀況)混合,恰好能被水完全吸收。
①計算該硝酸的物質的量濃度。
②計算并確定此種硬鋁的化學式。
(3)取5.1g Al-Mg合金與200mL 1mol·L-1的NaOH(aq)充分反應,產生氣體a L。過濾,向濾液中通入V L CO2后開始出現沉淀,繼續通入CO2使沉淀完全。過濾、洗滌、干燥、灼燒,得到固體5.1 g。則a = ,V = 。(氣體體積均為標準狀況)
(4)向Cu、Cu2O和CuO的混合粉末中加入500mL 0.6 mol·L-1 HNO3(aq),恰好完全溶解,同時收集到1120 mL NO(標準狀況)。通過計算推斷混合粉末中Cu的物質的量。
查看答案和解析>>
科目:高中化學 來源:2011年浙江省高考化學模擬試卷(七)(解析版) 題型:選擇題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com