
【題目】電解飽和食鹽水時,下列敘述正確的是
A.正極產生氯氣,負極產生氫氣B.陽極得到的氣體能使碘化鉀溶液變藍
C.在陽極區滴入酚酞試液,溶液顯紅色D.陽極得到氯氣,陰極得到鈉
【答案】B
【解析】
電解飽和食鹽水氯化鈉和水反應生成氫氧化鈉、氫氣、氯氣,反應的化學方程式2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,氯離子在陽極失電子生成氯氣,溶液中氫離子在陰極得到電子生成氫氣。
2NaOH+H2↑+Cl2↑,氯離子在陽極失電子生成氯氣,溶液中氫離子在陰極得到電子生成氫氣。
A. 電解原理為溶液中氯離子在陽極失電子生成氯氣,溶液中氫離子在陰極得到電子生成氫氣,故A錯誤;
B. 陽極得到的氣體是氯氣,能使碘化鉀溶液變藍,故B正確;
C. 陰極溶液中氫離子得到電子生成氫氣,2H++2e-=H2↑,水電離平衡被破壞,向生成OH-的方向移動,附近氫氧根離子濃度增大,在陰極區滴入酚酞試液,溶液顯紅色,故C錯誤;
D. 陽極得到氯氣,陰極得氫氣和氫氧化鈉,故D錯誤;
故選B。


 舉一反三同步巧講精練系列答案
舉一反三同步巧講精練系列答案 口算與應用題卡系列答案
口算與應用題卡系列答案科目:高中化學 來源: 題型:
【題目】I.某溫度時,在一個2L的密閉容器中,X、Y、Z三種氣態物質的物質的量隨時間的變化曲線如圖所示。根據圖中數據,試填寫下列空白:

①該反應的化學方程式為____________________________。
②從開始至2min,Z的平均反應速率為________________。
③若要提高X的轉化率,請提出兩條合理措施_______________________________、____________________________。
II.某探究性學習小組用相同質量的鋅和相同濃度的足量的稀鹽酸反應得到實驗數據如表所示:
實驗編號 | 鋅的狀態 | 反應溫度/℃ | 收集100mL氫氣 所需時間/s |
Ⅰ | 薄片 | 15 | 200 |
Ⅱ | 薄片 | 25 | 90 |
Ⅲ | 粉末 | 25 | 10 |
①該實驗的目的是探究__________、__________對鋅和稀鹽酸反應速率的影響;
②實驗Ⅰ和Ⅱ表明__________,化學反應速率越大;
③能表明固體的表面積對反應速率有影響的實驗編號是 ______ 和 ______ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙酸甲酯的催化醇解反應可用于制備甲醇和乙酸已酯,該反應的化學方程式為:CH3COOCH3(l)+C6H13OH(l)![]() CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
已知v正=k正·x(CH3COOCH3)·x(C6H13OH),v逆=k逆·x(CH3COOC6H13)·x(CH3OH),其中k正、k逆為速率常數(受溫度影響),x為各組分的物質的量分數。反應開始時,CH3COOCH3和C6H13OH按物質的量之比1:1投料,測得338K、343K、348K三個溫度下CH3COOCH3轉化率(α)隨時間(t)的變化關系如圖所示。下列說法正確的是( )

A.該反應的△H>0
B.348K時,該反應的平衡常數為1.8
C.A、B、C、D四點中,v正最大的是D
D.在曲線①、②、③中,k正-k逆最大的曲線是①
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉛蓄電池的充放電反應為Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(1)。某鉛蓄電池的正、負極標記被磨損,試用如困裝置設計實驗,識別出此鉛蓄電池的正、負極。
2PbSO4(s)+2H2O(1)。某鉛蓄電池的正、負極標記被磨損,試用如困裝置設計實驗,識別出此鉛蓄電池的正、負極。
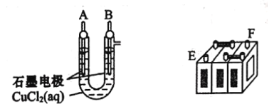
(1)將A接E、B接F,B電極出現_____________現象,電極反應式為_____________,說明F為正極。
(2)鉛蓄電池工作時(放電),E電極的反應式為_____________,充電時該極與外接電源的_____________極相連。
(3)若有0.2mol電子發生轉移,則正極消耗PbO2的物質的量是______mol。
(4)如圖是在金屬鋅板上貼上一張用某溶液浸濕的濾紙。
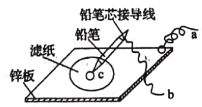
①若用硫酸鈉和酚酞的混合溶液浸濕濾紙,用導線將a、b直接相連,則濾紙出現____色,鉛筆芯c點處的電極反應式為________________。
②若用KI-淀粉溶液浸濕濾紙,用導線將a、b與鉛蓄電池的E、F電極相連,鉛筆芯c點處出現藍色,則b接的是_______(填“E”或“F”)電極。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年諾貝爾化學獎頒給在鋰離子電池發展方面作出突出貢獻的三位科學家,頒獎詞中說:他們創造了一個可再充電的世界。下面是最近研發的Ca-LiFePO4可充電電池的工作示意圖,鋰離子導體膜只允許Li+通過,電池反應為:xCa2++2LiFePO4![]() xCa+2Li1-xFePO4+2xLi+。下列說法錯誤的是
xCa+2Li1-xFePO4+2xLi+。下列說法錯誤的是

A.LiPF6-LiAsF6為非水電解質,其與Li2SO4溶液的主要作用都是傳遞離子
B.放電時,負極反應為:LiFePO4xe===Li1-xFePO4+xLi+
C.充電時,Li1-xFePO4/LiFePO4電極發生Li+脫嵌,放電時發生Li+嵌入
D.充電時,當轉移0.2 mol電子時,左室中電解質的質量減輕2.6 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,水中存在電離平衡:H2O ![]() H++OH-△H>0。下列敘述正確的是
H++OH-△H>0。下列敘述正確的是
A.將水加熱,Kw增大,pH不變
B.向水中加入少量NaOH固體,平衡逆向移動,c(OH-)降低
C.向水中加入少量NH4Cl固體,平衡正向移動,溶液呈堿性
D.向0.1mol/L的醋酸溶液中加入一定量醋酸鈉晶體,溶液中c(OH-)增大,Kw不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列幾種物質:A.石墨和金剛石 B. 35Cl和37Cl C.CH3CH=CHCH3和(CH3)2C=CH2 D.丁烷和新戊烷E. 
(1)屬于同素異形體的是__________________
(2)屬于同位素的是__________________
(3)屬于同分異構體的是__________________
(4)屬于同系物的是__________________
(5)屬于同種物質的是__________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銨明礬[NH4Al(SO4)2·12H2O]是分析化學常用基準試劑,其制備過程如下。下列分析不正確的是( )

A.過程Ⅰ反應:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4
B.檢驗溶液B中陰離子的試劑僅需BaCl2溶液
C.若省略過程Ⅱ,則銨明礬產率明顯減小
D.向銨明礬溶液中逐滴加入NaOH溶液并加熱,先后觀察到:刺激性氣體逸出→白色沉淀生成→白色沉淀消失
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com