
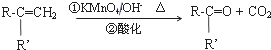
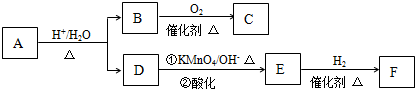
| 3mol |
| 0.5mol |
| 2.5mol×2 |
| 0.5mol |
| 130-12×6-10 |
| 16 |
| 3mol |
| 0.5mol |
| 2.5mol×2 |
| 0.5mol |
| 130-12×6-10 |
| 16 |
| Cu |
| △ |
| Cu |
| △ |
 ,故答案為:
,故答案為: ;
; ,
, ;
; ,
, ;
;

 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
| A、用鋁礬土(主要成分Al2O3)生產金屬鋁 |
| B、用硫鐵礦(主要成分FeS2)生產硫酸 |
| C、用海水、貝殼生產氯化鎂晶體 |
| D、用氯化鈉生產燒堿 |
查看答案和解析>>
科目:高中化學 來源: 題型:
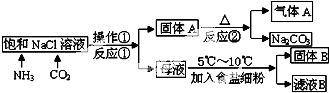
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、若ω1=2ω2,則c1<2c2,V=100ml |
| B、若ω1=2ω2,則c1>2c2,V=100ml |
| C、若c1=2c2,則ω1<2ω2,V>100ml |
| D、若c1=2c2,則,ω1=2ω2,V=100ml |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、鐵和硝酸銀溶液反應:Fe+Ag+=Ag+Fe3+ |
| B、氫氧化鎂與硫酸溶液反應:H++OH-=H2O |
| C、碳酸鈣與醋酸溶液反應:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
| D、鐵與稀硫酸反應:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:
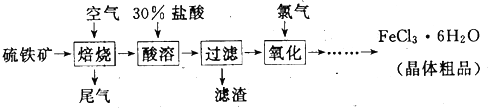
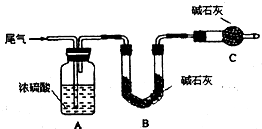
查看答案和解析>>
科目:高中化學 來源: 題型:
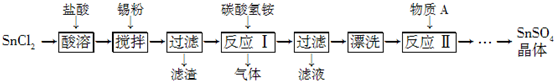
查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗用品 | 溶液溫度 | 中和熱 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.3℃ | |
| ② | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.5℃ | |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com