
【題目】A、B、X、Y、Z、R、Q為前四周期元素,且原子序數依次增大。A是所有元素中原子半徑最小的;B的核外電子排布式為ls22s22p2;X原子單電子數在同周期元素中最多;Y與X同周期,第一電離能比X的低;Z的M層電子數是K層電子數的2倍;R與Y同主族;Q的最外層只有一個電子,其它電子層電子均處于飽和狀態。
回答下列問題:
(1)Q+的核外電子排布式為______,Z的價電子軌道表達式(價電子排布圖)為_______。
(2)化合物XA3中X原子的雜化方式為______;A3Y+的立體構型為______。
(3)① B、Z的最高價氧化物的沸點較高的是______(填化學式),原因是______。
② Y與R的簡單氫化物中Y的熔沸點更高,原因是______。
(4)向Q元素的硫酸鹽溶液中通入足量XA3,充分反應后溶液呈深藍色,該反應的離子方程式為______。
(5)B有多種同素異形體,其中一種同素異形體的晶胞結構如圖,該晶體一個晶胞中B原子數為______,B原子的配位數為______,若晶胞的邊長為apm,晶體的密度為ρg/cm3,則阿伏加德羅常數為______(用含a和p的式子表示)。

【答案】 ls22s22p63s23p63dl0 ![]() sp3 三角錐形 SiO2 SiO2為原子晶體,CO2固體為分子晶體 水分子間存在氫鍵,而H2S分子間只存在范德華力 Cu2++4NH3= [Cu(NH3)4]2+或Cu2++4NH3·H2O=[ Cu(NH3)4]2++4H2O 8 【答題空10】4
sp3 三角錐形 SiO2 SiO2為原子晶體,CO2固體為分子晶體 水分子間存在氫鍵,而H2S分子間只存在范德華力 Cu2++4NH3= [Cu(NH3)4]2+或Cu2++4NH3·H2O=[ Cu(NH3)4]2++4H2O 8 【答題空10】4 ![]()
【解析】A、B、X、Y、Z、R、Q為前四周期元素,且原子序數依次增大。A是所有元素中原子半徑最小的,則A為H元素;B的核外電子排布為1s22s22p2,故B為C元素;Z的M層電子數是K層電子數的2倍,Z是Si;X原子單電子數在同周期元素中最多,則外圍電子排布為ns2np3,原子序數小于Si,Y與X同周期,第一電離能比X的低,則X是N,Y是O;R與Y同主族,R是S;Q的最外層只有一個電子,其他電子層電子均處于飽和狀態,不可能為短周期元素,原子序數小于30,故核外電子排布為1s22s22p63s23p63d104s1,則Q為Cu元素,則
(1)Cu+核外電子排布式為:1s22s22p63s23p63d10;Si的價電子軌道表達式(價電子排布圖)為![]() ;(2)化合物NH3是三角錐形結構,N元素含有一對孤對電子,N原子的雜化方式為sp3雜化;H3O+中中心原子的價層電子對數是
;(2)化合物NH3是三角錐形結構,N元素含有一對孤對電子,N原子的雜化方式為sp3雜化;H3O+中中心原子的價層電子對數是![]() ,含有一對孤對電子,其立體構型為三角錐形。(3)①B、Z的最高價氧化物分別為二氧化碳、二氧化硅,SiO2為原子晶體,CO2為分子晶體,故沸點較高的是 SiO2;②由于水分子間存在氫鍵,而H2S分子間只存在范德華力,因此水的沸點更高;(4)向硫酸銅溶液中通入氨氣,充分反應后溶液呈深藍色,反應生成[Cu(NH3)4]2+,該反應的離子方程式為Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O;(5)碳有多種同素異形體,其中一種同素異形體的晶胞結構如圖,該晶體一個晶胞的C原子數為:4+8×1/8+6×1/2=8;每個C與周圍的4個C原子相鄰,故C原子的配位數為4;若晶胞的邊長為a pm,則晶胞體積為(a×10-10)3cm3,晶體的密度為ρ g/cm3,則晶胞質量為(a×10-10)3cm3×ρ g/cm3=ρa3×10-30ρ g,則8×12/NAg=ρa3×10-30ρ g,故NA=96×1030/a3ρmol-1。
,含有一對孤對電子,其立體構型為三角錐形。(3)①B、Z的最高價氧化物分別為二氧化碳、二氧化硅,SiO2為原子晶體,CO2為分子晶體,故沸點較高的是 SiO2;②由于水分子間存在氫鍵,而H2S分子間只存在范德華力,因此水的沸點更高;(4)向硫酸銅溶液中通入氨氣,充分反應后溶液呈深藍色,反應生成[Cu(NH3)4]2+,該反應的離子方程式為Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O;(5)碳有多種同素異形體,其中一種同素異形體的晶胞結構如圖,該晶體一個晶胞的C原子數為:4+8×1/8+6×1/2=8;每個C與周圍的4個C原子相鄰,故C原子的配位數為4;若晶胞的邊長為a pm,則晶胞體積為(a×10-10)3cm3,晶體的密度為ρ g/cm3,則晶胞質量為(a×10-10)3cm3×ρ g/cm3=ρa3×10-30ρ g,則8×12/NAg=ρa3×10-30ρ g,故NA=96×1030/a3ρmol-1。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】世界環保聯盟建議全面禁止使用氯氣用于飲用水的消毒,而建議采用高效“綠色”消毒劑二氧化氯。二氧化氯是一種極易爆炸的強氧化性氣體,易溶于水、不穩定、呈黃綠色,在生產和使用時必須盡量用稀有氣體進行稀釋,同時需要避免光照、震動或受熱。實驗室以電解法制備 ClO2 的流程如下:
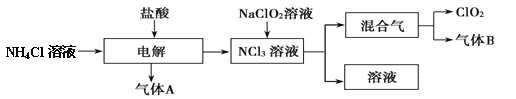
(1)ClO2 中所有原子_____(填“是”或“不是”)都滿足 8 電子結構。上圖所示方法制得的混合氣中雜質氣體 B 能使石蕊試液顯藍色,除去該雜質氣體可選用_____;
A.飽和食鹽水 B.堿石灰 C.濃硫酸 D.蒸餾水
(2)穩定性二氧化氯是為推廣二氧化氯而開發的新型產品。下列說法正確的是_____;
A.二氧化氯可廣泛用于工業和飲用水處理
B.應用在食品工業中能有效地延長食品貯藏期
C.穩定性二氧化氯的出現大大增加了二氧化氯的使用范圍
D.在工作區和成品儲藏室內,要有通風裝置和監測及警報裝置
(3)歐洲國家主要采用氯酸鈉氧化濃鹽酸制備,但該方法缺點是產率低、產品難以分離, 還可能污染環境。寫出該方法發生的化學方程式_____;
(4)我國廣泛采用經干燥空氣稀釋的氯氣與固體亞氯酸鈉(NaClO2)反應制備,化學方程式是______,此法相比歐洲方法的優點是_____。
(5)科學家又研究出了一種新的制備方法,利用硫酸酸化的草酸(H2C2O4)溶液還原氯酸鈉,化學反應方程式為_____,此法提高了生產及儲存、運輸的安全性,原因是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物C是一種藥物的中間體,其合成路線如下圖所示:
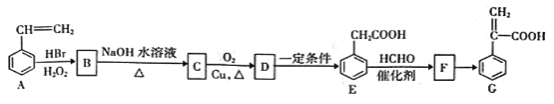
已知:①CH3CH=CH2+HBr![]() CH3CH2CH2Br
CH3CH2CH2Br
②CH3COOH+HCHO![]() HOCH2CH2COOH
HOCH2CH2COOH
回答下列問題:
(1)F中含氧官能團的名稱為_______。
(2)C→D的化學方程式為_______。
(3)D→E、E→F的反應類型分別為_______、_______;F→G的反應條件為_______。
(4)下列說法正確的是_______(填標號)。
a. A中所有原子可能都在同一平面上
b. B能發生取代、加成、消去、縮聚等反應
c.合成路線中所涉及的有機物均為芳香族化合物
d.一定條件下1mol有機物G最多能與4molH2發生反應
(5)化合物F有多種同分異構體,其中同時滿足下列條件的同分異構體的結構簡式為應_______。
① 屬于芳香族化合物,且含有兩個甲基;
② 能發生水解反應和銀鏡反應;
③ 能與FeCl3發生顯色反應;
④ 核磁共振氫譜有4組峰,且峰面積之比為6:2:1:1。
(6)已知:苯環上有烷烴基時,新引入的取代基連在苯環的鄰對位。根據題中的信息,以甲苯為原料合成有機物![]() ,請設計合成路線:_______(無機試劑及溶劑任選)。合成路線流程圖示例如下:
,請設計合成路線:_______(無機試劑及溶劑任選)。合成路線流程圖示例如下:
![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分。表中所列的字母分別代表一種化學元素。

試回答下列問題:
(1)元素p為26號元素,請寫出其原子的三價陽離子的電子排布式:______________。
(2)e與a反應的產物的分子中中心原子的雜化形式為__________,該分子是__________(填“極性”或“非極性”)分子。
(3)請寫出f的氫化物在水中所存在氫鍵的表達式:(任寫兩種即可)_________________________。
(4)o、p兩元素的部分電離能數據列于下表:
元素 | o | p | |
電離能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
比較兩元素的I2、I3可知,氣態o2+再失去一個電子比氣態p2+再失去一個電子難。對此,你的解釋是___________________________________;
(5)i單質晶體中原子的堆積方式如下圖甲所示,其晶胞特征如下圖乙所示,原子之間相互位置關系的平面圖如下圖丙所示。

請問晶胞中i原子的配位數為________,一個晶胞中i原子的數目為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.硬脂酸甘油酯是天然高分子化合物
B.葡萄糖在酒化酶催化下,可以水解為乙醇,這是釀酒的原理
C.濃的硫酸鈉溶液加入雞蛋清中,蛋白質變性而凝聚
D.“離離原上草,一歲一枯榮”,小草富含纖維素,可以用來造紙
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生產、生活密切相關,下列對應關系正確的是
選項 | 性質 | 實際應用 |
A | 活性炭可吸附水中的懸浮物 | 用于自來水的殺菌消毒 |
B | SO2具有還原性 | 漂白紙漿 |
C | 鐵被氧氣氧化時會放出熱量 | 鐵、活性炭、無機鹽、水等的混合物制成曖寶貼 |
D | 氧化鋁是兩性氧化物 | 作耐高溫材料 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. HF的熱穩定性很好,是因為HF分子間存在氫鍵
B. 構成單質分子的粒子之間不一定存在共價鍵
C. 由非金屬元素組成的化合物不一定是共價化合物
D. 陰、陽離子間通過離子鍵一定能形成離子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“瘦肉精”是一種能減少脂肪增加瘦肉的藥品,有很危險的副作用,輕則導致心律不齊,重則導致心臟病。下列關于兩種常見瘦肉精的說法不正確的是( )
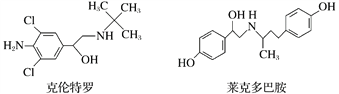
A. 克倫特羅分子的分子式為C12H18ON2Cl2
B. 克倫特羅能發生加成、氧化、消去等反應
C. 克倫特羅和萊克多巴胺可以用FeCl3溶液鑒別
D. 萊克多巴胺與足量NaOH溶液反應,生成物的化學式為C18H20NO3Na3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生在實驗室制取乙酸乙酯的主要步驟如下:①在大試管A中配制反應混合液;②按圖甲所示連接好裝置(裝置氣密性良好),用小火均勻加熱大試管A 5~10 min;③待試管B收集到一定量產物后停止加熱,撤去導管并用力振蕩,然后靜置,待分層;④分離出乙酸乙酯層,洗滌、干燥。

已知:乙醇可以和氯化鈣反應,生成微溶于水的CaCl2·6C2H5OH;無水硫酸鈉易吸水形成硫酸鈉結晶水合物。
有關試劑的部分數據如下:
物質 | 熔點/℃ | 沸點/℃ | 密度/g·cm-3 |
乙醇 | -117.3 | 78.5 | 0.789 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.90 |
濃硫酸(98%) |
| 338.0 | 1.84 |
(1)配制反應混合液的主要操作步驟為_______________________(不必指出液體體積);制取乙酸乙酯的化學方程式為________________。
(2)上述實驗中飽和Na2CO3溶液的作用是________(填字母)。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.減小乙酸乙酯的溶解度,有利于其分層析出
D.加速乙酸乙酯的生成,提高其產率
(3)步驟②中需要小火均勻加熱,其主要原因之一是溫度過高會發生副反應,另一個原因是________________________________________________________。
(4)寫出步驟③中觀察到的現象___________________________。
(5)分離出乙酸乙酯層后,一般用飽和CaCl2溶液洗滌。通過洗滌可除去的雜質是________(填名稱);干燥乙酸乙酯可選用的干燥劑為________(填字母)。
A.P2O5 B.無水硫酸鈉
C.堿石灰 D.NaOH固體
(6)某化學課外小組設計了圖乙所示的制取乙酸乙酯的裝置(圖中鐵架臺、鐵夾、加熱裝置均已略去),與圖甲裝置相比,圖乙裝置的主要優點有________(填字母)。

a.增加了溫度計,有利于控制反應溫度
b.增加了分液漏斗,能隨時補充反應混合液,減少反應物蒸發
c.增加了冷凝裝置,有利于收集產物
d.反應容器容積大,容納反應物的量多
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com