
【題目】一定溫度下,向10 mL H2O2溶液中加入適量FeCl3溶液,反應分兩步進行:
①2Fe3++ H2O2=2Fe2++ O2↑+ 2H+,② H2O2 + 2Fe2+ + 2H+ =2Fe3++2H2O,
反應過程中能量變化如下圖所示。下列說法正確的是( )
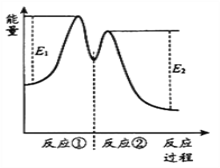
A. 反應②的ΔH=(E2 -E1)kJ·mol-1
B. Fe3+的作用是增大過氧化氫的分解速率
C. 反應2H2O2(aq)=2H2O(l)+O2(g)的△H<0
D. 反應①是放熱反應、反應②是吸熱反應
【答案】BC
【解析】A.焓變=生成物的總能量-反應物的總能量,整個反應2H2O2(aq) = 2H2O(l)+O2(g)的ΔH=E1-E2,反應②的ΔH=②反應的生成物總能量-②反應的反應物總能量。不等于E1-E2,故A錯誤;B.根據總反應2H2O2(aq)=2H2O(l)+O2(g),Fe3+是催化劑,其作用是加快過氧化氫的分解速率,故B正確;C.由圖知反應物的總能量大于生成物的總能量,所以反應2H2O2(aq)=2H2O(l)+O2(g)為放熱反應,故△H<0,故C正確;D.反應①生成物的能量大于反應物的能量是吸熱反應,反應②生成物的能量小于反應物的能量是放熱反應,故D錯誤;答案:BC。


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案科目:高中化學 來源: 題型:
【題目】有關物質的轉化關系如圖1所示.A是黑色非金屬單質,C、E、F均為氧化物,E、F常溫下呈氣態,且E能使品紅褪色,G是一種常見的無色液體,I是一種難溶于水的白色膠狀沉淀,能溶于B溶液.請回答下列問題: 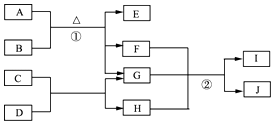
(1)C的化學式為 .
(2)G的電子式為 .
(3)寫出①反應的化學方程式: .
(4)寫出過量的F參加反應時②的離子方程式: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是某課外小組制取乙炔并測定乙炔的某些性質的實驗. 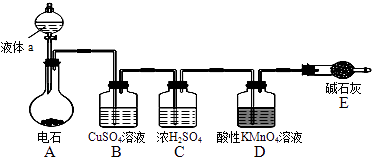
(1)寫出實驗室制取乙炔的化學方程式: .
(2)實驗室制取乙炔時,分液漏斗中的液體a通常是 .
(3)CuSO4溶液的作用是 .
(4)裝置D中的現象是: .
(5)工業上常用乙炔、飽和食鹽水等物質作原料來合成聚氯乙烯,請寫出相關方程式:
; ; ; .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能用H++ OH-= H2O來表示的化學反應是( )
A. CuO溶于稀H2SO4 B. 澄清石灰水和HNO3溶液反應
C. KOH溶液和碳酸溶液反應 D. Ba(OH)2溶液和H2SO4溶液反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.納米材料是指一種稱為“納米”的新物質制成的材料
B.復合材料一般有強度高、質量輕、耐高溫、耐腐蝕等優異性能,其綜合性質超過了單一材料
C.淀粉和纖維素通式都是(C6H10O5)n , 都是天然高分子化合物
D.合成纖維的主要原料是石油、天然氣、煤等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酸鈉是一種重要的化工原料,請回答下列問題:
I.高鐵酸鉀(K2FeO4)溶液呈紫紅色,向其中加入過量亞硝酸鈉后,溶液紫紅色逐漸褪去,并出現紅褐色沉淀,請寫出該反應的離子方程式__________________。
I1.實驗室模擬下圖所示流程制備亞硝酸鈉:

已知: ①氧化過程中,控制反應液溫度在35~60℃條件下主要發生反應:
C6H12O6+ 12HNO3=3HOOC-COOH+9NO2↑+3NO↑+9H2O
②氫氧化鈉溶液吸收NO 和NO2發生反應:
NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O

(1)木屑的主要成分是纖維素,結合已知信息①,你認為向木屑中加稀硫酸的作用是_____ ,氧化過程中反應溫度不宜高于60℃,原因是______________。
(2)不做任何處理,按此過程進行,氫氧化鈉溶液吸收后的溶液中除了OH-外還有兩種陰離子,其中一種是NO2-,NO2-與另一種陰離子的物質的量之比為________。
(3)裝置B用于制備NaNO2,盛裝的試劑除NaOH(aq)外,還可以是_____ (填字母)。
A.NaCl(aq) B.Na2CO3(aq) C.NaNO3( aq )
Ⅲ.測定產品純度:
[實驗步驟] ①準確稱量ag 產品配成200mL溶液
②從步驟①配制的溶液中移取20.00mL 加入錐形瓶中
③用c mol/L酸性KMnO4溶液滴定至終點
④重復以上操作3 次,消耗酸性KMnO4溶液的平均體積為VmL
(1)錐形瓶中發生反應的離子方程式為____________。
(2)產品中NaNO2 的純度為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】今年6月20日,2016年全球最受關注的十大化學成果發布,其中有兩項與空氣中的二氧化碳處理利用技術有關。其一為美國伊利諾斯大學芝加哥分校和阿貢國家實驗室科學家聯合設計的新型太陽能電池,可直接把大氣中的二氧化碳轉化為合成氣(CO和H2)該設計同時具有環保和經濟價值,不僅可以減緩二氧化碳的排放,而且可以生成重要的化工原料。
(1)下列材料也可以用于制造太陽能電池的是____________。
A.Ag2O B.Fe3O4 C.Si D.SiO2
(2)下圖裝置可實現二氧化碳到一氧化碳的轉化

①電源的正極為______(“A”或“B")。
②陰極發生反應的電極方程式為:___________.
(3)CO 和H2可用于合成甲醇。
①已知CO、H2、CH3OH(1)的燃燒熱為283.0kJ/mol、285. 8kJ/mol、726.5kJ/mol,寫出 由CO和H2制備CH3OH(1)的熱化學方程式__________。
②在398K,1L的恒容容器中充入0.1molCO和0.2molH2,發生反應CO(g)+2H2(g)=CH3OH(g),反應過程中氣體的壓強如下表所示(atm為標準大氣壓)。
時間(min) | 0 | 1 | 5 | 10 | 30 | 50 |
壓強(atm) | 10 | 9.3 | 8.0 | 7.2 | 4 | 4 |
5min內該反應的平均速率用CO可表示為______,該溫度下的平衡常數是_____。達到平衡后,向該容器中通入0.05mol的氣態CH3OH,再次達到平衡時,CH3OH的體積分數比原平衡時_____( 填“大”或“小”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列與有機物結構、性質相關的敘述不正確的是( )
A.苯分子中所有原子均在同一平面
B.甲烷是一種無色,有臭味的氣體
C.甲烷和氯氣反應生成一氯甲烷與苯和硝酸反應生成硝基苯的反應類型相同
D.苯不能使溴水因發生化學反應褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數的值,下列說法正確的是( )
A.1molFeCl2與1molCl2反應時轉移的電子數為2NA
B.2g H218O與D216O的混合物中所含電子數目為NA
C.273K,101kPa下,28g乙烯與丙烯混合物中含有C﹣H鍵的數目為5NA
D.pH=1的H2SO3溶液10L,含H+的數目為2NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com