
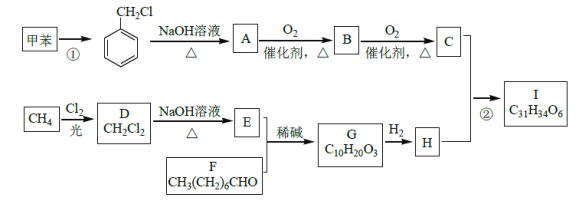
【題目】高血脂是一種常見的心血管疾病,治療高血脂的新藥I的合成路線如圖:
已知:a.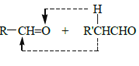
![]()
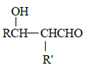
b.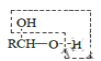
![]() RCHO
RCHO
c.E是甲醛
回答下列問題:
(1)反應①所需試劑、條件分別是___;F的化學名稱為___。
(2)②的反應類型是___;A→B的化學方程式為____。
(3)G的結構簡式為____;H中所含官能團的名稱是___。
(4)化合物W的相對分子質量比化合物C大14,且滿足下列條件,W的可能結構有___種。其中核磁共振氫譜顯示有5種不同化學環境的氫,峰面積比為2:2:2:1:1,寫出符合要求的W的結構簡式___。
①遇FeCl3溶液顯紫色②屬于芳香族化合物③能發生銀鏡反應
(5)設計用甲苯和乙醛為原料制備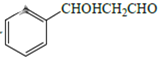 的合成路線,其他無機試劑任選___(合成路線常用的表示方式為:A
的合成路線,其他無機試劑任選___(合成路線常用的表示方式為:A![]() B……
B……![]() 目標產物)
目標產物)
【答案】Cl2、光照 辛醛 取代反應 2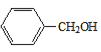 +O2
+O2![]() 2
2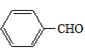 +2H2O
+2H2O 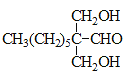 羥基 13
羥基 13 ![]()
![]()
![]()
![]()
【解析】
甲烷和氯氣在光照條件下發生取代反應生成D(CH2Cl2),D在氫氧化鈉的水溶液、加熱條件下發生取代反應,但同一個碳原子上含有兩個羥基不穩定會失水生成醛,則E為HCHO,CH3(CH2)6CHO和甲醛反應生成G,根據題給信息知G為 ,G和氫氣發生加成反應生成H為
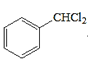
,G和氫氣發生加成反應生成H為 ;甲苯在光照條件下與氯氣發生取代反應生成
;甲苯在光照條件下與氯氣發生取代反應生成![]() ,
,![]() 水解得到A為
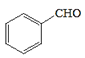
水解得到A為![]() ,A氧化生成B為
,A氧化生成B為![]() ,B進一步氧化生成C為
,B進一步氧化生成C為![]() ,C與H發生酯化反應生成I為
,C與H發生酯化反應生成I為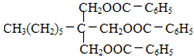 ;
;
(5)苯與氯氣在光照條件下生成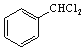 ,然后發生水解反應生成
,然后發生水解反應生成![]() ,最后與乙醛在堿性條件下反應生成目標物。
,最后與乙醛在堿性條件下反應生成目標物。
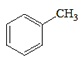
(1)反應①為甲苯和氯氣在光照條件下發生取代反應生成![]() ,該反應所需試劑、條件分別是Cl2、光照;用系統命名法命名F的化學名稱為辛醛;
,該反應所需試劑、條件分別是Cl2、光照;用系統命名法命名F的化學名稱為辛醛;
(2)C與H發生酯化反生成I為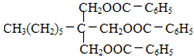 ,則②的反應類型是酯化反應或取代反應;A為
,則②的反應類型是酯化反應或取代反應;A為![]() ,A氧化生成B為
,A氧化生成B為![]() ,A→B的化學方程式為 2
,A→B的化學方程式為 2 +O2
+O2![]() 2
2 +2H2O;
+2H2O;
(3)G 的結構簡式為 ;H 為
;H 為 ,所含官能團的名稱是:羥基;
,所含官能團的名稱是:羥基;
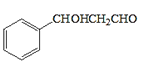
(4)C為![]() ,化合物W的相對分子質量比化合物C大14,W比C多一個CH2,遇FeCl3溶液顯紫色,說明含有酚羥基,說明含有苯環屬于芳香族化合物;能發生銀鏡反應,說明含有醛基;①苯環上有三個取代基,分別為醛基、羥基和甲基,先固定醛基和羥基的位置,鄰間對,最后移動甲基,可得到10種不同結構;②苯環上有兩個取代基,分別為-OH和-CH2CHO,鄰間對位共3種,所以W的可能結構有10+3=13種;其中核磁共振氫譜顯示有5種不同化學環境的氫、峰面積比為2:2:2:1:1,其結構簡式:
,化合物W的相對分子質量比化合物C大14,W比C多一個CH2,遇FeCl3溶液顯紫色,說明含有酚羥基,說明含有苯環屬于芳香族化合物;能發生銀鏡反應,說明含有醛基;①苯環上有三個取代基,分別為醛基、羥基和甲基,先固定醛基和羥基的位置,鄰間對,最后移動甲基,可得到10種不同結構;②苯環上有兩個取代基,分別為-OH和-CH2CHO,鄰間對位共3種,所以W的可能結構有10+3=13種;其中核磁共振氫譜顯示有5種不同化學環境的氫、峰面積比為2:2:2:1:1,其結構簡式:![]() ;
;
(5)苯與氯氣在光照條件下生成 ,然后發生水解反應生成
,然后發生水解反應生成![]() ,最后與乙醛在堿性條件下反應生成目標物,合成路線流程圖為:
,最后與乙醛在堿性條件下反應生成目標物,合成路線流程圖為: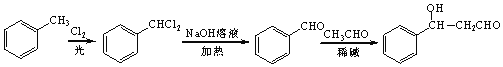 。
。


科目:高中化學 來源: 題型:
【題目】【化學選修3:物質結構與性質】A、B、C、D、E五種元素的原子序數依次增大,其中非金屬元素A的基態原子中成對電子數是未成時電子數的兩倍,C元素在地殼中含量最高,D的單質是短周期中熔點最低的金屬,E的合金是我國使用最早的合金。
(1)E元素的基態原子電子排布式為__________________。
(2)A的某種氫化物A2H2分子中含有___個σ鍵和____個π鍵。
(3)A 的含氧酸根離子AO3n-的空間構型是___________。
(4)B的最簡單的氫化物的沸點比A 的最簡單的氫化物的沸點高得多,其原因是_____。
(5)E的最高價氧化物對應的水化物溶解于氨水中生成的復雜化合物的化學式是______。
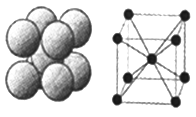
(6)下圖是D單質的晶體堆積方式,這種堆積方式的晶胞中原子的配位數為____,若該原子的半徑為rpm ,此晶體的密度ρ=______g/cm3(用含r的代數式表示,阿伏伽德羅常數用NA表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業制得的氮化鋁(AlN)產品中常含有少量 Al4C3、Al2O3 、C 等雜質。某化學實驗小組設計了如下實驗, 分別測定氮化鋁(AlN)樣品中 AlN 和 Al4C3 的質量分數(忽略NH3在強堿溶液中的溶解)。
(1)實驗原理:
①Al4C3與硫酸發生復分解反應,寫出該反應的化學方程式 ___________。
②AlN溶于強酸產生銨鹽,溶于強堿生成氨氣,請寫出AlN和NaOH溶液反應的化學方程式_______。實驗裝置如下圖所示:
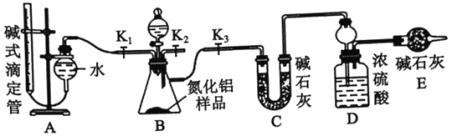
(2)實驗過程:
①根據題干信息:連接實驗裝置,檢查裝置氣密性。稱得D裝置的質量為y g,滴定管的讀數為amL。該步驟中,檢查裝置A氣密性的操作為___________。
②稱取x g AlN 樣品置于錐形瓶中; 塞好膠塞, 關閉活塞K2、K3,打開活塞 K1,通過分液漏斗加入足量的____(填化學式),與錐形瓶內物質充分反應。
③待反應進行完全后,關閉活塞K1,打開活塞K3, 通過分液漏斗加入過量_________(填化學式),與錐形瓶內溶質充分反應。
④_____(填入該步應進行的操作)。
⑤實驗中記錄滴定管的讀數為b mL,稱得D裝置的質量為z g。
(3)數據
①AlN 的質量分數為____________。
②若讀取滴定管中氣體的體積時,先冷卻到室溫,再__________,然后平視凹液面讀數。液面左高右低,則所測氣體的體積___________(填“偏大”“偏小”或“無影響”)。
③Al4C3的質量分數為 ____________(該實驗條件下氣體摩爾體積為Vm molL-1) 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.  與
與![]() 含有相同的官能團,互為同系物
含有相同的官能團,互為同系物
B. 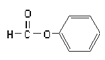 屬于醛類,官能團為-CHO
屬于醛類,官能團為-CHO
C. ![]() 的名稱為:2-乙基-1-丁烯
的名稱為:2-乙基-1-丁烯
D. ![]() 的名稱為:2-甲基-1,3-二丁烯
的名稱為:2-甲基-1,3-二丁烯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子在給定條件下一定能大量共存的是
A.強酸性溶液中:H+、NO![]() 、SO
、SO![]()
B.pH=12的溶液中:OH-、K+、Cl-、HCO![]()
C.加入鋁粉能放出氫氣的溶液中一定存在:NH![]() 、NO
、NO![]() 、AlO
、AlO![]() 、SO
、SO![]()
D.25C時pH=7的無色溶液中:Na+、Cl-、SO![]() 、K+
、K+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】歷史上曾利用“地康法”制氯氣,其原理是以氯化銅作催化劑,利用氧氣氧化氯化氫。如圖為“地康法”制氯氣的模擬裝置.下列關有說法不正確的是
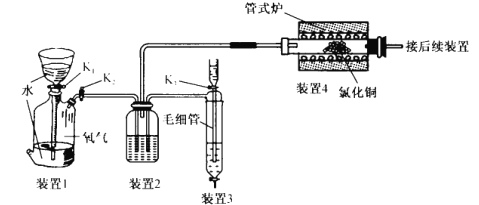
A.關閉 K2打開K1, 若漏斗中的液面不持續下降 ,則裝置1的氣密性良好
B.打開K3 ,將濃鹽酸逐滴滴入濃硫酸中可制備反應所需要的氯化氫
C.裝置 2 中盛放的是濃硫酸,通過觀察氣泡逸出的快慢可判斷氣體的通入量
D.后續需要凈化氯氣的裝置中 ,除雜試劑依次為飽和食鹽水、堿石灰
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】環戊二烯基鐵[ Fe(C5H5)2]是一種有機過渡金屬化合物,常溫下為橙黃色粉末,難溶于水,易溶于有機溶劑,溫度超過100 °C能夠升華,實驗室制備環戊二烯基鐵的裝置和步驟如下:
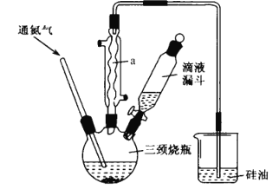
實驗步驟:
步驟1:在三頸燒瓶中加入10mL乙二醇二甲醚(作溶劑)和4. 5 g研細的 KOH 粉末,通入氮氣并開啟磁力攪拌器 ,然后加入1. 5mL環戊二烯(過量);
步驟2:將1.5g FeCl24H2O溶于5 mL二甲基亞砜中 ,并轉入滴液漏斗中,將步驟1中的混合物猛烈攪拌10 min,打開滴液漏斗將氯化亞鐵的二甲基亞砜溶液在45 min鐘左右滴完;
步驟3:關閉滴液漏斗,在氮氣保護下繼續攪拌30 min;
步驟4:將反應后的混合液倒入100 m L燒杯內,加入少量鹽酸除去剩余的KOH,再加入20mL 水,繼續攪拌懸濁液15min,抽濾產物,并用水洗滌產物3~4次,最后將產物鋪在面皿上,置于真空干燥器內干燥。回答下列問題:
(1)儀器a的作用是___________________。
(2)制備過程中若不通入氮氣,會降低環戊二烯基鐵的產率,試分析其中的原因: __________。
(3)硅油的主要作用是______。
(4)步驟4中分離環戊二烯基鐵也可采用如下方法,請將分離步驟補充完整:向反應后的混合液加入10 mL乙醚(ρ= 0.71g cm-3 ) 充分攪拌,然后轉入_____(填儀器名稱)中,依次用鹽酸、水各洗滌兩次,待液體分層后_____________(填完整操作過程),將含有二環戊二烯基合鐵的溶液在通風櫥中蒸發得到二環戊二烯基合鐵粗產品。
(5)可采用如圖所示的簡易裝置分離提純環戊二烯基鐵。將顆粒狀環戊二烯基鐵放入蒸發皿中并小火加熱,環戊二烯基鐵在扎有小孔的濾紙上凝結,該分離提純方法的名稱是_______________,裝置棉花的作用是___________。
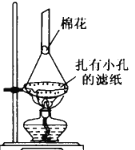
(6)若最終制得環戊二烯基鐵質量為 0.16g,則產率為_____%(保留一位小數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式如圖所示,它可以發生反應的類型有( )
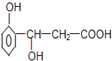
①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚
A. ①②③④B. ①②④⑤
C. ①②⑤⑥D. ③④⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是
A.向NH4HSO4溶液中滴加NaOH溶液至水的電離程度最大:2OH-+NH4++H+=NH3·H2O+H2O
B.硫酸型酸雨久置,pH減小:![]()
C.將Cl2通入少量FeBr2溶液中:2Fe2++Cl2=2Fe3++2Cl-
D.4mol·L-1的NaAlO2溶液和7mol·L-1的鹽酸等體積混合:![]() +7H++H2O=3Al(OH)3↓+Al3+
+7H++H2O=3Al(OH)3↓+Al3+
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com