


 開心蛙狀元作業系列答案
開心蛙狀元作業系列答案 課時掌控隨堂練習系列答案
課時掌控隨堂練習系列答案 一課一練一本通系列答案
一課一練一本通系列答案 浙江之星學業水平測試系列答案
浙江之星學業水平測試系列答案科目:高中化學 來源: 題型:
| A、H3PO2中,P元素的化合價為+1價 |
| B、在溶液中Ag+氧化H3PO2為H3PO4時,氧化劑與還原劑的物質的量之比為4:1 |
| C、次磷酸在水中的電離方程式為H3PO2?H++H2PO2- |
| D、NaH2PO2屬于酸式鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:
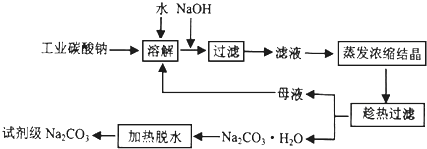
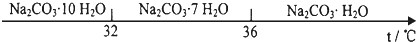
查看答案和解析>>
科目:高中化學 來源: 題型:
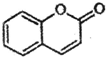 ) 是一種存在于某些植物的果、花等中的天然香料.又知:
) 是一種存在于某些植物的果、花等中的天然香料.又知: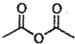 ;
;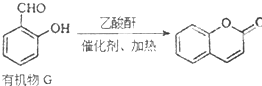
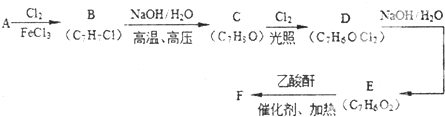
 (是一種常用有機溶劑)的合成路線流程圖(無機試劑任用).合成路線流程圖示例如下:
(是一種常用有機溶劑)的合成路線流程圖(無機試劑任用).合成路線流程圖示例如下:| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化學 來源: 題型:
 W、X、Y、Z是四種常見的短周期元素,其原子半徑隨原子序數變化如下圖所示.已知W的一種核素的質量數為18,中子數為10;X和Ne原子的核外電子數相差1;Y的最高價氧化物的對應水化物是一種強酸;Z的非金屬性在同周期主族元素中最強.
W、X、Y、Z是四種常見的短周期元素,其原子半徑隨原子序數變化如下圖所示.已知W的一種核素的質量數為18,中子數為10;X和Ne原子的核外電子數相差1;Y的最高價氧化物的對應水化物是一種強酸;Z的非金屬性在同周期主族元素中最強.查看答案和解析>>
科目:高中化學 來源: 題型:
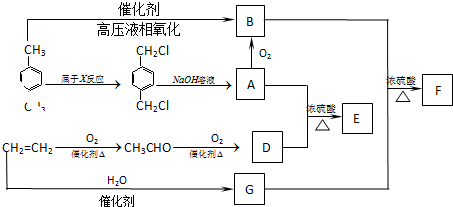
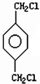 →A:
→A:查看答案和解析>>
科目:高中化學 來源: 題型:
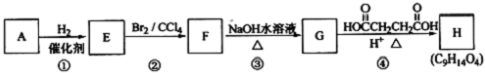
查看答案和解析>>
科目:高中化學 來源: 題型:

| 氯氣 |
| 熱空氣或 |
| 水蒸氣 |
| 堿液 |
| 吸收 |
| 酸化 |
| 蒸餾 |
| 煅燒 |
| 水 |
| 海水 |
| 過濾 |
| 灼燒 |
| 熔化 |
| 電解 |
| 放電 |
| 水 |
| 吸收 |
| 一定 |
| 條件下 |
| 合成塔 |
| 過量氮氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:
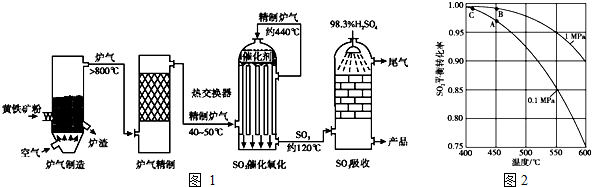
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com