
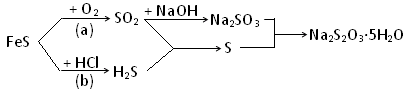
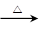 2Fe2O3+4SO2、Na2SO3+S
2Fe2O3+4SO2、Na2SO3+S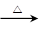 Na2S2O3
Na2S2O3| | 第一份 | 第二份 | 第三份 |
| 樣品的質量/g | 7.54 | 15.08 | 35.00 |
| 二氧化硫的體積/L | 0.672 | 1.344 | 2.688 |
| 硫的質量/g | 0.80 | 1.60 | 3.20 |
 2Fe2O3+4SO2, FeS+2HCl=FeCl2+H2S↑.2H2S +SO2=3S+2H2O.SO2+2NaOH=Na2SO3+ H2O;Na2SO3+S
2Fe2O3+4SO2, FeS+2HCl=FeCl2+H2S↑.2H2S +SO2=3S+2H2O.SO2+2NaOH=Na2SO3+ H2O;Na2SO3+S Na2S2O3。若恰好完全反應,則Na2SO3:S=1:1,根據方程式進行逆推,可得到FeS在反應(a)和(b)中的理論分配比為2:1。
Na2S2O3。若恰好完全反應,則Na2SO3:S=1:1,根據方程式進行逆推,可得到FeS在反應(a)和(b)中的理論分配比為2:1。 Na2S2O3可知Na2SO3:S=1:1。假設產生的Na2SO3的物質的量為x.由于NaOH溶液吸收SO2的吸收率為96%,反應消耗的SO2的物質的量為x÷0.96.其余的S完全(1- x÷0.96)完全轉化為S單質, 1- x÷0.96=x.解得x=0.4898.所以得到的Na2S2O3·5H2O質量為:0.4898mol×248g/mol=121.5 g。
Na2S2O3可知Na2SO3:S=1:1。假設產生的Na2SO3的物質的量為x.由于NaOH溶液吸收SO2的吸收率為96%,反應消耗的SO2的物質的量為x÷0.96.其余的S完全(1- x÷0.96)完全轉化為S單質, 1- x÷0.96=x.解得x=0.4898.所以得到的Na2S2O3·5H2O質量為:0.4898mol×248g/mol=121.5 g。

科目:高中化學 來源:不詳 題型:問答題

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
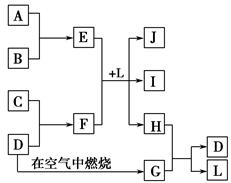
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.②③④⑥ | B.②④⑤⑥ | C.①②④⑤ | D.③④⑤⑥ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.NaHCO3和Al(OH)3 | B.BaCl2和NaCl |
| C.KClO3和K2SO4 | D.Na2SO3和BaCO3 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
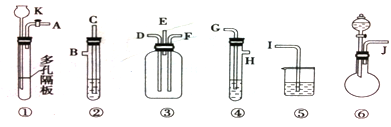
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 Na2S2O3
Na2S2O3
 2NaI+Na2S4O6。產品中的Na2S2O3·5H2O的純度為 %。
2NaI+Na2S4O6。產品中的Na2S2O3·5H2O的純度為 %。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.將蔗糖加入濃硫酸后變黑,說明濃硫酸具有脫水性 |
| B.濃硫酸可用作氣體干燥劑,說明濃硫酸具有吸水性 |
| C.銅與濃硫酸共熱有刺激性氣味氣體放出,說明濃硫酸具有強氧化性 |
| D.常溫下濃硫酸可以用鋁罐儲存,說明鋁與冷的濃硫酸不反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com