
【題目】有機物A蒸氣的密度是相同條件下氫氣密度的29倍,5.8 g A在氧氣中完全燃燒生成13.2 g CO2和5.4 g H2O。
(1)請通過計算確定A的分子式_______。(寫出計算過程)
(2)已知A的1H核磁共振氫譜如下圖所示,則A的結構簡式為______________________。
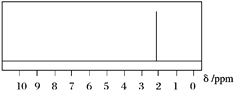
(3)已知B、C都是A的同分異構體。
①若B可發生銀鏡反應,則此反應的化學方程式為__________________________________。
②若C無甲基且可與金屬鈉反應,則C的結構簡式為______________________________。
【答案】C3H6O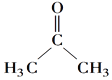 CH3CH2CHO+2Ag(NH3)2OH
CH3CH2CHO+2Ag(NH3)2OH![]() CH3CH2COONH4+2Ag↓+3NH3+H2OCH2===CH—CH2OH(或
CH3CH2COONH4+2Ag↓+3NH3+H2OCH2===CH—CH2OH(或![]() —OH)
—OH)
【解析】
(1)有機化合物的蒸汽的密度是同條件下氫氣的29倍,有機物的相對分子質量=29×2=58,5.8 g A的物質的量n(A)=5.8g÷58g/mol=0.1mol,燃燒生成13.2 g CO2的物質是量為n(CO2)=13.2g÷44/mol=0.3mol,5.4 g H2O的物質的量為n(H2O)=5.4g÷18g/mol=0.3mol,則有機物中碳原子個數N(C)=0.3÷0.1=3,氫原子個數N(H)=0.3×2÷0.1=6,氧原子個數N(O)=(58-3×12-6×1)÷16=1,故A的分子式為C3H6O;(2)核磁共振氫譜只有一個吸收峰,則6個H原子等效,所以是丙酮,故答案為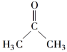 ;(3)①若B可發生銀鏡反應,說明分子中含有醛基,B為丙醛,反應方程式為CH3CH2CHO+2Ag(NH3)2OH
;(3)①若B可發生銀鏡反應,說明分子中含有醛基,B為丙醛,反應方程式為CH3CH2CHO+2Ag(NH3)2OH![]() CH3CH2COONH4+2Ag↓+3NH3+H2O;②C無甲基且可與金屬鈉反應,則C的結構簡式中含有一個羥基,其結構可能為CH2=CH—CH2OH(或
CH3CH2COONH4+2Ag↓+3NH3+H2O;②C無甲基且可與金屬鈉反應,則C的結構簡式中含有一個羥基,其結構可能為CH2=CH—CH2OH(或![]() —OH)。
—OH)。


科目:高中化學 來源: 題型:
【題目】2017年5月4日《光明日報》報道稱,中科院大連化學物理研究所的研究團隊利用多功能催化劑首次實現了CO2直接加氫制汽油的過程。其轉化過程如圖所示。
![]()
下列說法正確的是( )
A. 反應①的產物中含有水
B. 反應②為化合反應
C. 所制得汽油的主要成分是烴和烴的含氧衍生物
D. 這種人造汽油用作汽車的燃料時,汽車尾氣不含氮氧化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖甲中①②③④表示不同化學元素所組成的化合物,圖乙表示由四個單體構成的化合物。以下說法不正確的是( )
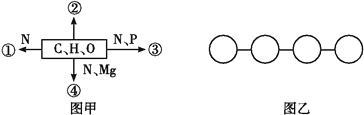
A. 若圖甲中的②大量存在于皮下和內臟器官周圍等部位,則②是脂肪
B. 若圖甲中④能吸收、傳遞和轉換光能,則④可用無水乙醇提取
C. 圖乙中若單體是氨基酸,則該化合物徹底水解后的產物中氧原子數增加3個
D. 圖乙中若單體是四種脫氧核苷酸,則該化合物徹底水解后的產物有5種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】香料茉莉酮是一種人工合成的有機化合物,其結構簡式為![]() ,下列關于茉莉酮的說法正確的是( )
,下列關于茉莉酮的說法正確的是( )
A. 該有機物的化學式是C10H14O
B. 1 mol該有機物與H2充分反應,消耗4 mol H2
C. 該有機物屬于不飽和酮類物質,能發生銀鏡反應
D. 該有機物能發生加成反應,但不能發生氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉬酸鈉晶體(Na2MoO4·2H2O)常用于制造阻燃劑和無公害型冷水系統的金屬抑制劑。下圖是利用鉬精礦(主要成分是MoS2,含少量PbS等)為原料生產鉬酸鈉晶體的工藝流程圖:

回答下列問題:
(1)提高焙燒效率的方法有____________。(寫一種)
(2)“焙燒”時MoS2轉化為MoO3,該反應過程的化學方程式為________________________,氧化產物是________(寫化學式)。
(3)“堿浸”時含鉬化合物發生的主要反應的化學方程式為__________________________。
(4)若“除重金屬離子”時加入的沉淀劑為Na2S,則廢渣成分的化學式為________。
(5)測得“除重金屬離子”中部分離子的濃度:c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L。“結晶”前需先除去SO42-,方法是加入Ba(OH)2固體。假設加入Ba(OH)2固體后溶液體積不變,當SO42-完全沉淀(c(SO42-)≤1.0×10-5mol/L)時,BaMoO4是否會析出?____________________________________。(請計算說明)[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8]
(6)鉬精礦在堿性條件下,加入NaClO溶液,也可以制備鉬酸鈉,同時有SO42-生成,該反應的離子方程式為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(化學-物質結構與性質)氮及其化合物廣泛存在于自然界中,回答下列問題:
(1)在基態15N原子的p能級上存在_____個自旋方向相同的電子;CN—中σ鍵與π鍵數目之比為_____。
(2)堿性肥料氰氨化鈣(CaCN2)的組成元素中第一電離能最小的是_______(填名稱)。
(3)化合物(CH3)3N能溶于水,其原因是____________________________________,(CH3)3N與鹽酸反應生成[(CH3)3NH]+,該過程新生成的化學鍵類型為_______________。
(4)陽離子[(CH3)3NH]+和陰離子A按個數比4:1組成化合物,陰離子A的結構如下圖所示,則s原子的雜化軌道類型是__________,陰離子A的化學式為_______________。
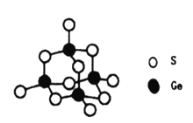
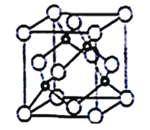
(5)立方氮化硼晶胞如下圖所示(白球為氮原子,黑球為硼原子),則硼原子的配位數為___;若晶胞邊長為acm,則立方氮化硼的密度是______g·cm-3(只要求列算式,阿伏加德羅常數用NA表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據報道,某些建筑材料會產生放射性同位素氡22286Rn,從而對人體產生危害。該同位素原子的中子數和核外電子數之差為
A. 136 B. 50 C. 86 D. 222
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】歸納法是高中化學學習常用的方法之一,某化學研究性學習小組在學習了《化學反應原理》后作出了如下的歸納總結,其中正確的是
①常溫下,pH=3的醋酸溶液與pH=11的NaOH溶液等體積混合,則有c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②對已建立化學平衡的某可逆反應,當改變條件使化學平衡向正反應方向移動時,生成物的百分含量一定增加
③常溫下,AgCl在同物質的量濃度的CaCl2和NaCl溶液中的溶解度相同
④常溫下,已知醋酸電離平衡常數為Ka;醋酸根水解平衡常數為Kh;水的離子積為Kw;則有:Ka·Kh=Kw
⑤電解精煉銅時,電解質溶液中銅離子濃度不變 。
A.①④ B.①②④ C.①②④⑤ D.①②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有A、B、C、D、E五種短周期元素,已知相鄰的A、B、C、D四種元素原子核外最外層共有24個電子,在周期表中的位置如圖所示.E的單質可與酸反應,1molE單質與足量酸作用,在標準狀況下能產生33.6LH2;E的陽離子與A的陰離子核外電子層結構完全相同
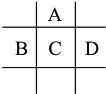
回答下列問題:
(1) A與E形成的化合物的化學式是__________.B的最高價氧化物化學式為_____________,
(2)D的單質與水反應的方程式為__________________________________________________.
(3) 向D與E形成的化合物的水溶液中滴入燒堿溶液直至過量,觀察到的現象是___________________:有關反應的離子方程式為:_____________________________________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com